
【题目】25℃,101KPa 下,将 V L 氯化氢气体溶于水得 V L 水溶液,关于该溶液的叙述正确的是
A.溶液的物质的量浓度为 1 mol/LB.溶液中 c(H+)= ![]() mol/L
mol/L
C.溶液中水分子数和 H+数之比为 1:1D.溶液的物质的量浓度稍小于![]() mol/L
mol/L
【答案】D
【解析】
25℃、1.01×105pa时气体摩尔体积大于22.4L/mol,故VLHCl的物质的量<![]() mol,
mol,
A. 所得溶液体积为VL,故溶液物质的量浓度<![]() mol/L,故A错误;
mol/L,故A错误;
B. VLHCl的物质的量<![]() mol,溶液的体积为V L,根据c=
mol,溶液的体积为V L,根据c=![]() ,溶液中c(H+)=c(HCl)<
,溶液中c(H+)=c(HCl)<![]() mol/L,故B错误;
mol/L,故B错误;
C. 常温下水的密度为1g/cm3,水的质量约是1000Vg,水物质的量约为![]() =
=![]() mol,而n(H+)=n(HCl) <
mol,而n(H+)=n(HCl) <![]() mol,则溶液中水分子数与H+数之比一定不是1:1,故C错误;
mol,则溶液中水分子数与H+数之比一定不是1:1,故C错误;
D. VLHCl的物质的量<![]() mol,所得溶液体积为VL,根据c=
mol,所得溶液体积为VL,根据c=![]() ,故溶液物质的量浓度<
,故溶液物质的量浓度<![]() mol/L,故D正确;
mol/L,故D正确;
答案选D。


 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案科目:高中化学 来源: 题型:
【题目】某工厂的氨氮废水中主要含有![]() ,可用电化学氧化法加以处理。
,可用电化学氧化法加以处理。
(1)图1是电化学氧化法的原理示意图。a的电极反应式是_____________。
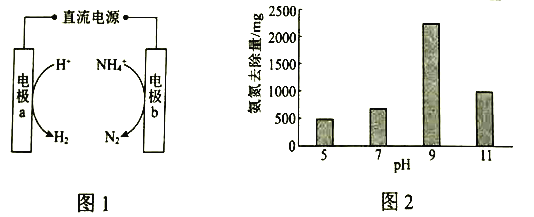
(2)研究显示,其他条件不变时,不同![]() 下氨氮的去除量如图2所示。已知:
下氨氮的去除量如图2所示。已知:![]() 与
与![]() 相比,在电极表面的吸附效果更好。结合平衡移动原理和图中数据,解释
相比,在电极表面的吸附效果更好。结合平衡移动原理和图中数据,解释![]() 从5到9时氨氮去除量增大的原因:______________。
从5到9时氨氮去除量增大的原因:______________。
(3)在电解废水的过程中,![]() 会经历“
会经历“![]() ”的过程。其他条件相同、
”的过程。其他条件相同、![]() 的浓度不同时,废水中氨氮脱除效率的实验结果如下:
的浓度不同时,废水中氨氮脱除效率的实验结果如下:
| 400 | 100 |
电解时间/h | 0.5 | 0.5 |
氨氮脱除效率/( | 2.40.8 |
①其它条件相同、适当提高![]() 的浓度,可以显著增大废水中
的浓度,可以显著增大废水中![]() 的脱除效率。
的脱除效率。
用化学用语解释原因:____________、![]() 。
。
②图2中,![]() 时,废水中
时,废水中![]() 去除量下降,可能的原因是:_______________。
去除量下降,可能的原因是:_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z是第ⅠA~ⅦA族的三种非金属元素,它们在元素周期表中的位置如图所示,试回答下列问题。
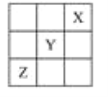
(1)X元素单质的化学式是________。
(2)Y元素的原子结构示意图是____________,Y与Na所形成化合物的电子式为________________________。
(3)Z元素的名称是________,从元素原子得失电子的角度看,Z元素具有________性;若从Z元素在元素周期表中所处位置看,它具有这种性质的原因是_________________________,其价电子排布式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种浓差电池如图所示,阴、阳离子交换膜交替放置,中间的间隔交替充以河水和海水,选择性透过Cl-和Na+,在两电极板形成电势差,进而在外部产生电流。下列关于该电池的说法错误的是( )
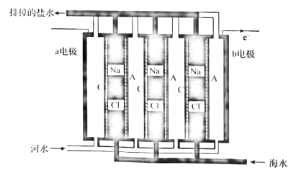
A. a电极为电池的正极,电极反应为![]()
B. A为阴离子交换膜,C为阳离子交换膜
C. 阳极(负极)隔室的电中性溶液通过阳极表面的氧化作用维持
D. 该电池的缺点是离子交换膜价格昂贵,电极产物也没有经济价值
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用![]() 与
与![]() 反应制备KI固体,装置如图所示。实验步骤:①检查装置的气密性;②关闭K,在各装置中加入相应试剂,向装置B中滴入30%的KOH溶液,制得
反应制备KI固体,装置如图所示。实验步骤:①检查装置的气密性;②关闭K,在各装置中加入相应试剂,向装置B中滴入30%的KOH溶液,制得![]() ;③打开K,通入
;③打开K,通入![]() 直至饱和可制得KI,同时有黄色沉淀生成;④关闭K,向所得溶液滴入稀硫酸,水浴加热,充分逸出
直至饱和可制得KI,同时有黄色沉淀生成;④关闭K,向所得溶液滴入稀硫酸,水浴加热,充分逸出![]() ;⑤把装置B中混合液倒入烧杯,为除去硫酸,加入足量碳酸钡,再经过一系列操作可得成品。下列有关该实验的叙述错误的是( )
;⑤把装置B中混合液倒入烧杯,为除去硫酸,加入足量碳酸钡,再经过一系列操作可得成品。下列有关该实验的叙述错误的是( )
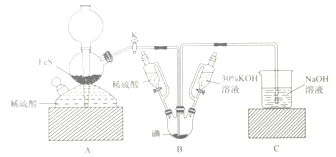
A. 步骤②可观察到固体溶解,溶液由棕黄色变为无色
B. 步骤③装置B中发生反应的离子方程式为![]()
C. 装置C中氢氧化钠溶液的作用是吸收硫化氢
D. 步骤⑤中一系列操作为过滤,洗涤,合并滤液和洗液,蒸馏
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的化学用语表达正确的是( )
A. 乙烯的结构简式:CH2CH2 B. 羟基的电子式:![]()
C. 甲醇的球棍模型:![]() D. 乙酸的实验式:CH3COOH
D. 乙酸的实验式:CH3COOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ba(OH)2 是一种强碱,可用于测定天然气中 CO2 的含量。
(1)CO2 的密度比空气______(填“大”或“小”)
(2)①称取5.25g 试样[含有 Ba(OH)2xH2O 和杂质]配成 100 mL 溶液,配制溶液中用到的仪器有天平、药匙、量筒、烧杯、玻璃棒、______、胶头滴管。用 15.00 mL 0.2 mol/L盐酸与上述 Ba(OH)2 溶液反应,消耗该 Ba(OH)2溶液 10.00 mL(杂质不与酸反应)
②另取5.25 g 试样加热至失去全部结晶水(杂质不分解),称得剩余固体质量为3.09 g, 求 Ba(OH)2xH2O中的 x=______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烃的衍生物A的化学式为C6H12O2,已知:
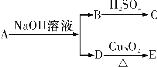
又知D不与Na2CO3反应,C和E均不能发生银镜反应,则A的结构可能有( )
A. 1种 B. 2种 C. 3种 D. 4种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值。下列说法正确的是
A. 2L 0.5mol/L亚硫酸溶液中含有的H+离子数为2NA
B. 室温下,1L pH=13的NaOH溶液中,由水电离的OH-离子数目为0.1NA
C. 电解精炼铜的过程中,每转移NA个电子时,阳极溶解铜的质量为32g
D. 某密闭容器中盛有0.1mol N2和0.3mol H2,在一定条件下充分反应,转移电子的数目小于0.6NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com