
·ÖĪö £Ø1£©øł¾ŻŹµŃé·¢Éś×°ÖĆ”ś³żŌÓ×°ÖĆ”śŠŌÖŹ¼ģŃé×°ÖĆ”śĪ²Ęų“¦Ąķ×°ÖĆÅÅŠņ£»
£Ø2£©ÉÕĘæÖŠÅØŃĪĖįÓė¶žŃõ»ÆĆĢŌŚ¼ÓČČĢõ¼žĻĀ·“Ӧɜ³ÉĀČĘų”¢ĀČ»ÆĆĢŗĶĖ®£»
£Ø3£©øł¾Ż»ģŗĻĘųĢåµÄ³É·Ö¼°ÅØĮņĖį”¢ĒāŃõ»ÆÄĘ”¢±„ŗĶŹ³ŃĪĖ®µÄŠŌÖŹ·ÖĪö£»
£Ø4£©ŅĄ¾ŻĀČĘų²»¾ßÓŠĘư׊Ō£¬“ĪĀČĖį¾ßÓŠĘư׊Ō½ā“š£»
£Ø5£©ĀČĘųÓėĒāŃõ»ÆÄĘČÜŅŗ·“Ӧɜ³ÉĀČ»ÆÄĘ”¢“ĪĀČĖįÄĘŗĶĖ®£®
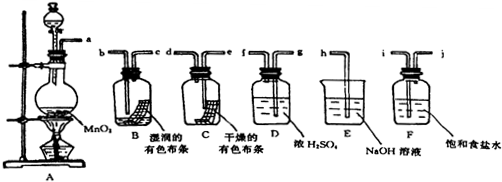
½ā“š ½ā£ŗ£Ø1£©ŹŌŃé×°ÖƵÄĮ¬½ÓĖ³ŠņĪŖ£ŗ·¢Éś×°ÖĆ”ś³żŌÓ×°ÖĆ”śŠŌÖŹ¼ģŃé×°ÖĆ”śĪ²Ęų“¦Ąķ×°ÖĆ£»ŅņĪŖŹÕ¼ÆµÄŹĒĘųĢ壬ĖłŅŌ³żŌÓ×°ÖĆÖŠ³¤µ¼¹Ü½ųĘų£¬¶Ģµ¼¹Ü³öĘų£»ŅņĪŖ±„ŗĶŹ³ŃĪĖ®ÖŠÓŠĖ®£¬ÅØĮņĖįÓŠĪüĖ®ŠŌ£¬ĖłŅŌĻČĮ¬½Ó±„ŗĶŹ³ŃĪĖ®×°ÖĆŗóĮ¬½ÓÅØĮņĖį×°ÖĆ£»ŹŌŃéøÉŌļµÄCl2ŗĶ³±ŹŖµÄCl2ÓŠĪŽĘư׊Ō£¬ŅņĪŖŹŖČóµÄÓŠÉ«²¼ĢõÓŠĖ®·Ö£¬ĖłŅŌD×°ÖĆĻČĮ¬½ÓCŗóĮ¬½ÓB£¬Ė³ŠņĪŖa”śi”śj”śg”śf”śe”śd”śb”śc”śh£¬
¹Ź“š°øĪŖ£ŗi£»j£»g£»f£»e£»d£»b£»c£»h£»
£Ø2£©ÉÕĘæÖŠÅØŃĪĖįÓė¶žŃõ»ÆĆĢŌŚ¼ÓČČĢõ¼žĻĀ·“Ӧɜ³ÉĀČĘų”¢ĀČ»ÆĆĢŗĶĖ®£¬·½³ĢŹ½£ŗMnO2+4HCl£ØÅØ£©$\frac{\underline{\;\;”÷\;\;}}{\;}$MnCl2+Cl2”ü+2H2O£»
¹Ź“š°øĪŖ£ŗMnO2+4HCl£ØÅØ£©$\frac{\underline{\;\;”÷\;\;}}{\;}$MnCl2+Cl2”ü+2H2O£»
£Ø3£©ÅØŃĪĖįÓŠ»Ó·¢ŠŌ£¬ÅØŃĪĖįÖŠµÄĖ®ŌŚ¼ÓČȵÄĢõ¼žĻĀ±ä³ÉĖ®ÕōĘų£¬ĖłŅŌĀČĘųÖŠ»ģÓŠĀČ»ÆĒāŗĶĖ®ÕōĘų£»ÅØĮņĖįÓŠĪüĖ®ŠŌ£¬ĒŅ²»ŗĶĀČĘų·“Ó¦£¬ĖłŅŌæÉÓĆÅØĮņĖįøÉŌļĀČĘų£»ĀČĘųÓŠ¶¾£¬ĪŪČ¾»·¾³£¬ĖłŅŌ²»ÄÜÖ±½ÓÅÅæÕ£»ĀČĘųÄÜŗĶĒāŃõ»ÆÄĘ·“Ӧɜ³ÉĀČ»ÆÄĘ”¢“ĪĀČĖįÄĘŗĶĖ®£¬ĖłŅŌæÉÓĆĒāŃõ»ÆÄĘČÜŅŗĪüŹÕ¶ąÓąµÄĀČĘų£»ĀČ»ÆĒā¼«Ņ×ČÜÓŚĖ®£¬ĀČĘųÄÜČÜÓŚĖ®£¬ĒŅÓėĖ®·“Ó¦£¬Cl2+H2O=H++Cl-+HClO£¬Ź³ŃĪĖ®ČÜŅŗÖŠµÄĀČĄė×ÓŅÖÖĘĀČĘųµÄČܽā£¬½µµĶĀČĘųµÄČܽā¶Č£¬ĖłŅŌæÉÓƱ„ŗĶµÄŹ³ŃĪĖ®³żČ„HClĘųĢ壮
¹Ź“š°øĪŖ£ŗĪüŹÕĖ®ÕōĘų£¬øÉŌļCl2£»ĪüŹÕ¶ąÓąµÄĀČĘų£»³żČ„HClĘųĢ壻
£Ø4£©ĀČĘųÄÜĖ®·“Ó¦£¬·“Ó¦·½³ĢŹ½ĪŖ£ŗCl2+H2O=H++Cl-+HClO£¬CĘæÖŠµÄ³É·ÖŹĒĀČĘų£¬²»ÄÜŹ¹ÓŠÉ«²¼ĢõĶŹÉ«£¬BBĘæÖŠÓŠ“ĪĀČĖįÉś³É£¬Ź¹ÓŠÉ«²¼ĢõĶŹÉ«£¬ŅŌÉĻŹĀŹµĖµĆ÷ĘšĘÆ°××÷ÓƵÄĪļÖŹŹĒ“ĪĀČĖį£®
¹Ź“š°øĪŖ£ŗÓŠÉ«²¼Ģõ²»ĶŹÉ«£»ÓŠÉ«²¼ĢõĶŹÉ«£»“ĪĀČĖį£ØHClO£©£»
£Ø5£©ĀČĘųÓėĒāŃõ»ÆÄĘČÜŅŗ·“Ӧɜ³ÉĀČ»ÆÄĘ”¢“ĪĀČĖįÄĘŗĶĖ®£¬»Æѧ·½³ĢŹ½£ŗCl2+2NaOH=NaCl+NaClO+H2O£¬¹Ź“š°øĪŖ£ŗCl2+2NaOH=NaCl+NaClO+H2O£®
µćĘĄ ±¾Ģāæ¼²éĮĖĀČĘųµÄŹµŃéŹŅÖʱøŗĶĀČĘųŠŌÖŹµÄ¼ģŃ飬Ć÷Č·ĘųĢåÖʱøŌĄķ¼°ø÷×°ÖĆ×÷ÓĆŹĒ½āĢā¹Ų¼ü£¬²ąÖŲæ¼²éѧɜ·ÖĪöĪŹĢā”¢½ā¾öĪŹĢāµÄÄÜĮ¦£¬ĢāÄæÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĀĮÄÜÓėĖłÓŠµÄĖįŗĶ¼ī·“Ó¦·Å³öĒāĘų | |
| B£® | ÓĆ¾Ę¾«µĘĶāŃę¼ÓČČĀĮ²£¬æÉŅŌ擵½ÉŁĮæŅŗµĪŠü¶ų²»Ā䣬ĖµĆ÷ĀĮµÄČŪµć±ČŃõ»ÆĀĮøß | |
| C£® | ĀĮŗĻ½šÖŹĒį£¬Ēæ¶Č“ó£¬ÄĶøÆŹ“£¬æÉŅŌÓĆ×÷ĆÅ“° | |
| D£® | ĒāŃõ»ÆĀĮÄÜČÜÓŚ°±Ė® |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĀČ»ÆÄĘČÜŅŗĻŌÖŠŠŌ£¬æÉÓĆĀĮÖĘČŻĘ÷Öü“ęĀČ»ÆÄĘČÜŅŗ | |
| B£® | SO2¾ßÓŠĘư׊Ō£¬æÉŹ¹×ĻÉ«ŹÆČļŹŌŅŗĶŹĪŖĪŽÉ« | |
| C£® | ¶”“ļ¶ūŠ§Ó¦ŹĒĒų·Ö½ŗĢåŗĶČÜŅŗµÄŅ»ÖÖ³£ÓĆĪļĄķ·½·Ø | |
| D£® | ŌŚŹµŃéŹŅĄļ£¬³£ÓƵē½ā±„ŗĶŹ³ŃĪĖ®µÄ·½·ØÖĘČ”ĀČĘų |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ģ¼ŗĶŠæ | B£® | ĢśŠā | C£® | Ģ¼ŗĶĀĮ | D£® | Ģ¼ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ģå»ż | B£® | Ō×ÓŹż | C£® | ÖŹĮæ | D£® | ĆÜ¶Č |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Na2CO3 NH4Cl CH3COOH H2SO4 | |
| B£® | Na2CO3 H2SO4 CH3COOH NH4Cl | |
| C£® | NH4Cl H2SO4 CH3COOH Na2CO3 | |
| D£® | NH4Cl CH3COOH H2SO4 Na2CO3 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com