
分析 (1)氮气与氢气在高温、高压、催化剂条件下生成氨气;
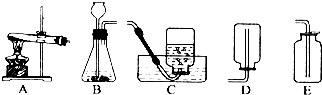
(2)依据反应物状态和反应条件选择合适的发生装置;
(3)依据反应物状态和反应条件选择合适的发生装置;依据氨气密度小于空气密度,极易溶于水,选择收集装置,氨气为碱性气体,遇到湿润的红色石蕊试纸变蓝,据此检验是否收集满;
解答 解:(1)氮气与氢气在高温、高压、催化剂条件下生成氨气,化学方程式:N2+3H2$?_{催化剂}^{高温高压}$2NH3;
在实验室难达到高温和高压的条件,所以该小组的同学没有选择第一种方法制取氨气;
故答案为:N2+3H2$?_{催化剂}^{高温高压}$2NH3;在实验室难达到高温和高压的条件;
(2)第二种方法:向浓氨水中加入生石灰生成氨气,反应物为固体和液体,反应条件不需要加热,所以应选择装置:B;
故答案为:B;
(3)用第三种方法制取氨气,方程式为:2NH4Cl+Ca(OH)2=$\frac{\underline{\;\;△\;\;}}{\;}$2NH3↑+2H2O+CaCl2,反应物为固体与液体,反应条件为加热,所以应选择A装置制备;
氨气密度小于空气密度,极易溶于水,只能选择向下排空气法收集,故选:D;
氨气为碱性气体,遇到湿润的红色石蕊试纸变蓝,可以用来检验氨气是否收集满;
故答案为:A;D;2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$2NH3↑+2H2O+CaCl2;湿润的红色石蕊试纸放在瓶口,若变蓝则收集满;
点评 本题考查了氨气的制备方法、收集方法,明确氨气制备原理和氨气的性质是解题关键,注意发生装置的选择应该依据反应物状态和反应条件,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 从溴水中提取溴,可加入酒精作萃取剂 | |
| B. | 萃取操作完成后,静置分液,上、下层液体均从下口放出 | |
| C. | 用一种有机溶剂,提取水溶液中的某物质,静置分液后,“水层”应在上层 | |
| D. | 萃取时,所加入的溶剂应与原溶剂互不相溶,且与溶质相互间不反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4LCHCl3中含有的氯原子的数目为3NA | |
| B. | 25℃、101kPa下,16gO3和O2混合气体中含有的氧原子数为NA | |
| C. | 等质量的N2和CO所含分子数相同且均为NA | |
| D. | 一定温度下,1L 1mol•L-1的CH3COONa溶液含NA个CH3COO- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 金属镍及其化合物在合金材料以及催化剂等方面应用广泛.
金属镍及其化合物在合金材料以及催化剂等方面应用广泛. 、④HCHO,其中碳原子采取sp2杂化的分子有①③④(填物质序号),HCHO分子的立体结构为平面三角形.
、④HCHO,其中碳原子采取sp2杂化的分子有①③④(填物质序号),HCHO分子的立体结构为平面三角形.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 复合材料由基体和增强体组成,其中基体起骨架作用,增强体起黏结作用 | |
| B. | 玻璃钢是玻璃纤维增强树脂,具有很好的耐腐蚀性,在排水工程中有广泛应用 | |
| C. | 碳纤维增强金属基复合材料具有很高的强度,可用于制作飞机的机翼和机身 | |
| D. | 碳纤维增强陶瓷保持了陶瓷的耐高温的特性,可用于飞机机身的隔热材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 增大氧气浓度 | B. | 升高反应温度 | C. | 增大木炭的量 | D. | 将炭磨成炭粉 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
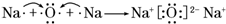 .A、B两种元素还可以形成A2B2型化合物,写出该化合物的电子式
.A、B两种元素还可以形成A2B2型化合物,写出该化合物的电子式 .
.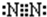 ;
; ;
;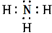 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com