
��9�֣�Ư���������ҵ��������;�㷺��Ư�۳��˾���Ư�������⣬����ɱ��������2003�꿹���ǵ䡱�ڼ䣬���̳�Ư�ۼ�����Ư�ײ�Ʒ��һ��������
��1��1998�꣬�ҹ�����������ɻ����������˰��겻�����ش��ˮ���������������ˮ��������Ư�۵�ҩƷ������������ã��Է���Ⱦ����������ƿװƯ�۾��ÿ����л�ʧЧ�����û�ѧ����ʽ��ʾƯ���ڿ�������ʧЧ��ԭ��
�� �� ��
��2����֪Ũ����ʹ�������ܷ������·�Ӧ��Ca(ClO)2 +4HCl��Ũ��===CaCl2+2Cl2��+2H2O
������ܾõ�Ư����Ũ�����Ƶõ������У������е����������ǣ� ��
��CO2 ��HCl ��H2O ��O2
A���٢ڢ� B�� �ڢۢ� C���ڢ� D���٢�
��3����Cl2��ʯ��������Ư�۵�Ŀ���ǣ� ��
A�� ת��Ϊ��HClO�ȶ����״��˵����� B�� ת��Ϊ��������ˮ������
C�� ��������������� D����ǿƯ������
��4����Cl2��ʯ��������Ư�۵ķ�Ӧ����ʽ
����Ч�ɷ��� �������ƣ���
��1����CO2+Ca��ClO��2+H2O=CaCO3+2HClO ��2HClO  2HCl+O2������2��A����3��A;��4��Cl2+2Ca��OH)2=CaCl2+Ca(ClO)2+2H2O,������ƣ�
2HCl+O2������2��A����3��A;��4��Cl2+2Ca��OH)2=CaCl2+Ca(ClO)2+2H2O,������ƣ�
��������
�����������1��Ư�۾��ÿ����У���ˮ��������̼��Ӧ����̼��ƺʹ����ᣬ������ֽ��ʹ��Ư��ʧЧ�������ķ�ӦΪCO2+Ca��ClO��2+H2O=CaCO3+2HClO��2HClO  2HCl+O2�����ʴ�Ϊ��CO2+Ca��ClO��2+H2O=CaCO3+2HClO��2HClO
2HCl+O2�����ʴ�Ϊ��CO2+Ca��ClO��2+H2O=CaCO3+2HClO��2HClO  2HCl+O2������2���ú�CaCO3��Ca(ClO)2��Ũ������Cl2��Cl2�б�Ȼ����CO2��H2O��HCl�����ʣ���ѡA����3��HClO�����ֽ⣬���״��棬����������ʯ���鷴Ӧ���ɴ�����ƣ�ת��Ϊ��HClO�ȶ����״��˵����ʣ���ѡA����4��������ʯ���鷴Ӧ�����Ȼ��ơ�������ƺ�ˮ������ʽΪCl2+2Ca��OH)2=CaCl2+Ca(ClO)2+2H2O,��Ч�ɷ�Ϊ������ƣ��ʴ�ΪCl2+2Ca��OH)2=CaCl2+Ca(ClO)2+2H2O,������ƣ�
2HCl+O2������2���ú�CaCO3��Ca(ClO)2��Ũ������Cl2��Cl2�б�Ȼ����CO2��H2O��HCl�����ʣ���ѡA����3��HClO�����ֽ⣬���״��棬����������ʯ���鷴Ӧ���ɴ�����ƣ�ת��Ϊ��HClO�ȶ����״��˵����ʣ���ѡA����4��������ʯ���鷴Ӧ�����Ȼ��ơ�������ƺ�ˮ������ʽΪCl2+2Ca��OH)2=CaCl2+Ca(ClO)2+2H2O,��Ч�ɷ�Ϊ������ƣ��ʴ�ΪCl2+2Ca��OH)2=CaCl2+Ca(ClO)2+2H2O,������ƣ�
���㣺Ư�۵��Ʊ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����������и�һ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
����ȷ��ʾ���л�ѧ��Ӧ�����ӷ���ʽ����
A������������Һ������ķ�Ӧ��OH?��H+ �� H2O
B��̼�������ϡ�����У�CaCO3��2H+��Ca2+��H2O��CO2?
C��CH3COOH��Һ��NH3��H2O��Һ��Ӧ��H����OH��===H2O
D�������ʯ��ˮ��ϡ���ᷴӦ��Ca(OH)2 + 2H+ = Ca2+ + 2H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�긣��ʡ�ĵ���У�߶���ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
���й�����Ҫͨ����ܽ��е���(����)
�ٵ��롡�ڵ�ơ��۵�⡡�ܵ绯ѧ��ʴ���ݵ�Ӿ
A���٢ڡ��� B���ڢۢ� C���ڢ� D��ȫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�긣��ʡ�ĵ���У��һ��ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
���и������������еķ����������ǡ�
A����״����11.2 L����B��17g������NH3����
C��1.204��1024��H2O���� D��0. 8mol����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�긣��ʡ�ĵ���У��һ��ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
�����й���������Ӧ�ĵ�λ�����ﲻ��ȷ����
A��Ħ��������g��mol-1B���ܶȣ�g��mL-1��
C������Ħ�������L D�������ӵ�������mol -1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�긣��ʡ�����и�һ��ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��ҵ������ĵ�һ����Ӧ�����û�ѧ����ʽ��ʾ���£�4FeS2+11O2=2Fe2O3+8SO2
�Դ˷�Ӧ����˵������ȷ���ǣ���
A��FeS2�������������ǻ�ԭ��
B��O2ֻ��������
C����������ֻ��Fe2O3
D��4molFeS2������Ӧʱ����Ӧ�й���22mol����ת��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�긣��ʡ�����и�һ��ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��NAΪ�����ӵ�������ֵ������˵������ȷ����
A�������Ħ��������NA��������ӵ���������ֵ�����
B��NA����������NA������ӵ������ȵ���16��1
C��28�˵�������ԭ����Ϊ4NA
D����״���£�0��5NA���ȷ�����ռ���Ϊ11��2L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����ʡ��һ9���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
������Һ��Cl��Ũ����С���ǣ� ��
A��200mL 2mol/L MgCl2��ҺB��1000mL 2.5mol/L NaCl��Һ
C��300mL 5mol/L KCl��ҺD��250mL 1mol/L AlCl3��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�������и߶���ѧ��9�����Ÿ�ϰ��ѧ�Ծ��������棩 ���ͣ�ѡ����
����ʵ����������߱仯��ȷ���ǣ� ��
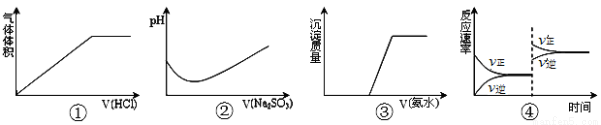
A���ٱ�ʾNa2CO3��Һ�е���ϡ����
B���ڱ�ʾ��ˮ�е���Na2SO3��Һ
C���۱�ʾAgNO3��Һ�е��백ˮ
D���ܱ�ʾһ��������2SO2+O2 2SO3 ��H<0��ƽ��������¶�
2SO3 ��H<0��ƽ��������¶�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com