
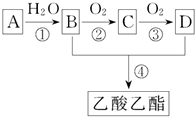
 一股淡淡清香能给人心旷神怡的感觉,主要由香精、酒精和水构成的香水备受爱美人士的青睐.香精里面含有酯类物质,工业上以A为主要原料来合成乙酸乙酯,其合成路线如图所示.其中A是石油裂解气的主要成分,A的产量通常用来衡量一个国家的石油化工水平.又知
一股淡淡清香能给人心旷神怡的感觉,主要由香精、酒精和水构成的香水备受爱美人士的青睐.香精里面含有酯类物质,工业上以A为主要原料来合成乙酸乙酯,其合成路线如图所示.其中A是石油裂解气的主要成分,A的产量通常用来衡量一个国家的石油化工水平.又知| 催化剂 |
| △ |
| 催化剂 |
| Cu |
| △ |
| Cu或Ag |
| △ |
 CH3COOCH2CH3+H2O,生成乙酸乙酯.
CH3COOCH2CH3+H2O,生成乙酸乙酯.| 催化剂 |
| 催化剂 |
| Cu或Ag |
| △ |
| Cu或Ag |
| △ |
 CH3COOCH2CH3+H2O,
CH3COOCH2CH3+H2O, CH3COOCH2CH3+H2O;
CH3COOCH2CH3+H2O;


科目:高中化学 来源: 题型:

| A、迷迭香酸属于芳香烃 |
| B、1mol迷迭香酸最多能和含6mol NaOH的水溶液完全 |
| C、迷迭香酸可以发生水解反应、取代反应和酯化反应 |
| D、1mol迷迭香酸最多能和9mol氢气发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

 ,②R-CN
,②R-CN R-COOH
R-COOH 制备高分子化合物
制备高分子化合物 的合成路线流程图
的合成路线流程图
查看答案和解析>>
科目:高中化学 来源: 题型:
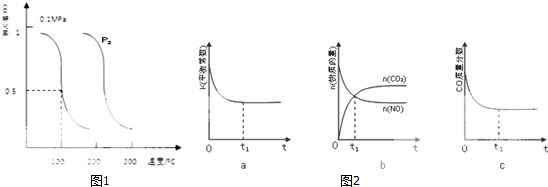
| 容器 | A | B | C |
| 反应物投入量 | 1molCO2(g)和 3molH2(g) | 1molCH3OH(g)和 1molH2O(g) | 2molCO2(g)和6mol H2(g) |
| CH3OH(g)浓度(mol/L) | c1 | c2 | c3 |
| 反应能量变化 | 放出29.4kJ | 吸收a kJ | 放出b kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com