
| A、LiH与D2O反应,所得氢气的摩尔质量为4g/mol | B、1mol LiAlH4 125℃完全分解,转移电子数为3NA | C、LiAlH4溶于适量水得到无色溶液,则化学方程式为:LiAlH4+2H2O═LiAlO2+4H2↑ | D、LiAlH4与乙醛作用生成乙醇,LiAlH4作还原剂 |


 应用题作业本系列答案
应用题作业本系列答案科目:高中化学 来源: 题型:
 ,回答下列问题
,回答下列问题查看答案和解析>>
科目:高中化学 来源: 题型:
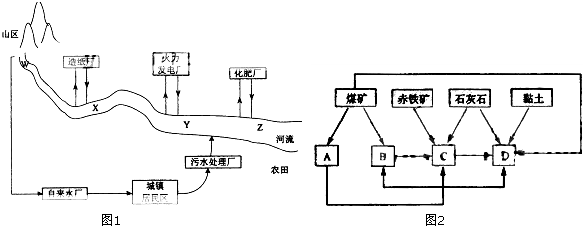
| 地点 项目 | W | X | Y | Z |
| 水温/℃ | 15 | 18 | 26 | 25 |
| pH | 6 | 8 | 5 | 5 |
| 溶解氧量/(mg?L-1) | 11 | 9 | 7 | 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、事物的性质总是在不断地发生变化 | B、元素周期表中最右上角的氦元素是得电子能力最强的元素 | C、ⅠA族元素的失电子能力肯 定比同周期ⅡA族元素的失电子能力强 | D、物质发生量变到一定程度必然引起质变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、AlCl3溶液中滴入过量NaOH溶液 | B、Fe2(SO4)3溶液中加入过量铁粉 | C、稀HNO3中加入少量铜片 | D、Ca(ClO)2溶液中通入过量CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na2O2、Cl2、SO2依次属于电解质、单质、非电解质 | B、1molNa2O2和水反应,转移电子数目为2mol | C、等物质的量的Cl2和SO2同时通入品红溶液,褪色更快 | D、在Na2O2中阴阳离子所含的电子数目相等 |
查看答案和解析>>
科目:高中化学 来源:2015届广东省湛江市高三第一次月考理综化学试卷(解析版) 题型:选择题
下列实验操作、现象和解释都正确的是
选项 | 实验操作 | 现象 | 解释 |
A. | 向某溶液中加入盐酸 | 产生无色气体 | 溶液中一定含有CO32? |
B. | 新制Fe(OH)2露置于空气中一段时间 | 白色固体迅速变为灰绿色,最终变为红褐色 | 说明Fe(OH)2易被氧化成Fe(OH)3 |
C. | 在CuSO4溶液中加入KI溶液,再加入苯,振荡 | 上层呈紫红色,下层有白色沉淀生产 | 铜离子可以氧化碘离子,白色沉淀可能为CuI |
D. | 向某无色溶液中滴加硝酸酸化的BaCl2溶液 | 产生白色沉淀 | 溶液中一定含有SO42- |
查看答案和解析>>
科目:高中化学 来源:2015届广东省惠州市高三第二次调研考试化学试卷(解析版) 题型:选择题
下列装置、试剂选用或操作正确的是
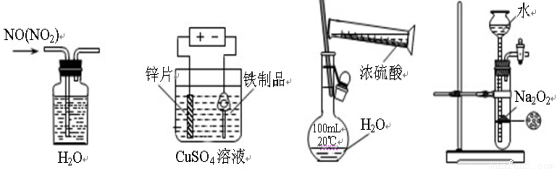
A.除去NO中的NO2 B.铁制品表面镀锌 C.稀释浓硫酸 D.制备少量O2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com