
分析 (1)根据n=$\frac{V}{{V}_{m}}$计算HCl物质的量,再根据c=$\frac{n}{V}$计算盐酸的物质的量浓度;
(2)根据n=$\frac{m}{M}$计算Zn的物质的量,根据方程式计算需要HCl的物质的量,再根据V=$\frac{n}{c}$计算需要盐酸的体积.
解答 解:(1)标况下3.36L HCl的物质的量为$\frac{3.36L}{22.4L/mol}$=0.15mol,盐酸的物质的量浓度为$\frac{0.15mol}{0.025L}$=6mol/L,
答:该盐酸的物质的量浓度为6mol/L;
(2)19.5g Zn的物质的量为$\frac{19.5g}{65g/mol}$=0.3mol,根据方程式:Zn+2HCl=ZnCl2+H2↑,可知需要HCl的物质的量为0.3mol×2=0.6mol,故需要盐酸的最小体积为$\frac{0.6mol}{6mol/L}$=0.1L,
答:需要该盐酸的最小体积为0.1L.
点评 本题考查物质的量有关计算、化学方程式计算,比较基础,有利于基础知识的巩固.


 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案科目:高中化学 来源: 题型:解答题
| 族 周期 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
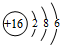 ,硒(Se)是人体必需的微量元素,与⑧同一主族且比⑧原子多一个电子层,则Se的原子序数为34.
,硒(Se)是人体必需的微量元素,与⑧同一主族且比⑧原子多一个电子层,则Se的原子序数为34.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ④①②③ | B. | ④②①③ | C. | ②④①③ | D. | ④①③② |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | R一定是一种盐 | B. | R一定是一种强碱 | ||
| C. | R一定是离子化合物 | D. | R可能是强酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
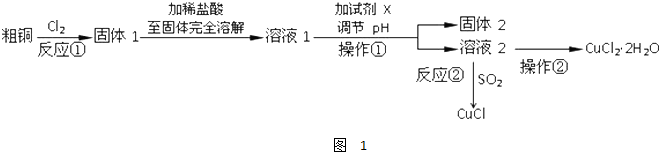

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ClO3-的空间构型为平面三角形 | |
| B. | SiF4 和 SO32-的中心原子均为 sp3 杂化 | |
| C. | 在所有的元素中,氟的第一电离能最大 | |
| D. | C2H5OH 分子中共含有 8 个极性键,1 个 π 键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
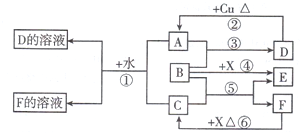
 .根据图中信息,B、C、X的氧化性由强到弱的顺序是MnO2>Cl2>H2O2(用化学式表示).
.根据图中信息,B、C、X的氧化性由强到弱的顺序是MnO2>Cl2>H2O2(用化学式表示).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com