
【题目】化合物甲(由氮和另一种常见的主族元素组成)是一种新型无机材料.将8.2g甲溶于足量的氢氧化钠溶液,可产生标准状况下为4.48L的气体,该气体可作制冷剂.向反应后的溶液中逐滴加入稀盐酸,产生白色沉淀质量最大为15.6g,继续滴加沉淀消失.则甲溶于氢氧化钠的化学方程式为
【答案】AlN+NaOH+H2O=NaAlO2+NH3↑
【解析】解:化合物甲(由氮和另一种常见的主族元素组成),溶于足量的氢氧化钠溶液,产生的气体可作制冷剂为氨气,产生标准状况下为4.48L的气体,n(NH3)= ![]() =0.2mol,反应后的溶滚中逐滴加入稀盐酸,先沉淀后沉淀为溶解,为铝的化合物的特征,产生白色沉淀质量最大为15.6g,为氢氧化铝,n[Al(OH)3]=
=0.2mol,反应后的溶滚中逐滴加入稀盐酸,先沉淀后沉淀为溶解,为铝的化合物的特征,产生白色沉淀质量最大为15.6g,为氢氧化铝,n[Al(OH)3]= ![]() =0.2mol,则m(N)+m(Al)=0.2mol×14g/mol+0.2mol×27g/mol=8.2g,则8.2g甲为AlN,甲溶于氢氧化钠的化学方程式为AlN+NaOH+H2O=NaAlO2+NH3↑, 所以答案是:AlN+NaOH+H2O=NaAlO2+NH3↑.
=0.2mol,则m(N)+m(Al)=0.2mol×14g/mol+0.2mol×27g/mol=8.2g,则8.2g甲为AlN,甲溶于氢氧化钠的化学方程式为AlN+NaOH+H2O=NaAlO2+NH3↑, 所以答案是:AlN+NaOH+H2O=NaAlO2+NH3↑.


科目:高中化学 来源: 题型:
【题目】将可能含有少量碳、硅杂质的a克镁铝合金投入100mL一定物质的量浓度的盐酸中,合金部分溶解,过滤,向所得溶液中滴加5mol/L NaOH溶液至过量,生成沉淀的质量与加入氢氧化钠溶液的体积的关系如图所示. 
(1)原合金中Mg、Al的质量各是多少?
(2)盐酸的物质的量浓度是多少?
(3)取过滤后所得滤渣,向其中加入足量1mol/L NaOH溶液,可生成标准状况下0.112LH2 , 则a的最小值是多少?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于仪器使用的说法正确的是( )
A.滴定管装滴定液时应先用蒸馏水洗净
B.锥形瓶用作反应容器时一定不能加热
C.蒸馏时温度计水银球可以高于蒸馏烧瓶支管口
D.振荡分液漏斗时应关闭玻璃塞和活塞
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室有三瓶失去标签的无色溶液:氯化钾、氢氧化钙和稀硫酸,可用一种常见酸碱指示剂X 或Na2CO3一次鉴别它们.根据有关操作及所加试剂填空. 
(1)现象:溶液显紫色;另取该溶液滴入Na2CO3溶液中,无明显现象.试推断试剂X为 .
(2)现象:溶液显蓝色;另取该溶液滴入Na2CO3溶液中的现象为 , 有关反应的离子方程式为 .
(3)现象:有气泡产生,有关反应的离子方程式为;另取该溶液滴入试剂X,则溶液显 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将适量铁粉放入三氯化铁溶液中,完全反应后,溶液中的Fe2+和Fe3+的物质的量浓度相等,则已反应的Fe3+和未反应的Fe3+的物质的量之比是
A. 2︰3 B. 3︰2 C. 1︰2 D. 1︰1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.Mg2+的半径小于N3-的半径
B.H2O比H2S稳定是因为H2O中存在分子间氢键
C.SiO2的相对分子质量大于CO2,所以SiO2的熔点高于CO2
D.由原子构成的晶体一定是原子晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2016年8月,联合国开发计划署在中国的首个“氢经济示范城市”在江苏如皋落户.用吸附了H2的碳纳米管等材料制作的二次电池的原理如图所示.下列说法正确的是( ) 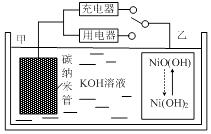
A.放电时,甲电极为正极,OH﹣移向乙电极
B.放电时,乙电极反应为:NiO(OH)+H2O+e﹣=Ni(OH)2+OH﹣
C.充电时,电池的碳电极与直流电源的正极相连
D.电池总反应为H2+2NiOOH ![]() 2Ni(OH)2
2Ni(OH)2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com