
 2C(g)����2 s(��)����C��Ũ��Ϊ0.6 mol/L���������м���˵����
2C(g)����2 s(��)����C��Ũ��Ϊ0.6 mol/L���������м���˵����| A���٢� | B���٢� | C���ڢ� | D���ۢ� |
 ����ʦ���һ��һ��ϵ�д�
����ʦ���һ��һ��ϵ�д� �Ͻ�ƽ��У����ϵ�д�
�Ͻ�ƽ��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2SO3(g) �������й�˵����ȷ���� �� ��
2SO3(g) �������й�˵����ȷ���� �� ��| A��������ʹ�ÿ�ʵ��SO2��ת����Ϊ100% |
| B���ﵽ��ѧƽ��ʱ�������ʵ�Ũ�Ȳ��ٸı� |
| C�������������䣬�����¶ȣ���������Ӧ������ |
| D�������������䣬����SO3��Ũ�ȣ���������Ӧ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������

 CO2+NO��2 minʱ�����������NO�����ʵ���Ϊ0.5 mol ����
CO2+NO��2 minʱ�����������NO�����ʵ���Ϊ0.5 mol �����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 B(g)+D(s)�����ֲ�ͬ�����½��У���Ӧ����Ϊ��ͬ�����ܱ�������B��D��ʼΪ0����Ӧ��A��Ũ�ȣ�mol��L?1���淴Ӧʱ�䣨min���ı仯������±���
B(g)+D(s)�����ֲ�ͬ�����½��У���Ӧ����Ϊ��ͬ�����ܱ�������B��D��ʼΪ0����Ӧ��A��Ũ�ȣ�mol��L?1���淴Ӧʱ�䣨min���ı仯������±���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
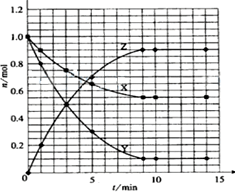
A����Ӧ�Ļ�ѧ����ʽ��X+2Y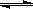 2Z 2Z |
| B���÷�Ӧ��0-3minʱ���ڲ���Z��ƽ����Ӧ����0.083mol��L��1��min��1 |
| C����3����ʱY��Z��Ũ����� |
| D�������������䣬�����¶ȣ�������Ӧ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��150mL 2mol��L-1������ | B��500mL 2mol��L-1������ |
| C��50mL 6mol��L-1��ϡ���� | D��50mL 18.4mol��L-1������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A�����ӷ�Ӧ�����������ѧ��Ӧ����һ���ӿ� |
| B��AgCl��ͬŨ�ȵ�CaCl2��NaCl��Һ�е��ܽ����ͬ |
| C��pH��ͬ������һԪ��HA��Һ��HB��Һ������Zn��Ӧ��HA��HB��Ӧ���ʿ�,˵��HA���Ը�ǿ |
| D����̼������Һ��̼��������Һ�ֱ����ɲ����գ����ù���ijɷ־�Ϊ̼���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 4C2(g) + 2D2 (g) ��5L�ܱ������н��У�����Ӻ�C2�����ʵ���������0.3mol����˷�Ӧ��ƽ������
4C2(g) + 2D2 (g) ��5L�ܱ������н��У�����Ӻ�C2�����ʵ���������0.3mol����˷�Ӧ��ƽ������ x
xA�� (B2) =" 0.01mol��(L��s)" �C1 (B2) =" 0.01mol��(L��s)" �C1 | B�� (C2) =" 0.002mol��(L��s)" �C1 (C2) =" 0.002mol��(L��s)" �C1 |
C�� (D2) =" 0.006mol��(L��s)" �C1 (D2) =" 0.006mol��(L��s)" �C1 | D�� (A2) =" 0.008mol��(L��s)" �C1 (A2) =" 0.008mol��(L��s)" �C1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 A���� B���٢� C���ڢ� D����
A���� B���٢� C���ڢ� D�����鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com