
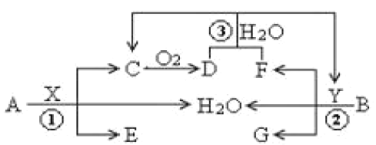
ЁОЬтФПЁПвбжЊСНжжГЃМћН№ЪєA(ЕиПЧжаКЌСПЕкЖўЕФН№Ъє)ЁЂB(КьЩЋН№Ъє)ЗжБ№гыСНжжЫсXЁЂYЗЂЩњЗДгІЃЌЦфзЊЛЏЙиЯЕШчЭМЫљЪОЃЌЦфжаDЮЊКьзиЩЋЦјЬхЁЃ
ЛиД№вдЯТЮЪЬтЃК
ЃЈ1ЃЉЗДгІЂлЕФРызгЗДгІЗНГЬЪНЮЊ___ЃЛ
ЃЈ2ЃЉ6.4gBгыЙ§СПXШмвК(8mol /LЁЂ60mL)ГфЗжЗДгІКѓЃЌЩњГЩЕФЛЙдВњЮягаCЁЂDЃЌЗДгІКѓШмвКжаЫљКЌXЮЊn mol ЃЌДЫЪБШмвКжаЫљКЌXЕФвѕРызгЕФЮяжЪЕФСПЮЊ___molЁЃ
ЃЈ3ЃЉГЃЮТЯТAгыYЕФЯЁШмвКФмЗЂЩњЗДгІЩњГЩбЮWЃЌЙигкЙЬЬхWЕФзЊЛЏЙиЯЕШчЭМЫљЪО(ЮоЙиЮяжЪвбТдШЅ)ЁЃЦфжаNЪЧКьзиЩЋЕФЛЏКЯЮяЁЃ
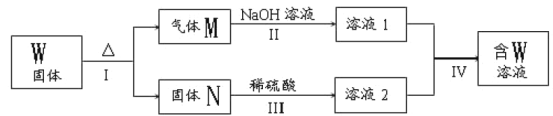
ЂйMгЩСНжжЛЏКЯЮязщГЩЃЌЦфжаКЌгаЃЦЃЛНЋЃЭЭЈШыBaCl2ШмвКЃЌЪЕбщЯжЯѓЪЧ___ЁЃ
ЂкШєОЗДгІIЕУЕН16 gЙЬЬхЃЮЃЌВњЩњЕФЦјЬхMЧЁКУБЛ0.3L1molЁЄLЃ1 NaOHШмвКЭъШЋЮќЪеЕУШмвК1ЃЌдђЗДгІЂєжаЗЂЩњЗДгІЕФРызгЗНГЬЪНЪЧ____ЁЃ
ЁОД№АИЁПSO2+NO2 +H2O=2H++SO42-+NO n+0.2 ВњЩњАзЩЋГСЕэ 2Fe3++HSO3-+H2O=2Fe2++SO42-+3H+
ЁОНтЮіЁП
ГЃМћН№ЪєAЮЊЕиПЧжаКЌСПЕкЖўЕФН№ЪєЃЌШЗЖЈЮЊFeЁЂBЮЊКьЩЋН№ЪєШЗЖЈЮЊCuЃЌИљОн DЮЊКьзиЩЋЦјЬхЃЌШЗЖЈDЮЊNO2ЃЌCЮЊNOЃЌXЮЊHNO3ЃЛBЮЊCuЃЌЭПЩвдгыХЈСђЫсЗДгІЩњГЩСђЫсЭЃЌЖўбѕЛЏСђКЭЫЎЃЛЩњГЩЕФЖўбѕЛЏСђгаЛЙдадЃЌПЩвдгыNO2ЗДгІЩњГЩСђЫсКЭЯѕЫсЃЌШЗЖЈBЮЊCuЃЌYЮЊСђЫсЃЌFЮЊSO2ЃЌGЮЊCuSO4ЃЛЃЈ3ЃЉAЃЈFeЃЉгыYЃЈСђЫсЃЉЕФЯЁШмвКЗДгІЩњГЩСђЫсбЧЬњКЭЧтЦјЃЌШЗЖЈWЮЊFeSO4ЃЌ2FeSO4![]() Fe2O3+SO2Ёќ+SO3ЁќЃЌЦјЬхMЮЊSO2КЭSO3ЕФЛьКЯЮяЃЌMгыNaOHЗДгІЩњГЩбЮКЭЫЎЃЌNЮЊFe2O3ЃЌгыЯЁСђЫсЗДгІЩњГЩСђЫсЬњКЭЫЎЁЃFe3+ОпгабѕЛЏадКЭ+4МлСђдЊЫиОпгаЛЙдадЃЌПЩвдЗЂЩњбѕЛЏЛЙдЗДгІЩњГЩСђЫсбЧЬњЃЌОнДЫЗжЮіЁЃ
Fe2O3+SO2Ёќ+SO3ЁќЃЌЦјЬхMЮЊSO2КЭSO3ЕФЛьКЯЮяЃЌMгыNaOHЗДгІЩњГЩбЮКЭЫЎЃЌNЮЊFe2O3ЃЌгыЯЁСђЫсЗДгІЩњГЩСђЫсЬњКЭЫЎЁЃFe3+ОпгабѕЛЏадКЭ+4МлСђдЊЫиОпгаЛЙдадЃЌПЩвдЗЂЩњбѕЛЏЛЙдЗДгІЩњГЩСђЫсбЧЬњЃЌОнДЫЗжЮіЁЃ
ЃЈ1ЃЉИљОнвдЩЯЗжЮіПЩжЊЃЌЗДгІЂлЮЊSO2ЁЂNO2КЭЫЎЕФЗДгІЃЌИљОнЕУЪЇЕчзгЪ§ЯрЕШКЭдзгЪиКуХфЦНЃЌЕУРызгЗДгІЗНГЬЪНЮЊSO2+NO2 +H2O=2H++SO42-+NOЃЛ
Д№АИЃКSO2+NO2 +H2O=2H++SO42-+NO
ЃЈ2ЃЉ6.4gBгыЙ§СПXШмвК(HNO3)ГфЗжЗДгІКѓЃЌЩњГЩЕФЛЙдВњЮягаNO2ЁЂNOЃЌЗДгІКѓШмвКжаЫљКЌHNO3ЮЊn mol ЃЌШмвКжаЫљКЌN![]() ЕФЮяжЪЕФСПЮЊЃКnЃЈN
ЕФЮяжЪЕФСПЮЊЃКnЃЈN![]() ЃЉ=nЃЈCu2+ЃЉЁС2+n=
ЃЉ=nЃЈCu2+ЃЉЁС2+n=![]() +n= n+0.2molЃЛ
+n= n+0.2molЃЛ
Д№АИЃКn+0.2
ЃЈ3ЃЉЂйНЋЃЭЃЈSO2ЁЂSO3ЃЉЭЈШыBaCl2ШмвКЃЌЗЂЩњЗДгІSO3+H2O+BaCl2=BaSO4Ё§+2HClЃЌгаАзЩЋГСЕэЩњГЩЃЛ
Д№АИЃКВњЩњАзЩЋГСЕэ
ЂкЗДгІЂёЃК2FeSO4![]() Fe2O3+ SO2Ёќ+ SO3ЁќЃЛЗДгІЂѓFe2O3+3H2SO4=Fe2(SO4)3+3H2OЃЛ
Fe2O3+ SO2Ёќ+ SO3ЁќЃЛЗДгІЂѓFe2O3+3H2SO4=Fe2(SO4)3+3H2OЃЛ
ИљОнЙЬЬхMЃЈFe2O3ЃЉЕФСПМЦЫуГіSO2КЭSO3ЕФЮяжЪЕФСПЁЃ
2FeSO4![]() Fe2O3+ SO2Ёќ+ SO3Ёќ
Fe2O3+ SO2Ёќ+ SO3Ёќ
160g 1mol 1mol
1.6g 0.01mol 0.01mol
ЗДгІЂђ SO3 + 2NaOH=Na2SO4+H2O
1mol 2mol 1mol
0.01mol 0.02mol 0.01mol
SO2+ NaOH = NaHSO3
1mol 1mol 1mol
0.01mol 0.01mol 0.01mol
ШмвК1ЮЊNa2SO4КЭNaHSO3ЕФЛьКЯЮяЃЛ
ЗДгІЂєЃКСђЫсЬњОпгабѕЛЏадЃЌбЧСђЫсЧтФЦОпгаЛЙдадЃЌИљОнЕУЪЇЕчзгЪ§ЯрЕШКЭдзгЪиКуЕУГіРызгЗНГЬЪН2Fe3++HSO3-+H2O=2Fe2++SO42-+3H+ЃЛ
Д№АИЃК2Fe3++HSO3-+H2O=2Fe2++SO42-+3H+



| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЙЄвЕЩЯЃЌПЩВЩгУЛЙдЗЈДІРэЮВЦјжаNOЃЌЦфдРэ:2NO(g)+2H2(g)![]() N2(g)+2H2O(g) ЁїH<0ЁЃдкЛЏбЇЩЯЃЌе§ЗДгІЫйТЪЗНГЬЪНБэЪОЮЊvЃЈе§ЃЉ=kЃЈе§ЃЉЁЄcm(NOЃЉЁЄcnЃЈH2ЃЉЃЌФцЗДгІЫйТЪЗНГЬЪНБэЪОЮЊvЃЈФцЃЉ=kЃЈФцЃЉЁЄcxЃЈN2ЃЉЁЄcyЃЈH2OЃЉЃЌЦфжаЃЌkБэЪОЗДгІЫйТЪГЃЪ§ЃЌжЛгыЮТЖШгаЙиЃЌmЃЌnЃЌxЃЌyНаЗДгІМЖЪ§ЃЌгЩЪЕбщВтЖЈЁЃдкКуШнУмБеШнЦїжаГфШыNOЁЂH2ЃЌдкTЁцЯТНјааЪЕбщЃЌВтЕУгаЙиЪ§ОнШчЯТЃК
N2(g)+2H2O(g) ЁїH<0ЁЃдкЛЏбЇЩЯЃЌе§ЗДгІЫйТЪЗНГЬЪНБэЪОЮЊvЃЈе§ЃЉ=kЃЈе§ЃЉЁЄcm(NOЃЉЁЄcnЃЈH2ЃЉЃЌФцЗДгІЫйТЪЗНГЬЪНБэЪОЮЊvЃЈФцЃЉ=kЃЈФцЃЉЁЄcxЃЈN2ЃЉЁЄcyЃЈH2OЃЉЃЌЦфжаЃЌkБэЪОЗДгІЫйТЪГЃЪ§ЃЌжЛгыЮТЖШгаЙиЃЌmЃЌnЃЌxЃЌyНаЗДгІМЖЪ§ЃЌгЩЪЕбщВтЖЈЁЃдкКуШнУмБеШнЦїжаГфШыNOЁЂH2ЃЌдкTЁцЯТНјааЪЕбщЃЌВтЕУгаЙиЪ§ОнШчЯТЃК
ЪЕбщ | c(NO)/molЁЄL-1 | c(H2)/molЁЄL-1 | v(е§)/molЁЄL-1ЁЄmin-1 |
Ђй | 0.10 | 0.10 | 0.414k |
Ђк | 0.10 | 0.40 | 1.656k |
Ђл | 0.20 | 0.10 | 1.656k |
ЯТСагаЙиЭЦЖЯе§ШЗЕФЪЧ
A. ЩЯЪіЗДгІжаЃЌЗДгІЮяЕФзмФмСПЕЭгкЩњГЩЮяЕФзмФмСП
B. ШєЩ§ИпЮТЖШЃЌдђkЃЈе§ЃЉдіДѓЃЌkЃЈФцЃЉМѕаЁ
C. дкЩЯЪіЗДгІжаЃЌЗДгІМЖЪ§ЃКm=2ЃЌn=1
D. дквЛЖЈЮТЖШЯТЃЌNOЁЂH2ЕФХЈЖШЖде§ЗДгІЫйТЪгАЯьГЬЖШЯрЭЌ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПдкЗДгІ 3Cl2ЃЋ6KOH![]() KClO3ЃЋ5KClЃЋ3H2O жаЃЌЯТСаЫЕЗЈе§ШЗЕФЪЧЃК( )
KClO3ЃЋ5KClЃЋ3H2O жаЃЌЯТСаЫЕЗЈе§ШЗЕФЪЧЃК( )
ЂйCl2ЪЧбѕЛЏМСЃЌKOHЪЧЛЙдМС ЂкKClЪЧЛЙдВњЮяЃЌKClO3ЪЧбѕЛЏВњЮя ЂлЗДгІжаУПЯћКФ3 mol Cl2Зжзгжага5mol ЕчзгЗЂЩњзЊвЦ ЂмБЛбѕЛЏгыБЛЛЙдЕФТШдзгЮяжЪЕФСПжЎБШЮЊ5ЁУ1
A.ЂйЂмB.ЂкЂлC.ЂкЂлЂмD.ЂкЂм
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПCЁЂNЁЂSЕФбѕЛЏЮяГЃЛсдьГЩвЛаЉЛЗОГЮЪЬтЃЌПЦбаЙЄзїепе§дкбаОПгУИїжжЛЏбЇЗНЗЈРДЯћГ§етаЉЮяжЪЖдЛЗОГЕФВЛРћгАЯьЁЃ
ЃЈ1ЃЉдкДпЛЏМСДцдкЕФЬѕМўЯТЃЌгУH2НЋNOЛЙдЮЊN2ЁЃвбжЊЃК

дђЧтЦјКЭвЛбѕЛЏЕЊЗДгІЩњГЩЕЊЦјКЭЫЎеєЦјЕФШШЛЏбЇЗНГЬЪНЪЧ_____ЁЃ
ЃЈ2ЃЉдк500ЁцЯТКЯГЩМзДМЕФЗДгІдРэЮЊЃК
CO2(g)ЃЋ3H2(g)![]() CH3OH(g)ЃЋH2O(g)дк1LЕФУмБеШнЦїжаЃЌГфШы1mol CO2КЭ3mol H2ЃЌбЙЧПЮЊp0ЃЌВтЕУCO2(g)КЭCH3OH(g)ЕФХЈЖШЫцЪБМфБфЛЏШчЭМЫљЪОЁЃ(ПЩФцЗДгІЕФЦНКтГЃЪ§ПЩвдгУЦНКтХЈЖШМЦЫуЃЌвВПЩвдгУЦНКтЗжбЙKpДњЬцЦНКтХЈЖШЃЌМЦЫуЗжбЙЃНзмбЙЁСЮяжЪЕФСПЗжЪ§)
CH3OH(g)ЃЋH2O(g)дк1LЕФУмБеШнЦїжаЃЌГфШы1mol CO2КЭ3mol H2ЃЌбЙЧПЮЊp0ЃЌВтЕУCO2(g)КЭCH3OH(g)ЕФХЈЖШЫцЪБМфБфЛЏШчЭМЫљЪОЁЃ(ПЩФцЗДгІЕФЦНКтГЃЪ§ПЩвдгУЦНКтХЈЖШМЦЫуЃЌвВПЩвдгУЦНКтЗжбЙKpДњЬцЦНКтХЈЖШЃЌМЦЫуЗжбЙЃНзмбЙЁСЮяжЪЕФСПЗжЪ§)
ЂйЗДгІНјааЕН4minЪБЃЌv(е§)__v(Фц) (ЬюЁА>ЁБЁА<ЁБЛђЁАЃНЁБ)ЁЃ0ЁЋ4minЃЌH2ЕФЦНОљЗДгІЫйТЪv(H2)ЃН_molЁЄLЃ1ЁЄminЃ1ЁЃ

ЂкCO2ЦНКтЪБЕФЬхЛ§ЗжЪ§ЮЊ___ЃЌИУЮТЖШЯТKpЮЊ__(гУКЌгаp0ЕФЪНзгБэЪО)ЁЃ
ЂлЯТСаФмЫЕУїИУЗДгІвбДяЕНЦНКтзДЬЌЕФЪЧ___ЁЃ
A.vе§(CH3OH)ЃН3vФц(H2)
B.CO2ЁЂH2ЁЂCH3OHКЭH2OХЈЖШжЎБШЮЊ1ЃК3ЃК1ЃК1
C.КуЮТКубЙЯТЃЌЦјЬхЕФЬхЛ§ВЛдйБфЛЏ
D.КуЮТКуШнЯТЃЌЦјЬхЕФУмЖШВЛдйБфЛЏ
Ђм500ЁцЁЂдк2ИіШнЛ§ЖМЪЧ2LЕФУмБеШнЦїжаЃЌАДВЛЭЌЗНЪНЭЖШыЗДгІЮяЃЌБЃГжКуЮТЁЂКуШнЃЌВтЕУЗДгІДяЕНЦНКтЪБЕФгаЙиЪ§ОнШчЯТЃК
ШнЦї | ШнЦїМз | ШнЦївв |
ЗДгІЮяЦ№ЪМЭЖШыСП | 1mol CO2ЃЌ3mol H2 | 0.5mol CO2ЃЌ1mol H2 1mol CH3OHЃЌ1mol H2O |
CH3OHЕФЦНКтХЈЖШ/mol ЁЄLЃ1 | C1 | C2 |
дђввШнЦїжаЗДгІЦ№ЪМЯђ___ЗНЯђНјааЃЛc1___c2ЁЃ(ЬюЁА>ЁБЁА<ЁБЛђЁАЃНЁБ)
ЃЈ3ЃЉМзДМзїЮЊвЛжжШМСЯЛЙПЩгУгкШМСЯЕчГиЁЃдкЮТЖШЮЊ650ЁцЕФШлШкбЮШМСЯЕчГижагУМзДМЁЂПеЦјгыCO2ЕФЛьКЯЦјЬхзїЗДгІЮяЃЌФјзїЕчМЋЃЌгУLi2CO3КЭNa2CO3ЛьКЯЮязїЕчНтжЪЁЃИУЕчГиЕФИКМЋЗДгІЪНЮЊ___ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПВнЫсЪЧвЛжжЖўдЊШѕЫсЃЌПЩгУзїЛЙдМСЁЂГСЕэМСЕШЁЃФГаЃПЮЭтаЁзщЕФЭЌбЇЩшМЦРћгУC2H2ЦјЬхжЦШЁH2C2O4ЁЄ2H2OЁЃЛиД№ЯТСаЮЪЬтЃК
(1)МззщЕФЭЌбЇвдЕчЪЏ(жївЊГЩЗжCaC2ЃЌЩйСПCaSМАCa3P2дгжЪЕШ)ЮЊдСЯЃЌВЂгУЯТЭМ1зАжУжЦШЁC2H2ЁЃ
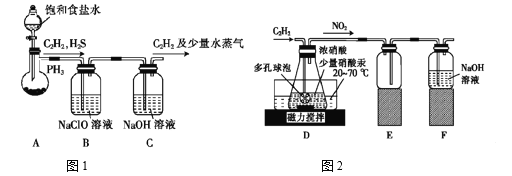
ЂйЕчЪЏгыЫЎЗДгІКмПьЃЌЮЊСЫМѕЛКЗДгІЫйТЪЃЌзАжУAжаГ§гУБЅКЭЪГбЮЫЎДњЬцЫЎжЎЭтЃЌЛЙПЩвдВЩШЁЕФДыЪЉЪЧ__________ЃЈаДвЛжжМДПЩЃЉЁЃ
ЂкзАжУBжаЃЌNaClOНЋH2SЁЂPH3 бѕЛЏЮЊСђЫсМАСзЫсЃЌБОЩэБЛЛЙдЮЊNaClЃЌЦфжаPH3БЛбѕЛЏЕФРызгЗНГЬЪНЮЊ______ЁЃИУЙ§ГЬжаЃЌПЩФмВњЩњаТЕФдгжЪЦјЬхCl2ЃЌЦфдвђЪЧЃК _____________ЃЈгУРызгЗНГЬЪНЛиД№ЃЉЁЃ
(2)ввзщЕФЭЌбЇИљОнЮФЯззЪСЯЃЌгУHg(NO3)2зїДпЛЏМСЃЌХЈЯѕЫсбѕЛЏC2H2жЦШЁH2C2O4ЁЄ2H2OЁЃжЦБИзАжУШчЩЯЭМ2ЫљЪОЃК
ЂйзАжУDжаЖрПзЧђХнЕФзїгУЪЧ______________________ЁЃ
ЂкзАжУDжаЩњГЩH2C2O4ЕФЛЏбЇЗНГЬЪНЮЊ____________________________ЁЃ
ЂлДгзАжУDжаЕУЕНВњЦЗЃЌЛЙашОЙ§_____________ЃЈЬюВйзїУћГЦЃЉЁЂЙ§ТЫЁЂЯДЕгМАИЩдяЁЃ
(3)БћзщЩшМЦСЫВтЖЈввзщВњЦЗжаH2C2O4ЁЄ2H2OЕФжЪСПЗжЪ§ЪЕбщЁЃЫћУЧЕФЪЕбщВНжшШчЯТЃКзМШЗГЦШЁm gВњЦЗгкзЖаЮЦПжаЃЌМгШыЪЪСПЕФеєСѓЫЎШмНтЃЌдйМгШыЩйСПЯЁСђЫсЃЌШЛКѓгУc molЁЄLЃ1ЫсадKMnO4БъзМШмвКНјааЕЮЖЈжСжеЕуЃЌЙВЯћКФБъзМШмвКV mLЁЃ
ЂйЕЮЖЈжеЕуЕФЯжЯѓЪЧ______________________ЁЃ
ЂкЕЮЖЈЙ§ГЬжаЗЂЯжЭЪЩЋЫйТЪПЊЪМКмТ§Кѓж№НЅМгПьЃЌЗжЮіПЩФмЕФдвђЪЧ_______________ЁЃ
ЂлВњЦЗжаH2C2O4ЁЄ2H2OЕФжЪСПЗжЪ§ЮЊ_______________ЃЈСаГіКЌ mЁЂcЁЂV ЕФБэДяЪНЃЉЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЙЄвЕДПМюжаГЃКЌгаЩйСПЕФNaClдгжЪЃЌФГЛЏбЇаЫШЄаЁзщШЁagЙЄвЕДПМюбљЦЗгызуСПЯЁбЮЫсГфЗжЗДгІЃЌМгШШЁЂеєИЩЁЂзЦЩеЃЌЕУbgЙЬЬхЁЃдђИУбљЦЗжаДПМюЕФжЪСПЗжЪ§ЪЧЃЈ ЃЉ
A. ![]() ЁС100%B.
ЁС100%B. ![]() ЁС100%C.
ЁС100%C. ![]() ЁС100%D.
ЁС100%D. ![]() ЁС100%
ЁС100%
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯжгаAЁЂBЁЂCШ§жжЬўЃЌЦфЧђЙїФЃаЭШчЯТЭМЃК
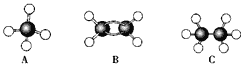
ЃЈ1ЃЉЕШжЪСПЕФвдЩЯЮяжЪЭъШЋШМЩеЪБКФШЅO2ЕФСПзюЖрЕФЪЧ________(ЬюЖдгІзжФИЃЌЯТЭЌ)ЃЛ
ЃЈ2ЃЉЭЌзДПіЁЂЭЌЬхЛ§ЕФвдЩЯШ§жжЮяжЪЭъШЋШМЩеЪБКФШЅO2ЕФСПзюЖрЕФЪЧ____________ЃЛ
ЃЈ3ЃЉЕШжЪСПЕФвдЩЯШ§жжЮяжЪШМЩеЪБЃЌЩњГЩЖўбѕЛЏЬМзюЖрЕФЪЧ________ЃЌЩњГЩЫЎзюЖрЕФЪЧ________ЁЃ
ЃЈ4ЃЉдк120ЁцЁЂ1.01ЁС105 PaЯТЪБЃЌгаСНжжЦјЬЌЬўКЭзуСПЕФбѕЦјЛьКЯЕуШМЃЌЯрЭЌЬѕМўЯТВтЕУЗДгІЧАКѓЦјЬхЬхЛ§УЛгаЗЂЩњБфЛЏЃЌетСНжжЦјЬхЪЧ__________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПНЋЩйСПБЅКЭFeCl3ШмвКЗжБ№ЕЮМгЕНЯТСаЮяжЪжаЃЌЕУЕНШ§жжЗжЩЂЯЕЃЌЭъГЩЯрЙиЮЪЬтЃК
МзЃКБЅКЭFeCl3ШмвКЕЮМгЕНРфЫЎжаЃЛ
ввЃКБЅКЭFeCl3ШмвКЕЮМгЕНNaOHШмвКжаЃЛ
БћЃКБЅКЭFeCl3ШмвКЕЮМгЕНЗаЫЎжаЁЃ
ЃЈ1ЃЉНЋБћМЬајМгШШжѓЗаЕУЕНКьКжЩЋЭИУївКЬхЃЌЗДгІЕФЛЏбЇЗНГЬЪНЮЊ___________
ЃЈ2ЃЉгУзюМђЕЅЕФЗНЗЈХаЖЯБћжаЪЧЗёГЩЙІжЦБИНКЬхЃЌЧыаДГіЯрЙиЕФВйзїЁЂЯжЯѓКЭНсТл__________
ЃЈ3ЃЉЯђОЙ§МьбщКѓЕФБћжаж№ЕЮМгШыЯЁбЮЫсЃЌЛсГіЯжвЛЯЕСаБфЛЏЃК
ЂйЯШГіЯжКЭввжаЯрЭЌЕФЯжЯѓЃЌдвђЮЊ_______________
ЂкЫцКѓЗЂЩњБфЛЏЕУЕНКЭМзЯрЭЌЕФШмвКЃЌДЫЗДгІЕФРызгЗДгІЗНГЬЪНЮЊ_______
ЃЈ4ЃЉЯђБћжаМгШыЕчМЋЭЈЕчКѓЃЌ_______МЋбеЩЋБфЩюЃЈЬюЁАвѕМЋЁБЛђЁАбєМЋЁБЃЉ
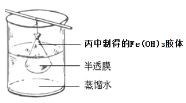
ЃЈ5ЃЉПЩгУШчЭМЫљЪОЕФзАжУГ§ШЅFeЃЈOHЃЉ3НКЬхжаЕФдгжЪРызгРДЬсДПFeЃЈOHЃЉ3НКЬхЃЌЪЕбщЙ§ГЬжаашВЛЖЯИќЛЛЩеБжаЕФеєСѓЫЎЁЃИќЛЛеєСѓЫЎШєИЩДЮКѓЃЌШЁЩйСПЩеБжаЕФвКЬхЃЌЯђЦфжаМгШыAgNO3ШмвКЃЌШє_______ЃЈЬюЪЕбщЯжЯѓЃЉЃЌдђЫЕУїИУFeЃЈOHЃЉ3НКЬхжаЕФдгжЪРызгвбОЭъШЋГ§ШЅЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЩш NA БэЪОАЂЗќМгЕТТоГЃЪ§ЕФжЕЃЌЯТСаЫЕЗЈе§ШЗЕФЪЧ
A.БъзМзДПіЯТЃЌ22.4L CCl4жаКЌгаЕФЗжзгЪ§ЮЊNA
B.1L 0.5 mol/LNa2SO4ШмвКжаЃЌКЌгаЕФбѕдзгзмЪ§ЮЊ2NA
C.0.5 mol/LFe2(SO4)3 ШмвКжаЃЌSO42ЃЕФЪ§ФПЮЊ 1.5 NA
D.C2H4 КЭ C3H6 ЕФЛьКЯЮя agЃЌЫљКЌдзгзмЪ§ЮЊ![]()
ВщПДД№АИКЭНтЮі>>
АйЖШжТаХ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com