
【题目】下列表述合理的是
A. 苯与乙炔的实验式均是C2H2
B. 溴乙烷的比例模型是
C. 羟基的电子式:![]()
D. CH3COOH的电离方程式是CH3COOH=CH3COO-+H+
科目:高中化学 来源: 题型:
【题目】某烃类化合物A,其蒸汽对氢气的相对密度是42,红外光谱表明分子中含有碳碳双键,核磁共振氢谱表明分子中只有一种类型的氢。
(1)A的结构简式为 ,名称为____________________。
(2)A中的碳原子是否都处于同一平面?___________(填“是”或“不是”);
(3)已知A、B、C有如下转化关系:

则反应②的化学方程式为 ;反应的类型是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是部分短周期元素化合价与原子序数的关系图,下列说法不正确的是
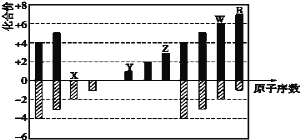
A.氢化物的沸点:H2W<H2X
B.WX3和水反应形成的化合物是离子化合物
C.X,Y,R形成的某种化合物可以用于漂白、消毒
D.Y,Z和W三者最高价氧化物对应的水化物能两两相互反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物E是重要的医药中间体,B中碳原子数目是A中的3倍。以A和B为原料合成该有机物的路线如下:
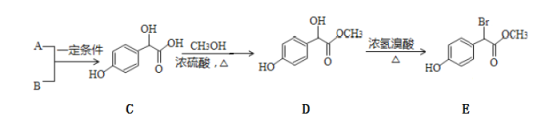
(1)已知A+B→C为加成反应,则A的结构简式为___________,B的化学名称为 _______,E中含有的官能团有_______________________(填名称)。
(2)1mol C在一定条件下与浓溴水反应,最多消耗溴的物质的量为______mol。C生成D的反应类型为______________。
(3)2分子C脱水可以生成F,核磁共振氢谱显示F分子中含有4种氢原子,其结构中有3个六元环,则F分子的结构简式为________________。
(4)E有多种同分异构体,其中苯环上只有2个对位取代基,含有-COOH且能使FeCl3溶液显紫色的结构有_______________(不考虑立体异构)种。
(5)根据已有知识并结合信息 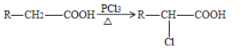 ,写出以CH3COOH为原料制备A的合成路线图:___________________________________。(无机试剂任选,注明反应条件)。
,写出以CH3COOH为原料制备A的合成路线图:___________________________________。(无机试剂任选,注明反应条件)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】指出下列原子的杂化轨道类型及分子的结构式、空间构型。
(1)CO2分子中的C采取______杂化,分子的结构式为______,空间构型呈______;
(2)CH2O中的C采取______杂化,分子的结构式为______,空间构型呈______;
(3)H2S分子中的S采取______杂化,分子的结构式为______,空间构型呈______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究表明,氮氧化物和二氧化硫在形成雾霾时与大气中的氨有关(如下图所示)。下列叙述错误的是

A. 雾和霾的分散剂相同
B. 雾霾中含有硝酸铵和硫酸铵
C. NH3是形成无机颗粒物的催化剂
D. 雾霾的形成与过度施用氮肥有关
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】青蒿酸是合成青蒿素的原料,可以由香草醛合成:

下列有关叙述正确的是
A. 香草醛的分子式是C8H10O3
B. 香草醛能与NaHCO3溶液反应
C. 两种物质均可与溴的四氯化碳溶液发生加成反应
D. 可用FeCl3溶液检验青蒿酸中是否含香草醛
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组欲利用 CuO 与 NH3 反应,研究 NH3 的某种性质并测定其组成,设计了如下实验装置(夹持装置未画出)进行实验。请回答下列问题:
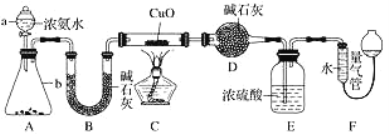
(1)仪器a的名称为_____;仪器b中可选择的试剂为________(填名称)。
(2)实验室中,利用装置A,还可制取的无色气体是______ (填字母)。
A.Cl2 B.O2 C.CO2 D.NO2
(3)实验中观察到装置C中黑色CuO粉末变为红色固体,量气管有无色无味的气体,上述现象证明NH3具有______性,写出相应的化学方程式____________。
(4)E装置中浓硫酸的作用________。
(5)读取气体体积前,应对装置F进行的操作:__________。
(6)实验完毕,若测得干燥管D增重mg,装置F测得气体的体积为nL(已折算成标准状况),则氨分子中氮、氢的原子个数比为___________(用含m、n字母的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业合成氨的反应是在高温、高压和有催化剂存在的条件下,用氢气和氮气直接化合制取:3H2+N2![]() 2NH3,这是一个正反应放热的可逆反应。如果反应在密闭容器中进行,下述有关说法中错误的是
2NH3,这是一个正反应放热的可逆反应。如果反应在密闭容器中进行,下述有关说法中错误的是
A.为了提高H2的转化率。应适当提高N2的浓度
B.达到平衡时,c(NH3)一定是c(H2)的三分之二
C.使用催化剂是为了加快反应速率,提高生产效率
D.达到平衡时,氨气分解速率是氮气消耗速率的两倍
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com