
【题目】苯甲酸广泛应用于制药和化工行业。某同学尝试用甲苯的氧化反应制备苯甲酸。
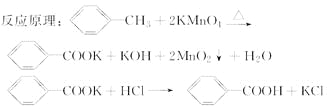
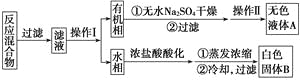
实验方法:一定量的甲苯和KMnO4溶液在100 ℃反应一段时间后停止反应,按如下流程分离出苯甲酸和回收未反应的甲苯。
已知:苯甲酸分子量122,熔点122.4 ℃,在25 ℃和95 ℃时溶解度分别为0.3 g和6.9 g;纯净固体有机物一般都有固定熔点。
(1)操作Ⅰ为________,操作Ⅱ为________。
(2)无色液体A是________,定性检验A的试剂是________,现象是________。
(3)测定白色固体B的熔点,发现其在115 ℃开始熔化,达到130 ℃时仍有少量不熔。该同学推测白色固体B是苯甲酸与KCl的混合物,设计了如下方案进行提纯和检验,实验结果表明推测正确。请在完成表中内容。
序号 | 实验方案 | 实验现象 | 结果 |
① | 将白色固体B加入水中,加热溶解,________ | 得到白色晶体和无色滤液 | |
② | 取少量滤液于试管中,________ | 生成白色沉淀 | 滤液含Cl- |
③ | 干燥白色晶体,________ | ________ | 白色晶体是苯甲酸 |
(4)纯度测定:称取1.220 g产品,配成100 mL苯甲酸溶液,移取25.00 mL溶液,滴定,消耗KOH的物质的量为2.40×10-3mol,产品中苯甲酸质量分数的计算结果为________(保留2位有效数字)。
【答案】(1)分液;蒸馏;
(2)甲苯 酸性KMnO4溶液 溶液颜色褪去(其他合理答案也可);
(3)①冷却结晶,过滤 ②滴加稀HNO3和AgNO3溶液 ③取适量加热,测定熔点 白色晶体在122.4 ℃熔化为液体(其他合理答案也可)
(4)
【解析】试题分析:一定量的甲苯和适量的KMnO4溶液在100℃反应一段时间后停止反应,按如图流程分离出苯甲酸和回收未反应的甲苯,苯甲酸能溶于水,甲苯不溶于水,互不相溶的液体采用分液方法分离,根据实验目的知,从而得到有机相和水相,有机相中含有甲苯、水相中含有苯甲酸,有机相中的甲苯采用蒸馏方法得到无色液体A,A是甲苯,将水相盐酸酸化再蒸发浓缩,根据苯甲酸的溶解度知,得到的固体B是苯甲酸。
(1)分离互不相溶的液体采用分液方法,根据流程图中,水相和有机相不互溶,可以采用分液方法分离,即操作I为分液,有机相中物质互溶且沸点不同,所以可以采用蒸馏方法分离,即操作II为蒸馏,故答案为:分液;蒸馏;
(2)通过以上分析知,A是甲苯,甲苯中有甲基,所以能被酸性高锰酸钾氧化为苯甲酸而使酸性高锰酸钾溶液褪色,则可以用酸性高锰酸钾溶液检验甲苯,故答案为:甲苯;酸性KMnO4溶液;溶液褪色;
(3)通过测定白色固体B的熔点,发现其在115℃开始熔化,达到130℃时仍有少量不熔,推测白色固体B是苯甲酸与KCl的混合物,氯化钾可以用硝酸酸化的硝酸银溶液检验氯离子的存在;利用苯甲酸的溶解度特征在25℃和95℃时溶解度分别为0.3g和6.9g;利用不同温度下的溶解度,分离混合物,得到晶体后通过测定熔点判断是否为苯甲酸;故答案为:
序号 | 实验方案 | 实验现象 | 结论 |
① | 将白色固体B加入水中加热,溶解,冷却、过滤 | 得到白色晶体和无色溶液 | -- |
② | 取少量滤液于试管中,滴入2-3滴AgNO3溶液 | 生成白色沉淀 | 滤液含有Cl- |
③ | 干燥白色晶体,加热使其融化,测其熔点; | 熔点为122.4℃ | 白色晶体是苯甲酸 |
(4)称取1.220g产品,配成100ml甲醇溶液,移取25.00ml溶液,滴定,消耗KOH的物质的量为2.40×10-3mol,苯甲酸是一元弱酸和氢氧化钾1:1反应,所以物质的量相同,注意溶液体积变化计算样品中苯甲酸的物质的量,计算质量分数;样品中苯甲酸质量分数= ,故答案为:96%。
,故答案为:96%。


科目:高中化学 来源: 题型:
【题目】在稀硫酸中加入铜粉,铜粉不溶解,再加入下列固体粉末:①FeCl2;②Fe2O3;③Zn;④KNO3,铜粉可溶解的是
A. ①② B. ②④ C. ②③ D. ①④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有a mol/L 的NaX和b mol/L的NaY两种盐溶液。下列说法正确的是
A.若a=b且c(X-)= c(Y-)+ c(HY),则HX为强酸
B.若a=b且pH(NaX)>pH(NaY),则c(X-)+ c(OH-)> c(Y-)+ c(OH-)
C.若a>b且c(X-)= c(Y-),则酸性HX>HY
D.若两溶液等体积混合,则c(Na+)=(a+b) mol/L(忽略混合过程中的体积变化)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产、生活、社会密切相关。下列说法中不正确的是
A.蛋白质、棉花、PVC、淀粉都是混合物
B.废弃的玻璃、金属、纸制品是可回收利用的资源
C.铁在潮湿的空气中放置,易发生化学腐蚀而生锈
D.用CO2合成聚碳酸酯可降解塑料,实现“碳”的循环利用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】目前工业上有一种方法是用CO2生产燃料甲醇。一定条件下发生反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g),图1表示该反应过程中能量(单位为kJ·mol—1)的变化。
CH3OH(g)+H2O(g),图1表示该反应过程中能量(单位为kJ·mol—1)的变化。

(1)该反应为 热反应,原因是 。
(2)下列能说明该反应已经达到平衡状态的是 (填序号)
A.v(H2)=3v(CO2)
B.容器内气体压强保持不变
C.v逆(CO2)=v正(CH3OH)
D.容器内气体密度保持不变
(3)在体积为1 L的密闭容器中,充入1 molCO2和3 molH2,测得CO2和CH3OH(g)的浓度随时间变化如图2所示。从反应开始到平衡,用氢气浓度变化表示的平均反应速率v(H2)= 。 达平衡时容器内平衡时与起始时的压强之比 。
(4)甲醇、氧气在酸性条件下可构成燃料电池,其负极的电极反应式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】配制下列溶液时常需加入少量括号内的物质,其中不是为了抑制离子水解的是
A.FeSO4(Fe) B.SnCl2(HCl) C.FeCl3(HCl) D.NaAlO2(NaOH)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能证明苯酚具有弱酸性的实验是()
A. 加入浓溴水生成白色沉淀
B. 苯酚钠溶液中通入CO2后,溶液由澄清变浑浊
C. 浑浊的苯酚加热后变澄清
D. 苯酚的水溶液中加NaOH溶液,生成苯酚钠
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物。某同学依据溴乙烷的性质,用右图实验装置(铁架台、酒精灯略)验证取代反应和消去反应的产物,请你一起参与探究。

实验操作Ⅰ:在试管中加入5 mL 1 mol/L NaOH溶液和5 mL 溴乙烷,振荡。
实验操作II:将试管如图固定后,水浴加热。
(1)用水浴加热而不直接用酒精灯加热的原因是______________________。
(2)观察到_____________________现象时,表明溴乙烷与NaOH溶液已完全反应。
(3)写出溴乙烷与NaOH溶液发生的反应方程式 ,为证明溴乙烷在NaOH乙醇溶液中发生的是消去反应,在你设计的实验方案中,需要检验的是______________,检验的方法是 (需说明:所用的试剂、简单的实验操作及预测产生的实验现象)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com