
”¾ĢāÄæ”æĻĀĮŠ·“Ó¦¼ČŹōÓŚŃõ»Æ»¹Ō·“Ó¦£¬ÓÖŹĒĪüČČ·“Ó¦µÄŹĒ
A. Ļ”ŃĪĖįÓėĒāŃõ»ÆÄʵķ“Ó¦ B. ¼×ĶéŌŚŃõĘųÖŠµÄČ¼ÉÕ·“Ó¦
C. NH4ClÓėBa(OH)2”¤8H2O·“Ó¦ D. ×ĘČȵÄĢ¼ÓėCO2µÄ·“Ó¦
”¾“š°ø”æD
”¾½āĪö”æ
·“Ó¦Ē°ŗóÓŠŌŖĖŲ»ÆŗĻ¼Ū·¢Éś±ä»ÆµÄ·“Ó¦ŹĒŃõ»Æ»¹Ō·“Ó¦£¬·“Ó¦Īļ×ÜÄÜĮæµĶÓŚÉś³ÉĪļ×ÜÄÜĮæµÄŹĒ·“Ó¦ŹĒĪüČČ·“Ó¦£¬¾Ż“Ė½ā“š”£
A. Ļ”ŃĪĖįÓėĒāŃõ»ÆÄʵķ“Ó¦ŹōÓŚ·ÅČČ·“Ó¦£¬ĒŅ²»ŹĒŃõ»Æ»¹Ō·“Ó¦£¬A“ķĪó£»
B. ¼×ĶéŌŚŃõĘųÖŠµÄČ¼ÉÕ·“Ó¦ŹĒŃõ»Æ»¹Ō·“Ó¦£¬µ«ŹōÓŚ·ÅČČ·“Ó¦£¬B“ķĪó£»
C. NH4ClÓėBa(OH)2”¤8H2O·“Ó¦ŹĒĪüČČ·“Ó¦£¬µ«²»ŹĒŃõ»Æ»¹Ō·“Ó¦£¬C“ķĪó£»
D. ×ĘČȵÄĢ¼ÓėCO2µÄ·“Ó¦ŹōÓŚĪüČȵÄŃõ»Æ»¹Ō·“Ó¦£¬DÕżČ·”£
“š°øŃ”D”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĘųĢå“óĮæÅŷŵ½æÕĘųÖŠ»įµ¼ÖĀĖįÓźŠĪ³ÉµÄŹĒ£Ø £©
A.SO2B.CO2C.COD.NH3
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŅČ²£ØCH”ŌCH£©ŹĒÖŲŅŖµÄ»Æ¹¤ŌĮĻ£¬¹ć·ŗÓ¦ÓĆÓŚŗøøī”¢Č¼ĮĻµē³Ų¼°ÓŠ»śŗĻ³ÉµČ”£
£Ø1£©ŅŅČ²-æÕĘųČ¼ĮĻµē³ŲŹĒŅ»ÖÖ¼īŠŌ£Ø20%-30%µÄKOHČÜŅŗ£©Č¼ĮĻµē³Ų”£µē³Ų·ÅµēŹ±£¬øŗ¼«µÄµē¼«·“Ó¦Ź½ĪŖ_____________£»
£Ø2£©æĘѧ¼ŅĄūÓĆ”°×éŗĻ×Ŗ»Æ¼¼Źõ”±£¬½«ŅŅČ²Č¼ÉÕ²śĪļCO2×Ŗ»Æ³ÉŅŅĻ©£¬·“Ó¦Ź½ĪŖ£ŗ6H2(g)+2CO2(g)![]() CH2=CH2(g)+4H2O(g)ĻĀĶ¼ĪŖĪĀ¶Č¶ŌCO2Ę½ŗā×Ŗ»ÆĀŹ”¢“߻ƼĮ“߻Ɗ§ĀŹµÄÓ°Ļģ”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ_____(ĢīŠņŗÅ)
CH2=CH2(g)+4H2O(g)ĻĀĶ¼ĪŖĪĀ¶Č¶ŌCO2Ę½ŗā×Ŗ»ÆĀŹ”¢“߻ƼĮ“߻Ɗ§ĀŹµÄÓ°Ļģ”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ_____(ĢīŠņŗÅ)
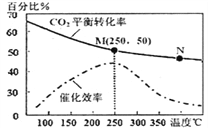
¢Ł250”ꏱ£¬“߻ƼĮµÄ“߻Ɗ§ĀŹ×ī“ó
¢ŚĖę×ÅĪĀ¶ČÉżøߣ¬ŅŅĻ©µÄ²śĀŹŌö“ó
¢ŪMµćĘ½ŗā³£Źż±ČNµćĘ½ŗā³£Źż“ó
¢ÜNµćÕż·“Ó¦ĖŁĀŹŅ»¶Ø“óÓŚMµćÕż·“Ó¦ĖŁĀŹ
¢ŻŌö“óŃ¹ĒææÉĢįøßŅŅĻ©µÄĢå»ż·ÖŹż
£Ø3£©¼×ĶéĮŃ½ā·ØÖĘČ”ŅŅČ²µÄ·“Ó¦·½³ĢŹ½ĪŖ£ŗ2CH4(g£©![]() C2H2(g£©+3H2(g£©”£ŅŃÖŖ£ŗ
C2H2(g£©+3H2(g£©”£ŅŃÖŖ£ŗ
CH4£Øg£©+2O2£Øg£©=CO2£Øg£©+2H2O£Øl£© ”÷H1= a kJ”¤mol-1
C2H2£Øg£©+2.5O2£Øg£©=2CO2£Øg£©+H2O£Øl£© ”÷H2= b kJ”¤mol-1
2H2£Øg£©+O2£Øg£©=2H2O£Øl£© ”÷H3= c kJ”¤mol-1
Ōņ2CH4(g£©![]() C2H2(g£©+3H2(g£© ”÷H=______kJ”¤mol-1
C2H2(g£©+3H2(g£© ”÷H=______kJ”¤mol-1
£Ø4£©¹žĖ¹ĢŲŃŠ¾æ·¢ĻÖ£ŗ¼×ĶéĮŃ½āŹ±£¬¼øÖÖĘųĢåĘ½ŗāŹ±·ÖŃ¹£ØPa£©ÓėĪĀ¶Č£Ø”ę£©Ö®¼äµÄ¹ŲĻµČēĶ¼ĖłŹ¾”£¼×ĶéĮŃ½āæÉÄÜ·¢ÉśµÄ·“Ó¦ÓŠ£ŗ2CH4(g£©![]() C2H2(g£©+3H2(g£©£¬2CH4(g£©
C2H2(g£©+3H2(g£©£¬2CH4(g£©![]() C2H4(g£©+2H2(g£©”£
C2H4(g£©+2H2(g£©”£
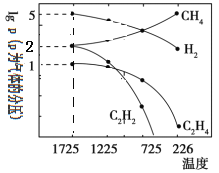
¢Ł1725”ꏱ£¬Ļņ1LŗćČŻĆܱÕČŻĘ÷ÖŠ³äČė0.3molCH4£¬“ļµ½Ę½ŗāŹ±£¬²āµĆc£ØC2H2£©=c£ØCH4£©”£ŌņCH4Éś³ÉC2H2µÄĘ½ŗā×Ŗ»ÆĀŹĪŖ_______£»
¢Ś1725”ꏱ£¬·“Ó¦2CH4(g£©![]() C2H2(g£©+3H2(g£©µÄĘ½ŗā³£ŹżKp=_________£ØÓĆĘ½ŗā·ÖŃ¹“śĢęĘ½ŗāÅØ¶Č£©£»
C2H2(g£©+3H2(g£©µÄĘ½ŗā³£ŹżKp=_________£ØÓĆĘ½ŗā·ÖŃ¹“śĢęĘ½ŗāÅØ¶Č£©£»
¢ŪÓÉĶ¼æÉÖŖ£¬¼×ĶéĮŃ½āÖĘŅŅČ²ÓŠø±²śĪļŅŅĻ©Éś³É”£ĪŖĢįøß¼×ĶéÖĘŅŅČ²µÄ²śĀŹ£¬³żøıäĪĀ¶ČĶā£¬»¹æɲÉČ”µÄ“ėŹ©ÓŠ_______”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ£Ø1£©·Ö±šŠ“³öŅŅČ©ÓėŅų°±ČÜŅŗ”¢±½·ÓÄĘČÜŅŗÖŠĶØČėÉŁĮæCO2·“Ó¦µÄĄė×Ó·½³ĢŹ½:__________________________________”¢__________________________________”£
£Ø2£©ŅŅĻ©ŹĒŅ»ÖÖÖŲŅŖµÄ»Æ¹¤ŌĮĻ£¬ŅŌŅŅĻ©ĪŖŌĮĻŃÜÉś³ö²æ·Ö»Æ¹¤²śĘ·µÄ·“Ó¦ČēĻĀ£Ø²æ·Ö·“Ó¦Ģõ¼žŅŃĀŌČ„£©£ŗĒė»Ų“šĻĀĮŠĪŹĢā£ŗ

£Ø1£©AµÄ»ÆѧĆū³ĘŹĒ_____£»
£Ø2£©BŗĶA·“Ӧɜ³ÉCµÄ»Æѧ·½³ĢŹ½ĪŖ________£¬øĆ·“Ó¦µÄĄąŠĶĪŖ_____________
£Ø3£©D£Ø»·×“»ÆŗĻĪļ£©µÄ½į¹¹¼ņŹ½ĪŖ___________£»
£Ø4£©FµÄ½į¹¹¼ņŹ½ĪŖ_____________£»
£Ø5£©DµÄĶ¬·ÖŅģ¹¹ĢåµÄ½į¹¹¼ņŹ½ĪŖ___________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻÖÓŠČż×éČÜŅŗ£ŗ¢Ł²Ė×ŃÓĶŗĶĀČ»ÆÄĘČÜŅŗ ¢Ś75%µÄŅ½ÓĆ¾Ę¾« ¢ŪĀČ»ÆÄĘŗĶµ„ÖŹäåµÄĖ®ČÜŅŗ£¬·ÖĄėŅŌÉĻø÷»ģŗĻŅŗµÄÕżČ··½·ØŅĄ“ĪŹĒ£Ø £©
A.¹żĀĖ ŻĶČ” ·ÖŅŗ
B.ŻĶČ” ·ÖŅŗ ÕōĮó
C.·ÖŅŗ ÕōĮó ŻĶČ”
D.ŻĶČ” ÕōĮó ·ÖŅŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”ææĘѧ¼Ņ¶ŌŅ»Ģ¼»Æѧ½ųŠŠĮĖ¹ć·ŗÉīČėµÄŃŠ¾æ²¢Č”µĆĮĖŅ»Š©ÖŲŅŖ³É¹ū”£
£Ø1£©ŅŃÖŖ£ŗCO(g)+2H2(g)![]() CH3OH(g) ¦¤H1=-90.1kJ”¤mol-1£»
CH3OH(g) ¦¤H1=-90.1kJ”¤mol-1£»
3CH3OH(g)![]() CH3CH=CH2(g)+3H2O(g) ¦¤H2=-31.0 kJ”¤mol-1”£
CH3CH=CH2(g)+3H2O(g) ¦¤H2=-31.0 kJ”¤mol-1”£
COÓėH2ŗĻ³ÉCH3CH=CH2µÄČČ»Æѧ·½³ĢŹ½ĪŖ______________________________________”£
£Ø2£©ĻÖĻņČżøöĢå»ż¾łĪŖ2LµÄŗćČŻĆܱÕČŻĘ÷¢ń”¢¢ņ”¢¢óÖŠ£¬¾ł·Ö±š³äČė1molCOŗĶ2molH2£¬·¢Éś·“Ó¦£ŗCO(g)+2H2(g)![]() CH3OH(g) ¦¤H=-90.1kJ”¤mol-1”£ČżøöČŻĘ÷µÄ·“Ó¦ĪĀ¶Č·Ö±šĪŖT1”¢T2”¢T3ĒŅŗć¶Ø²»±ä”£µ±·“Ó¦¾ł½ųŠŠµ½5minŹ±H2µÄĢå»ż·ÖŹżČēĶ¼1ĖłŹ¾£¬ĘäÖŠÖ»ÓŠŅ»øöČŻĘ÷ÖŠµÄ·“Ó¦ŅŃ¾“ļµ½Ę½ŗāדĢ¬”£
CH3OH(g) ¦¤H=-90.1kJ”¤mol-1”£ČżøöČŻĘ÷µÄ·“Ó¦ĪĀ¶Č·Ö±šĪŖT1”¢T2”¢T3ĒŅŗć¶Ø²»±ä”£µ±·“Ó¦¾ł½ųŠŠµ½5minŹ±H2µÄĢå»ż·ÖŹżČēĶ¼1ĖłŹ¾£¬ĘäÖŠÖ»ÓŠŅ»øöČŻĘ÷ÖŠµÄ·“Ó¦ŅŃ¾“ļµ½Ę½ŗāדĢ¬”£
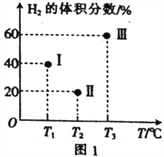
¢Ł5minŹ±ČżøöČŻĘ÷ÖŠµÄ·“Ó¦“ļµ½»ÆŃ§Ę½ŗāדĢ¬µÄŹĒČŻĘ÷_____________£ØĢīŠņŗÅ£©”£
¢Ś0~5minÄŚČŻĘ÷¢ńÖŠÓĆCH3OH±ķŹ¾µÄ»Æѧ·“Ó¦ĖŁĀŹv(CH3OH)=_________________”£
¢Ūµ±ČżøöČŻĘ÷ÖŠµÄ·“Ó¦¾ł“ļµ½Ę½ŗāדĢ¬Ź±£¬COµÄ×Ŗ»ÆĀŹ×īøߵďĒČŻĘ÷____________£ØĢīŠņŗÅ£¬ĻĀĶ¬£©£»Ę½ŗā³£Źż×īŠ”µÄŹĒČŻĘ÷____________________”£
£Ø3£©CO³£ÓĆÓŚ¹¤ŅµŅ±Į¶½šŹō£¬ŌŚ²»Ķ¬ĪĀ¶ČĻĀÓĆCO»¹ŌĖÄÖÖ½šŹōŃõ»ÆĪļ£¬“ļµ½Ę½ŗāŗóĘųĢåÖŠlg![]() ÓėĪĀ¶Č£ØT£©µÄ¹ŲĻµČēĶ¼2ĖłŹ¾”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ_____________£ØĢī×ÖÄø£©”£
ÓėĪĀ¶Č£ØT£©µÄ¹ŲĻµČēĶ¼2ĖłŹ¾”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ_____________£ØĢī×ÖÄø£©”£
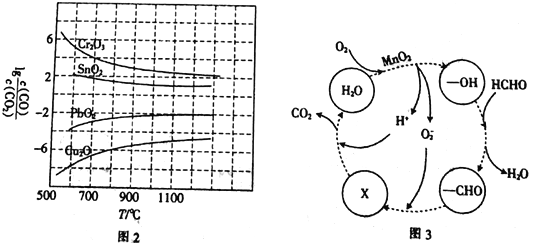
a.¹¤ŅµÉĻæÉŅŌĶعżŌöøß·“ӦװÖĆĄ“ŃÓ³¤æóŹÆŗĶCO½Ó“„µÄŹ±¼ä£¬¼õÉŁĪ²ĘųÖŠCOµÄŗ¬Įæ
b.COÓĆÓŚ¹¤ŅµŅ±Į¶½šŹōøõ(Cr)Ź±£¬»¹ŌŠ§ĀŹ²»øß
c.¹¤ŅµŅ±Į¶½šŹōĶ(Cu)Ź±£¬600”ęĻĀCOµÄĄūÓĆĀŹ±Č100”ęĻĀCOµÄĄūÓĆĀŹøü“ó
d.CO»¹ŌPbO2·“Ó¦µÄ¦¤H>0
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¶ĢÖÜĘŚŌŖĖŲX”¢Y”¢Z”¢WŌŚÖÜĘŚ±ķÖŠµÄĪ»ÖĆ¹ŲĻµČēĶ¼”£ĻĀĮŠĖµ·ØŅ»¶Ø²»ÕżČ·µÄŹĒ
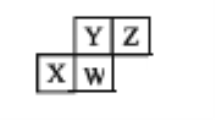
A. ZŌ×Ó±ČXŌ×ÓµÄ×īĶā²ćµē×ÓŹż¶ą2øö
B. Ō×Ó°ė¾¶£ŗW>X>Z>Y
C. ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦µÄĖ®»ÆĪļµÄ¼īŠŌ£ŗX>W
D. Yµ„ÖŹÓėĒāĘų·“Ó¦Ģõ¼ž±ČZµ„ÖŹøüæĮæĢ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ2012Äź2ŌĀ27ČÕ£¬Ą„Ć÷ŹŠŅ»¾ÓĆń·æŅņŅŗ»ÆĘųŠ¹Ā©Ņż·¢»šŌÖ”£ŅŃÖŖŅŗ»ÆĘųµÄÖ÷ŅŖ³É·ÖŹĒ±ūĶ飬ĻĀĮŠÓŠ¹Ų±ūĶéµÄŠšŹö²»ÕżČ·µÄŹĒ£Ø”” £©
A. ŹĒÖ±Į“Ģž£¬µ«·Ö×ÓÖŠĢ¼Ō×Ó²»ŌŚŅ»ĢõÖ±ĻßÉĻ
B. ŌŚ¹āÕÕĢõ¼žĻĀÄܹ»ÓėĀČĘų·¢ÉśČ”“ś·“Ó¦
C. ±ūĶé±Č¶”ĶéŅ×Ęū»Æ
D. 1 mol±ūĶéĶźČ«Č¼ÉÕĻūŗÄ5 mol O2
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŌĻĀŹĒÉśĪļĢåÄŚĖÄÖÖÓŠ»śĪļµÄ×é³ÉÓė¹¦ÄܹŲĻµĶ¼£¬ÓŠ¹ŲŠšŹö“ķĪóµÄŹĒ

A. Š”ĀóÖÖ×ÓĻø°ūÖŠ£¬ĪļÖŹAŹĒĘĻĢŃĢĒ£¬ĪļÖŹEŹĒµķ·Ū
B. ĻąĶ¬ÖŹĮæµÄEŗĶF³¹µ×Ńõ»Æ·Ö½ā£¬ŹĶ·ÅÄÜĮæ½Ļ¶ąµÄŹĒF
C. ĪļÖŹCµÄÖÖĄąŌ¼ÓŠ20ÖÖ£¬»ł±¾×é³ÉŌŖĖŲŹĒC”¢H”¢O”¢N
D. SARS²”¶¾µÄĪļÖŹH³¹µ×Ė®½āŗ󣬲śĪļŹĒCO2ŗĶH2O
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com