

 ,其中H2SO3的还原性最强,KMnO4的氧化性最强。对此反应体系:
,其中H2SO3的还原性最强,KMnO4的氧化性最强。对此反应体系:


科目:高中化学 来源:不详 题型:实验题
| 第1组 | 第2组 | 第3组 |
| S (单质) | SO2、H2SO3、M、NaHSO3 | SO3、H2SO4、Na2SO4、 NaHSO4 |

| n(SO32—):n(HSO3—) | 91:9 | 1:1 | 9:91 |
| pH | 8.2 | 7.2 | 6.2 |
| 序号 | 实验方案 | 实验现象 | 结论 |
| 方案① | 往第一份试液中加入KMnO4溶液溶液 | 紫红色褪去 | SO2与Fe3+反应生成了Fe2+ |
| 方案② | 往第二份试液中加入 | | SO2与Fe3+反应生成了Fe2+ |
| 方案③ | 往第二份试液中加入 | | SO2与Fe3+反应生成了SO42— |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题


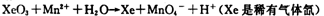


查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.NaCl是氧化产物,NaClO3是还原产物 | B.该反应中的电子转移数目为6e- |
| C.氧化剂和还原剂的质量比是1∶5 | D.Cl2既是氧化剂也是还原剂 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.NO+NO2+2NaOH==2NaNO3+H2O | B.NH3+HCl== NH4Cl |
| C.Br2+2KI==I2+2KBr | D.2H2O2==2H2O+O2↑ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
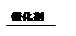 N2 + CO2,下列关于此反应的说法中,错误的是( )
N2 + CO2,下列关于此反应的说法中,错误的是( )| A.所涉及元素中原子半径: C>N>O |
| B.氧化剂与还原剂的物质的量之比为1︰1时,NOx中氮元素的化合价为+2价 |
| C.当x = 2时,每生成1mol N2,转移电子数为4mol ,N2为氧化产物 |
| D.等物质的量N2和CO2中,共价键的个数比为3︰4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com