
| A、KH中H是-1价 |
| B、该反应转移的电子数为2个 |
| C、H2是氧化产物,也是还原产物 |
| D、KH可以在野外生存时做应急生氢药品 |


 导学全程练创优训练系列答案
导学全程练创优训练系列答案科目:高中化学 来源: 题型:
| A、能量变化是化学反应的基本特征之一 |
| B、化学反应都伴随着能量变化和其他各种现象的出现 |
| C、拆开物质中的化学键一定需要吸收能量 |
| D、形成化学键的过程一定释放能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、化合物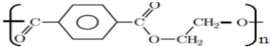 名称为聚对苯甲二酸乙二酯 名称为聚对苯甲二酸乙二酯 |
| B、C3H7OH与C4H9OH分子间脱水,最多可生成6种醚 |
C、1mol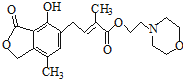 最多可与含4mol NaOH的水溶液完全反应 最多可与含4mol NaOH的水溶液完全反应 |
D、某油脂的化学式为 ,它属于酯类但不属于高分子化合物 ,它属于酯类但不属于高分子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com