
【题目】很多鲜花和水果的香味都来自酯的混合物。下图是乙烯等为原料制取乙酸乙酯的过程(部分产物和反应条件已略去)。
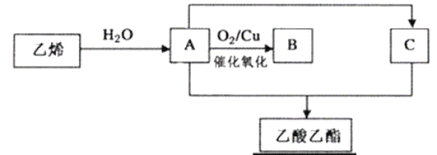
请回答下列问题:
(1)B的结构简式为______________。
(2)乙烯与水反应生成A的反应类型为______________。
(3)A与C反应生成乙酸乙酯的化学方程式为__________,其反应类型为__________。
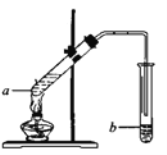
(4)实验室可用如图装置制取乙酸乙酯。
①在试管a中加好相关试剂后,还需要加入2—3块的碎瓷片,其作用是__________。
②试管b中盛有饱和碳酸钠溶液,生成的乙酸乙酯在该溶液的_______(填“上”或“下”)层,用分液的方法分离出该产品所需的主要仪器是________。试管b中的导管口应在液面上方而不伸入到液面以下,其原因是______________。
【答案】CH3CHO加成反应CH3CH2OH+CH3COOH![]() CH3COOCH2CH3+H2O酯化(或取代)反应防止暴沸上分液漏斗(烧杯等)防止倒吸
CH3COOCH2CH3+H2O酯化(或取代)反应防止暴沸上分液漏斗(烧杯等)防止倒吸
【解析】
乙烯在催化剂条件下与水发生加成反应生成CH3CH2OH,则A为CH3CH2OH,CH3CH2OH被催化氧化可生成CH3CHO,则B为CH3CHO,乙醇和C反应生成乙酸乙酯,则C应为CH3COOH。据此分析可得结论。
(1)由以上分析可得B为CH3CHO,故答案为:CH3CHO;(2)乙烯在催化剂条件下与水发生加成反应生成CH3CH2OH,方程式为CH2═CH2 + H2O![]() CH3CH2OH,故答案为:加成反应;(3)乙酸与乙醇在浓硫酸作用下的酯化反应或或取代反应生成乙酸乙酯,反应的方程式为CH3CH2OH + CH3COOH
CH3CH2OH,故答案为:加成反应;(3)乙酸与乙醇在浓硫酸作用下的酯化反应或或取代反应生成乙酸乙酯,反应的方程式为CH3CH2OH + CH3COOH ![]() CH3COOCH2CH3 + H2O,故答案为:CH3CH2OH + CH3COOH
CH3COOCH2CH3 + H2O,故答案为:CH3CH2OH + CH3COOH![]() CH3COOCH2CH3 + H2O;酯化反应或取代反应;(4)①在试管a中加入2—3块的碎瓷片,其作用是防止暴沸,故答案为:防止暴沸;②乙酸乙酯的密度小于水,在上层,分液所需的主要仪器是分液漏斗。试管b中的导管口应在液面上方而不伸入到液面以下,是防止倒吸,故答案为:上;分液漏斗(烧杯等);防止倒吸。
CH3COOCH2CH3 + H2O;酯化反应或取代反应;(4)①在试管a中加入2—3块的碎瓷片,其作用是防止暴沸,故答案为:防止暴沸;②乙酸乙酯的密度小于水,在上层,分液所需的主要仪器是分液漏斗。试管b中的导管口应在液面上方而不伸入到液面以下,是防止倒吸,故答案为:上;分液漏斗(烧杯等);防止倒吸。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】利用下图装置测定中和热的实验步骤如下:

①用量筒量取50 mL 0.25 mol·L-1硫酸倒入小烧杯中,测出硫酸温度;
②用另一量筒量取50 mL 0.55 mol·L-1NaOH溶液,并用另一温度计测出其温度;
③将NaOH溶液倒入小烧杯中,设法使之混合均匀,测出混合液最高温度。
回答下列问题:
(1)倒入NaOH溶液的正确操作是__________。
A.沿玻璃棒缓慢倒入 B.分三次少量倒入 C.一次迅速倒入
(2)使硫酸与NaOH溶液混合均匀的正确操作是________。
A.用温度计小心搅拌 B.揭开硬纸片用玻璃棒搅拌
C.轻轻地振荡烧杯 D.用套在温度计上的环形玻璃搅拌棒轻轻地搅动
(3)搅拌棒为何不用铜质的_____________.
(4)实验数据如下表:
①请填写下表中的空白:________。
温度 实验次数 | 起始温度 | 终止温度
| 温度差平均值 | ||
H2SO4 | NaOH | 平均值 | |||
1 | 26.2 | 26.0 | 26.1 | 29.5 | |
2 | 27.0 | 27.4 | 27.2 | 32.3 | |
3 | 25.9 | 25.9 | 25.9 | 29.2 | |
4 | 26.4 | 26.2 | 26.3 | 29.8 | |
②近似认为0.55 mol·L-1NaOH溶液和0.25 mol·L-1硫酸溶液的密度都是1 g·cm-3,中和后生成溶液的比热容c=4.18 J·g-1·℃-1。依据上表数据计算中和热ΔH=________(取小数点后一位)。
③中和热测定实验中,下列操作一定会降低实验准确性的是______。
A.滴定管(精量仪器,读数保留到0.01)取所用酸碱溶液的体积
B.NaOH溶液在倒入小烧杯时,有少量溅出
C.大、小烧杯体积相差较大,夹层间放的碎泡沫塑料较多
D.测量硫酸溶液的温度计用水洗净后才用来测NaOH溶液的温度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2 L容器中有3种物质进行反应,X、Y、Z的物质的量随时间的变化曲线如图所示,反应在t时刻达到平衡。

(1)该反应的化学方程式是____________。
(2)反应起始至t时刻,Y的平均反应速率是_______________。
(3)关于该反应的说法,正确的是______。
A.到达t时刻该反应已停止
B.加入催化剂,一定能加快反应速率
C.在t时刻正反应速率等于逆反应速率
D.增大压强,一定能加快反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示是一种以液态肼(N2H4)为燃料,氧气为氧化剂,某固体氧化物为电解质的新型燃料电池。该固体氧化物电解质的工作温度高达700~900℃时,O2-可在该固体氧化物电解质中自由移动,反应生成物均为无毒无害的物质。
下列说法正确的是

A. 电池内的O2-由电极乙移向电极甲
B. 电池总反应为N2H4+2O2=2NO+2H2O
C. 当甲电极上有1molN2H4消耗时,乙电极上有1mol被氧化
D. 电池外电路的电子由电极乙移向电极甲
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列①~⑧中物质间的反应不能产生气体的是 ( )
①石灰石和盐酸 ②冷浓硫酸中投入铝片 ③石英与苏打混和加强热 ④石墨与高温水蒸气 ⑤过氧化钠与水 ⑥氟与水 ⑦钠与硫酸铜溶液 ⑧碳酸氢钠与氢氧化钠溶液
A.①和⑤B.④和⑦C.③和⑦D.②和⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E五种短周期元素,A、B同主族,C、D同周期,B、E同周期。气体A2与气体C2混合后点燃能够发生爆炸,且产物在常温常压下是一种无色无味的液体。B、C、E简单离子的核外电子排布相同。E的最高价氧化物可与B的最高价氧化物的水化物反应生成一种易溶于水的的盐,D能形成自然界硬度最大的单质。请根据上述所提供的信息回答下列问题。
(1)写出A、B两种元素的元素名称:A________、B________写出D的最高价氧化物的电子式___________。
(2)写出由B和C两元素形成的原子个数比为1:1的化合物F存在的化学键是_______________________
(3)写出F和A2C反应的离子方程式:________________________________。
(4)潜艇中使用的液氨-液氧燃料电池工作原理如图2所示:

①电极b名称是____。
②电解质溶液中OH-离子向____移动(填“电极a”或“电极b”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】5种物质已按沸点由低到高顺序排列),则正己烷最可能插入的位置是( )
① | ② | ③ | ④ | ⑤ |
甲烷 | 乙烯 | 戊烷 | 2-甲基戊烷 | 甲苯 |
A.③④之间B.②③之间C.④⑤之间D.⑤之后
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2008年初我国南方遭遇的冰雪灾害中,使用了一种融雪剂,其主要成分的化学式为XY2,X原子的结构示意图![]() X的阳离子与Y的阴离子的电子层结构相同。元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,Z与Y相邻且Z、W能形成一种WZ2型分子。
X的阳离子与Y的阴离子的电子层结构相同。元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,Z与Y相邻且Z、W能形成一种WZ2型分子。
(1)m=________,该融雪剂的化学式为________。
(2)Z、W元素的名称为________、_______。
(3)下列说法正确的是________。
A.XY2和WZ2都为离子化合物
B.XY2分子中仅含离子键,WZ2中仅含极性共价键
C.H2Z比HY的稳定性强
D.X的阳离子比Y的阴离子半径大
(4)下列化学用语表达正确的是________。
A.XY2的电子式:![]()
B.WZ2的结构式:Z=W=Z
C.Y元素的单质与H2Z水溶液反应的离子方程式为:Y2+Z2-=2Y+Z↓
D.用电子式表示XY2的形成过程为:![]()
(5)冰雪的化学成分是H2O,水的沸点比H2Z的沸点高,其原因是_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,在体积一定的密闭容器中加入1 mol N2和3 mol H2发生反应:
N2+ 3H2![]() 2NH3(正反应是放热反应)。下列有关说法正确的是( )
2NH3(正反应是放热反应)。下列有关说法正确的是( )
A. 降低温度可以加快反应速率
B. 达到化学反应限度时,生成2mol NH3
C. 向容器中再加入N2可以加快反应速率
D. 1mol N2和3mol H2的总能量低于2mol NH3的总能量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com