
已知X、M都是中学教材常见元素,下列对两个离子反应通式的推断中,其中正确的是
(甲)XO3n-+Xn-+H+→X单质+H2O(未配平);(乙)Mm++mOH-=M(OH)m↓
①若n=1,则XO3n-中X元素为+5价,X位于周期表第ⅤA族
②若n=2,则X最高价氧化物的水化物可能与它的氢化物反应
③若m=1,则M(NO3)m溶液和氨水互滴时的现象可能不同
④若m=2,则在空气中蒸干、灼烧MSO4溶液一定能得到MSO4
⑤若m=3,则MCl3与足量氢氧化钠溶液反应一定生成M(OH)m
A.④⑤ B.①③ C.②③ D.①②
 阳光课堂课时优化作业系列答案
阳光课堂课时优化作业系列答案科目:高中化学 来源: 题型:
已知① CH3CH2OH  CH2=CH2↑+H20
CH2=CH2↑+H20
CH2=CH2+Br2  BrCH2—CH2Br
BrCH2—CH2Br
②乙醇、1,2-二溴乙烷、乙醚的有关物理性质如下表所示。
乙醇 | 1,2-二溴乙烷 | 乙醚 | |
通常状况下的状态 | 无色液体 | 无色液体 | 无色液体 |
密度/g·cm-3 | 0.79 | 2.2 | 0.71 |
熔点/℃ | -130 | 9 | -116 |
沸点/℃ | 78.5 | 132 | 34.6 |
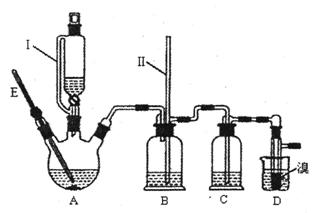 某化学小组拟用乙醇、溴等为原料在实验室制备少量的1,2一二溴乙烷,实验装置如右图所示(装置A中的加热部分的仪器装置省略没有画出)。
某化学小组拟用乙醇、溴等为原料在实验室制备少量的1,2一二溴乙烷,实验装置如右图所示(装置A中的加热部分的仪器装置省略没有画出)。
(1)仪器E的名称是 。
(2)仪器Ⅰ是漏斗,其左部的玻璃管的作 用是 (填字母)。
a.使漏斗中液体容易滴下
b.有利于吸收气体杂质
c.防止A中三颈烧瓶里的液体爆沸
(3)实验时,A中三颈烧瓶里放入几片碎瓷片的目的是 。加热反应过程中,三颈烧瓶里除生成乙烯外,还可能生成的有机副产物主要是 。
(4)反应过程中,若B中长玻璃导管(Ⅱ)里的液面上升,则说明可能是由于 (填“D中出现堵塞”或“C中杂质已除尽”)造成的。
(5)反应过程中,D中需用冷水冷却盛有液溴的试管,其主要目的是 。
说明制备1,2-二溴乙烷的反应已经结束的实验现象是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:2M(g) N(g);△H <0。现将M和N的混和气体通入体积为1L的恒温密闭容器
N(g);△H <0。现将M和N的混和气体通入体积为1L的恒温密闭容器
 中,反应体系中物质浓度随时间变化关系如右图所示。下列说法正确的是( )
中,反应体系中物质浓度随时间变化关系如右图所示。下列说法正确的是( )
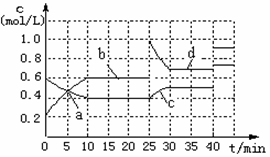
 A.a、b、c、d四个点中处于平衡状态的点是a、b
A.a、b、c、d四个点中处于平衡状态的点是a、b
 B.反应进行至25min时,曲线发生变化的原因是加入
B.反应进行至25min时,曲线发生变化的原因是加入 了 0.4molN
了 0.4molN
 C.若调节温度使35min时体系内N的百分含量与
C.若调节温度使35min时体系内N的百分含量与 15min时相等,应升高温度
15min时相等,应升高温度
 D.若40min后出现如图所示变化,则可能是加入了
D.若40min后出现如图所示变化,则可能是加入了 某种催化剂
某种催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式正确的是 ( )
A.NH4HCO3溶液与过量NaOH溶液反应:NH 4++ OH―=NH3↑+ H2O
B.用惰性电极电解饱和氯化钠溶液:2Cl― + 2H +  H2↑+ Cl2↑
H2↑+ Cl2↑
C.向Fe(NO3)3溶液中加入过量的HI溶液:2Fe3++2I― = 2Fe2++I2
D.Na2SO3溶液使酸性KMnO4溶液褪色:5SO32― + 6H+ + 2MnO4―=5SO4 2― + 2Mn2+ +3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
Ⅰ、(4分)(1)某化学兴趣小组欲从下列装置中选取必要的装置制取(NH4)2SO4溶液,连接的顺序(用接口序号字母表示)是:a
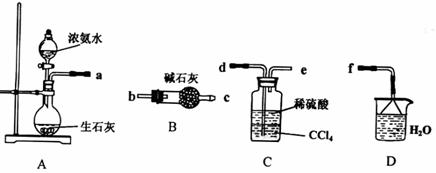
(2)将装置C中两种液体分离开的操作名称是__ _______。
装置D的作用是 。
Ⅱ、(4分)为提高氯化铵的经济价值,我国化学家设计了利用氢氧化镁热分解氯化铵制氨气并得到碱式氯化镁(MgOHCl)的工艺。某同学根据该原理设计的实验装置如图:

请回答下列问题:
(1) 装置A中发生反应生成碱式氯化镁的化学方程式为_________ ____
装置B中碱石灰的作用是_____ __
(2) 反应过程中持续通入N2的作用有两点:一是使反应产生的氨气完全导出并被稀硫酸充分吸收,二是_______________ ______
(3) 装置C的试管中反应的离子方程式为 ______________
查看答案和解析>>
科目:高中化学 来源: 题型:
苯甲酸乙酯(C9H10O2)别名为安息香酸乙酯。 它是一种无色透明液体,不溶于水,稍有水果气味,用于配制香水香精和人造精油,大量用于食品工业中,也可用作有机合成中间体,溶剂等。其制备方法为:
|

已知:
| 名称 | 相对分子质量 | 颜色,状态 | 沸点(℃) | 密度(g·cm-3) |
| 苯甲酸* | 122 | 无色片状晶体 | 249 | 1.2659 |
| 苯甲酸乙酯 | 150 | 无色澄清液体 | 212.6 | 1.05 |
| 乙醇 | 46 | 无色澄清液体 | 78.3 | 0.7893 |
| 环己烷 | 84 | 无色澄清液体 | 80.8 | 0.7318 |
 *苯甲酸在100℃会迅速升华。
*苯甲酸在100℃会迅速升华。
实验步骤如下:
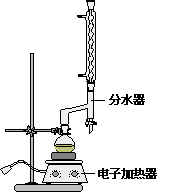
①在圆底烧瓶中加入12.20 g苯甲酸,25 mL 95%的乙醇(过量),20 mL环己烷以及4 mL浓硫酸,混合均匀并加入沸石,按右图所示装好仪器,控制温度在65~70℃加热回流2 h。利用分水器不断分离除去反应生成的水,回流环己烷和乙醇。
②反应结束,打开旋塞放出分水器中液体后,关闭旋塞,继续加热,至分水器中收集到的液体不再明显增加,停止加热。
③将烧瓶内反应液倒入盛有适量水的烧杯中,分批加入Na2CO3至溶液至呈中性。用分液漏斗分出有机层,水层用25 mL乙醚萃取分液,然后合并至有机层,加入氯化钙,静置,过滤,对滤液进行蒸馏,低温蒸出乙醚和环己烷后,继续升温,接收210~213℃的馏分。
④检验合格,测得产品体积为12.86 mL。
回答下列问题:
(1)在该实验中,圆底烧瓶的容积最适合的是 (填入正确选项前的字母)。
A.25 mL B.50 mL C.100 mL D.250 mL
(2)步骤①中使用分水器不断分离除去水的目的是 。
(3)步骤②中应控制馏分的温度在 。
A.65~70℃ B.78~80℃ C.85~90℃ D.215~220℃
(4)步骤③加入Na2CO3的作用是 ;若Na2CO3加入不足,在之后蒸馏时,蒸馏烧瓶中可见到白烟生成,产生该现象的原因是
。
(5)关于步骤③中的萃取分液操作叙述正确的是
A.水溶液中加入乙醚,转移至分液漏斗中,塞上玻璃塞,分液漏斗倒转过来,用力振摇
B.振摇几次后需打开分液漏斗上口的玻璃塞放气
C.经几次振摇并放气后,手持分液漏斗静置待液体分层
D.放出液体时,应打开上口玻璃塞或将玻璃塞上的凹槽对准漏斗口上的小孔
(6)计算本实验的产率为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验装置能达到实验目的的是(夹持仪器未画出)

A.①装置用于检验1-溴丙烷消去产物 B.②装置用于石油的分馏
C.③装置用于实验室制硝基苯 D.④装置可证明酸性:盐酸>碳酸>苯酚
查看答案和解析>>
科目:高中化学 来源: 题型:
元素X原子的最外层有3个电子,元素Y原子的最外层有6个电子,这两种元素形成的化合物的化学式可能是 ( )
A.XY2 B.X2Y3 C.X3Y2 D.X2Y
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com