
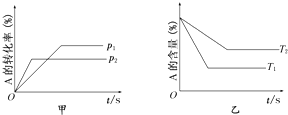
| A、p1<p2 T1>T2 |
| B、减小压强,正逆反应速率都减小,平衡右移 |
| C、△H>0△S>0 |
| D、升高温度,混合气体的平均摩尔质量增大 |
| 气体总质量 |
| 气体总物质的量 |


科目:高中化学 来源: 题型:
| 选项 | 实验目的 | 玻璃仪器 |
| A | 配制一定质量分数的NaCl溶液 | 胶头滴管、量筒、烧杯、玻璃棒 |
| B | 测定NaOH溶液浓度 | 滴定管、锥形瓶、烧杯 |
| C | 鉴别葡萄糖和蔗糖 | 试管、烧杯、酒精灯 |
| D | 实验室用浓氨水和生石灰制备氨气 | 普通漏斗、烧杯、玻璃棒 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
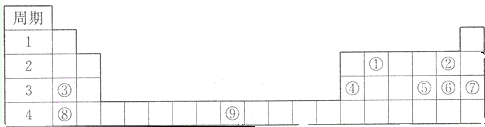
| A、①②⑤ | B、①③④ |
| C、②④⑤ | D、①③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
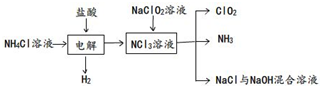
| A、①② | B、②③ | C、①③ | D、③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.2 mol/L |
| B、0.25 mol/L |
| C、0.45 mol/L |
| D、0.225 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1 mol/(L?min) |
| B、2mol/(L?min) |
| C、4 mol/(L?min) |
| D、8mol/(L?min) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com