
| A. | 2H2+O2 $\frac{\underline{\;点燃\;}}{\;}$2H2O | |
| B. | CaO+H2O=Ca(OH)2 | |
| C. | CaCO3 $\frac{\underline{\;\;△\;\;}}{\;}$CaO+CO2↑ | |
| D. | CH3CH2OH(酒精)+3O2 $\frac{\underline{\;点燃\;}}{\;}$2CO2+3 H2O |
分析 反应中生成物总能量高于反应物总能量,说明该反应是一个吸热反应,而常见的吸热反应有:①绝大多数的分解反应;②以H2、CO和C为还原剂的氧化还原反应;③Ba(OH)2•8H2O与NH4Cl的反应,据此分析.
解答 解:A、2H2+O$\frac{\underline{\;点燃\;}}{\;}$2H2O是燃烧反应,是一个放热反应,故A错误;
B、CaO+H2O=Ca(OH)2是一个放热反应,故B错误;
C、CaCO3$\frac{\underline{\;\;△\;\;}}{\;}$CaO+CO2↑是一个吸热反应,故C正确;
D、CH3CH2OH(酒精)+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O是燃烧反应,是一个放热反应,故D错误.
故选C.
点评 本题考查学生常见的反应的吸热放热情况,可以根据所学知识进行回答,难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 纳米材料的表面粒子数占粒子总数的比例很大,这是它有许多特殊性质的原因.假设某硼镁化合物的结构如图所示(六个硼原子位于棱柱内),则这种纳米颗粒的化学式( )
纳米材料的表面粒子数占粒子总数的比例很大,这是它有许多特殊性质的原因.假设某硼镁化合物的结构如图所示(六个硼原子位于棱柱内),则这种纳米颗粒的化学式( )| A. | Mg3B6 | B. | Mg14B6 | C. | MgB2 | D. | Mg5B12 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 硫的非金属性较强,所以只以化合态存在于自然界 | |
| B. | 分离黑火药(S、C、KNO3)的成分需要使用二硫化碳、水及过滤操作 | |
| C. | 硫与金属或非金属反应时均做氧化剂 | |
| D. | 1.6克硫与6.4克铜反应能得到8.0克纯净硫化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫化氢在氧气中燃烧 | B. | 铁在硫蒸气中燃烧 | ||
| C. | 二氧化硫通入石灰水中 | D. | 硫酸中加入铁粉 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2O 和Na2O2 | B. | CaCl2 和 Na2S | C. | CO2 和 CaO | D. | HCl 和NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用10ml的量筒准确量取8.80ml的稀硫酸 | |
| B. | 用NaOH溶液作标准液滴定未知浓度的醋酸,选择甲基橙做指示剂 | |
| C. | 测定中和反应的热反应,将碱缓慢倒入酸中,所测温度值不变 | |
| D. | 氯水或硝酸银溶液存放在配有磨口塞的棕色玻璃瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
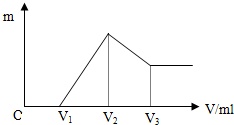 将0.1mol的镁、铝混合物溶于100ml 4mol/L的盐酸中,然后滴加NaOH溶液,在滴加NaOH溶液过程中,沉淀的质量m随加入NaOH溶液的体积V变化的关系如图所示.
将0.1mol的镁、铝混合物溶于100ml 4mol/L的盐酸中,然后滴加NaOH溶液,在滴加NaOH溶液过程中,沉淀的质量m随加入NaOH溶液的体积V变化的关系如图所示.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com