
| A.过量CO2通入澄清石灰水中:CO2 + Ca2+ + 2OH-= CaCO3↓ + H2O |
| B.Na2O2与水发生反应:O22-+ H2O = 2OH-+ H2↑ |
| C.向AlCl3溶液中加入过量的NaOH溶液: Al3+ + 3OH-= Al(OH)3↓ |
| D.Ca(HCO3)2与足量的NaOH溶液反应: Ca2+ + 2HCO3-+ 2OH-= CaCO3↓+ CO32-+ 2H2O |
 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案 期末金牌卷系列答案
期末金牌卷系列答案科目:高中化学 来源:不详 题型:单选题
A.铁钉在空气中出现红色的铁锈,其负极反应式为:Fe-3e- Fe3+ Fe3+ |
B.氢氧化镁白色沉淀溶于氯化铵溶液:Mg(OH)2+2N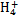  Mg2++2NH3·H2O Mg2++2NH3·H2O |
C.SO2通入到滴加酚酞的NaOH溶液中,红色变浅:SO2+2OH- S S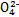 +H2O +H2O |
D.向K2Cr2O7溶液中加入少量NaOH浓溶液,溶液由橙色变为黄色:Cr2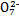 +H2O +H2O 2Cr 2Cr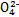 +2H+ +2H+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.苯酚钠溶液中通入少量CO2:2C6H5O-+CO2+H2O→2C6H5OH+CO32- |
B.甲醛溶液中加入足量的银氨溶液并加热:HCHO+2[Ag(NH3)2]++2OH- HCOO-+NH4++2Ag↓+3NH3+H2O HCOO-+NH4++2Ag↓+3NH3+H2O |
C.乙醛与碱性氢氧化铜悬浊液混合后加热至沸腾:CH3CHO+2Cu(OH)2+OH— Cu2O↓+CH3COO—+3H2O Cu2O↓+CH3COO—+3H2O |
| D.向小苏打溶液中加入醋酸: CO32-+2CH3COOH =CO2↑+H2O+2CH3COO- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.金属钠溶于足量水中的离子方程式:Na+2H2O=Na++H2↑+2OH- |
| B.加入铝粉后产生大量氢气的溶液中:NH4+、Na+、NO3-、Cl-可以大量共存 |
| C.等物质的量浓度、等体积的氨水与盐酸混和,溶液中离子浓度关系为c(C1-)>c(NH4+)>c(OH-)>c(H+) |
| D.等物质的量的二元弱酸H2X与其钾盐K2X的混合溶液中c(K+)=c(H2X)+c(HX-)+c(X2-) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
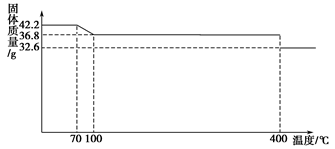
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 Fe(SCN)2+ K1="200" ②Fe(SCN)2++SCN-
Fe(SCN)2+ K1="200" ②Fe(SCN)2++SCN- Fe(SCN)2+ K2
Fe(SCN)2+ K2查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.稀硫酸滴在铁片上:2Fe + 6H+=2Fe3+ + 3H2 |
| B.氧化镁与稀盐酸混合:MgO + 2H+=Mg2+ + H2O |
| C.铜片插入硝酸银溶液中:Cu + Ag+=Cu2+ + Ag |
| D.氯气通人水中:Cl2+H2O=2H++Cl-+ Cl0- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.亚硫酸的电离:H2SO3 2H++ SO3 2H++ SO3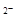 |
B.氯化铵水解的离子方程式为:NH4+ +H2O  NH3·H2O + H+ NH3·H2O + H+ |
C.NaHCO3水解的离子方程式为:HCO3-+H2O CO3 CO3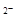 +H3O+ +H3O+ |
D.向氯化铝溶液中加入过量的氨水:A1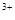 +3NH3·H2O= Al(OH)3↓+3NH4+ +3NH3·H2O= Al(OH)3↓+3NH4+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com