
【题目】有机物X和Y可作为“分子伞”给药载体的伞面和中心支撑架(未表示出原子或原子团的空间排列)。
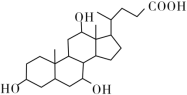
X(C24H40O5)
H2NCH2CH2CH2NHCH2CH2CH2CH2NH2 Y
下列叙述错误的是 ( )。
A.1 mol X在浓硫酸作用下发生消去反应,最多生成3 mol H2O
B.1 mol Y发生类似酯化的反应,最多消耗2 mol X
C.X与足量HBr反应,所得有机物的分子式为C24H37O2Br3
D.Y和癸烷的分子链均呈锯齿形,但Y的极性较强
科目:高中化学 来源: 题型:
【题目】(1)请根据氧化还原反应Fe+2H+=Fe2++H2↑设计成原电池:
①负极材料为:__________发生的电极反应是: ,电流__________(填“流出”或“流入”)
②正极发生的电极反应是: ,该反应为 (填“氧化反应”或“还原反应”) 。
③若电路中转移6.02×1022个e﹣,则产生标况下H2的体积为_____ _____。
(2)铁处于Ⅰ、Ⅱ、Ⅲ三种不同的环境中如图所示,则铁被腐蚀的速率由慢到快的顺序是(填序号) 。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用CO生产燃料甲醇。一定条件下发生反应:CO(g)+2H2(g) ![]() CH3OH(g)。一定条件下,将0.5molCO和0.5molH2在体积为2L的密闭容器中发生上述反应,则下列示意图合理的是 ( )
CH3OH(g)。一定条件下,将0.5molCO和0.5molH2在体积为2L的密闭容器中发生上述反应,则下列示意图合理的是 ( )
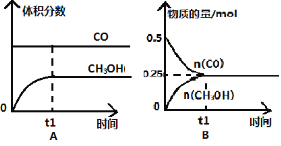
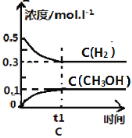

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组探究SO2气体还原Fe3+、I2,他们使用的药品和装置如下图所示:

(1)SO2与Fe3+反应的还原、氧化产物分别是 、 (填离子符号)。
(2)下列实验方案可以用于在实验室制取所需SO2的是 。
A.Na2SO3溶液与HNO3
B.Na2SO3固体与浓硫酸
C.固体硫在纯氧中燃烧
D.铜与热浓H2SO4
(3)装置C的作用是 。
(4)如果有280mL SO2气体(已折算为标态)进入C装置中,则C中,50mL NaOH溶液的浓度至少为 mol/L才能达到目的。
(5)在上述装置中通入过量的SO2为了验证A中SO2与Fe3+发生了氧化还原反应,他们取A中的溶液,分成三份,并设计了如下实验:
方案①:往第一份试液中加入KMnO4溶液,紫红色褪去。
方案②:往第一份试液加入KSCN溶液,不变红,再加入新制的氯水,溶液变红。
方案③:往第二份试液加入用稀盐酸酸化的BaCl2,产生白色沉淀。
上述方案不合理的是 ,原因是 。
(6)能表明I﹣的还原性弱于SO2的现象是 ,写出有关离子方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,请回答有关问题

(1)⑤和⑧的元素符号是_______和_______。
(2)表中最活泼的金属元素是___________,形成化合物种类最多的元素是_________(填写元素名称)。
(3)表中能形成两性氢氧化物的元素是___________,分别写出该元素的氢氧化物与⑥、⑨最高价氧化物的水化物反应的化学方程式:__________________;__________________。
(4)证明元素⑥、⑦非金属性强弱,用一个化学方程式表示:_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用KMnO4氧化溶质质量分数为36.5%的盐酸。反应方程式如下:
2KMnO4+16HCl═2KCl+2MnCl2+5Cl2↑+8H2O
(1)若此盐酸的密度为1.2g/cm3,其物质的量浓度为_________________________;
(2)用双线桥表示电子的得失_________________________;
(3)此反应中氧化剂是_________,氧化产物____________;
(4)若有xmolKMnO4参加反应,则转移电子的物质的量为____________;
(5)15.8gKMnO4完全反应,产生标准状况下Cl2的体积为_________,同时有________molHCl被氧化。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学上常用燃烧法确定有机物组成,这种方法是在电炉加热时用纯氧气氧化管内样品,根据产物的质量确定有机物的组成。下列装置是用燃烧法确定有机物分子式常用的装置。
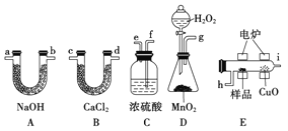
(1)产生的O2按从左到右的流向,所选装置各导管的正确连接顺序是 。
(2)C装置中浓硫酸的作用是 。
(3)D装置中MnO2的作用是 。
(4)燃烧管中CuO的作用是 。
(5)若实验中所取样品只含C、H、O三种元素中的两种或三种,准确称取0.92 g样品,经充分反应后,A管质量增加1.76 g,B管质量增加1.08 g,则该样品的实验式为 。
(6)用质谱仪测定其相对分子质量,得如图一所示的质谱图,则该有机物的相对分子质量为 。

(7)能否根据A的实验式确定A的分子式 (填“能”或“不能”),若能,则A的分子式是 (若不能,则此空不填)。
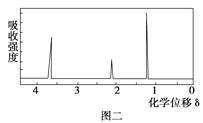
(8)该物质的核磁共振氢谱如图二所示,则其结构简式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四种短周期元素在周期表中的位置如图,其中只有M为金属元素。下列说法不正确的是

A. 原子半径Z<M
B. Y的最高价氧化物对应水化物的酸性比X的弱
C. X的最简单气态氢化物的热稳定性比Z的小
D. Z位于元素周期表中第2周期、第ⅥA族
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2015年“812”天津港危化仓库爆炸,造成生命、财产的特大损失。据查危化仓库中存有大量的钠、钾,硝酸铵和氰化钠(NaCN)。NaCN属于剧毒物质,若处理不当,极易污染土壤和海水。请回答下列问题:
(1)钠、钾着火,下列可用来灭火的是______________。
A.水 B.泡沫灭火器 C.干粉灭火器 D.细沙盖灭
(2)NH4NO3为爆炸物,在不同温度下受热分解,可发生不同的化学反应:
在110℃时:NH4NO3=NH3+HNO3
在185~200℃时:NH4NO3=N2O+2H2O
在230℃ 以上时,同时有弱光:2NH4NO3=2N2+O2+4H2O
在400℃ 以上时,发生爆炸:4NH4NO3=3N2+2NO2+8H2O
上述反应过程中一定破坏了______________。(填“离子键”或“共价键”或“离子键和共价键”)
(3)NaCN 的电子式为______________。下列能说明碳与氮两元素非金属性相对强弱的是______________。
A.酸性:HNO2>H2CO3
B.相同条件下水溶液的 pH:NaHCO3>NaNO3
C.CH4比NH3更稳定
D.C 与H2的化合比N2与H2的化合更容易
(4)海水中含有Ca2+、Mg2+、HCO3- 等杂质离子。用惰性电极电解海水时阴极易产生水垢,其主要成分是 Mg(OH)2和CaCO3。写出电解海水的离子方程式______________;生成CaCO3的离子方程式是______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com