
在生产、保存、运输和使用浓硫酸时,下列说法不正确的是
A.工业制取硫酸过程中生成的SO2可循环使用
B.常温下可选用铁制或铝制容器盛装
C.盛装容器的标签上应标注氧化剂和腐蚀品
D.使用时向其中直接加水可制得稀硫酸
科目:高中化学 来源:2016-2017学年广东省肇庆市高二上学期期末化学试卷(解析版) 题型:实验题
已知草酸晶体(H2C2O4·xH2O)可溶于水,并可与酸性高锰酸钾溶液完全反应:
2KMnO4+5H2C2O4+3H2SO4==K2SO4+2MnSO4+8H2O+10CO 2↑
2↑
现用氧化还原滴定法测定草酸晶体的结晶水分子数X,步骤如下:
①用分析天平称取草酸晶体1.260g,将其配制成100.00mL待测草酸溶液;
②用移液管移取25.00mL待测草酸溶液于锥形瓶中,并加入适量硫酸酸化
③用浓度为0.1000 mol·L-1的KMnO4标准溶液进行滴定,三次结果如下:
第一次滴定 | 第二次滴定 | 第三次滴定 | |
待测溶液体积(mL) | 25.00 | 25.00 | 25.00 |
标准溶液体积(mL) | 9.99 | 10.01 | 10.00 |
已知H2C2O4的相对分子质量 为90,请回答下列问题:
为90,请回答下列问题:
(1)滴定时,KMnO4标准溶液应该装在 (填“酸式”或“碱式”)滴定管中。
(2)在整个实验过程中,不需要的仪器或用品是 (填 序号)。
序号)。
①100mL容量瓶 ②烧杯 ③滴定管夹 ④漏斗 ⑤玻璃棒 ⑥托盘天平
(3)到达滴定终点的标志是 。
(4)根据上述数据计算x= 。
(5)误差分析(填:偏高、偏低、无影响):
①若滴定开始时仰视滴定管刻度,滴定结束时俯视滴定管刻度,则x值 ;
②若滴定管水洗后直接加入KMnO4标准溶液,则X值 。
查看答案和解析>>
科目:高中化学 来源:2017届吉林长春外国语学校高三上期末化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数值,下列说法正确的是
A.1 mol Cl2分别与足量的铁或氢氧化钠溶液反应,转移电子数均为2NA
B.将NA个NH3分子溶于1 L水中得到1 mol·L-1的氨水
C. 标准状况下,22.4 L氮
标准状况下,22.4 L氮 气与22.4 L苯所含分子数均为 NA
气与22.4 L苯所含分子数均为 NA
D.常温常压下,32gO2、O3的混合物含有2Na个氧原子
查看答案和解析>>
科目:高中化学 来源:2017届北京市丰台区高三上学期期末化学试卷(解析版) 题型:实验题
石油裂解气用途广泛,可用于合成各种橡胶和医药中间体。利用石油裂解气合成CR橡胶和医药中间体K的线路如下:
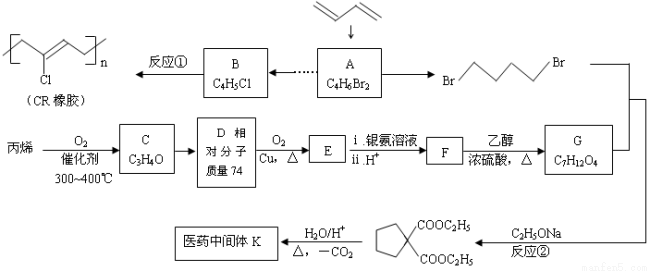
已知: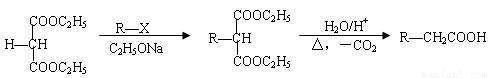
(1)A的顺式异构体的结构简式为_________。
(2)用系统命名法给B命名,其名称是_________。
(3)C含有的官能团名称是_________。
(4)K的结构简式为_________。
(5)依次写出①、②的反应类型_________、_________。
(6)写出下列反应的化学方程式:
D→E:____________________;F→G:___________________。
(7)F还能与其他醇类发生反应,写出F与乙二醇发生聚合反应的化学方程式_________________。
(8)写出同时满足下列条件的医药中间体K的同分异构体的结构简式_____________。
a.与E互为同系物b.核磁共振氢谱有3种峰
(9)已知双键上的氢原子很难发生取代反应。以A为起始原料,选用必要的无机试剂合成B,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。
查看答案和解析>>
科目:高中化学 来源:2017届北京市丰台区高三上学期期末化学试卷(解析版) 题型:选择题
工业上可以利用水煤气(H2、CO)合成二甲醚(CH3OCH3),同时生成CO2。
2 H2(g)+CO(g) = CH3OH(g) ΔH=-91.8 kJ/mol
2CH3OH(g) = CH3OCH3 (g) + H2O(g) ΔH=-23.5 kJ/mol
CO(g) + H2O(g) = CO2(g) +H2(g) ΔH=-41.3 kJ/mol
下列说法不正确的是
A.二甲醚与乙醇互为同分异构体
B.CH3OCH3中只含有极性共价键
C.CH3OH和乙醇均可发生消去反应
D.水煤气合成二甲醚的热化学方程式: 3H2(g)+ 3CO(g) = CH3OCH3 (g) + CO2(g)ΔH=-248.4kJ/mol
查看答案和解析>>
科目:高中化学 来源:2017届北京市昌平区高三上学期期末化学试卷(解析版) 题型:实验题
氯化铁和高铁酸钾都是常见的水处理剂,下图为制备粗高铁酸钾的工业流程。
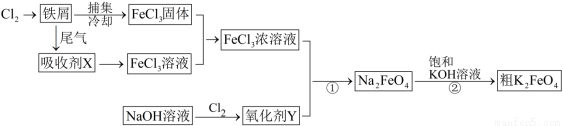
请回答下列问题:
(1)氯化铁做净水剂的原因是(结合化学用语表达) 。
(2)吸收剂X的化学式为 ,氧化剂Y的化学式为 。
(3)碱性条件下反应①的离子方程式为 。
(4)过程②将混合溶液搅拌半小时,静置,抽滤获得粗产品。该反应的化学方程式为2KOH+NaFeO4=K2FeO4+2NaOH,请根据反应原理分析反应能发生的原因 。
(5)K2FeO4在水溶液中易发生反应:4FeO42-+10H2O=4Fe(OH)3+8OH-+3O2↑。在提纯K2FeO4时采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用 (填序号)。
A.H2O B.稀KOH溶液 C.NH4Cl溶液 D.Fe(NO3)3溶液
除了这种洗涤剂外,一般工业生产还要加入异丙醇作为洗涤剂,你认为选择异丙醇的原因是 。
(6)高铁电池是正在研制中的充电电池,具有电压稳定、放电时间长等优点。以高铁酸钾、二氧化硫和三氧化硫为原料,硫酸钾为电解质,用惰性电极设计成能在高温下使用的电池,写出该电池的正极反应式 。
查看答案和解析>>
科目:高中化学 来源:2017届北京市昌平区高三上学期期末化学试卷(解析版) 题型:选择题
纳米Fe3O4晶体材料可以作为核磁共振造影增强剂,用于疾病的诊断和治疗。其制备过程如图所示、下列叙述不合理的是
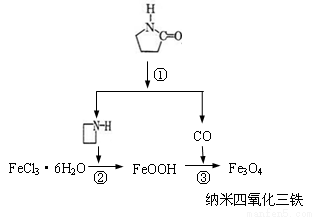
A.在反应②中,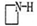 的作用可能是促进氯化铁水解
的作用可能是促进氯化铁水解
B.反应③的化学方程式是:6FeOOH + CO ==2Fe3O4+3H2O+CO2
C.直接加热FeCl3溶液也可以得到四氧化三铁
D.纳米四氧化三铁形成的分散剂,有可能产生丁达尔现象
查看答案和解析>>
科目:高中化学 来源:2016-2017学年吉林省长春市五县高二上期末化学试卷(解析版) 题型:选择题
常温下,向10mL 0.1mol·L-1HR溶液中逐滴滴入0.1mol·L-1的氨水,所得溶液pH及导电能力与加入氨水体积的关系如图。下列说法不正确的是( )
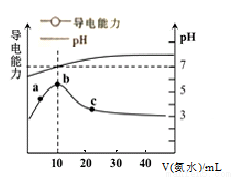
A.常温下,电离平衡常数Ka(HR)≈Kb(NH3·H2O)
B.b点溶液pH=7,此时HR溶液与氨水恰好完全反应
C.c点溶液中存在c(NH4+)>c(R-)>c(OH-)>c(H+)
D.a、b、c三点中,c点NH3·H2O的电离程度最大
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江、吉林省两省六校高一上期中化学试卷(解析版) 题型:选择题
今年8月天津港发生爆炸,其爆炸品中含“TNT”,则在“TNT”包装袋上的标签上应印有的警示标记是 ( )
A.  B.
B. 
C.  D.
D. 
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com