
下列反应的离子方程式中正确的是( )
A.钠与水反应:2Na+2H2O = 2Na+ +2OH-+H2↑
B.氢氧化钡溶液和硫酸铵溶液反应:Ba2++ SO42- = BaSO4↓
C.硫化钠溶于水呈碱性:S2- + 2H2O  H2S + 2OH-
H2S + 2OH-
D.向溴化亚铁溶液中通入少量氯气:Cl2+2Br-=2Cl-+Br2
科目:高中化学 来源:2015-2016学年江西省高一上学期期中考试化学试卷(解析版) 题型:选择题
下列关于纯净物、混合物、电解质、非电解质的正确组合为
A. 纯 盐酸 水煤气 硫酸 干冰 B. 蒸馏水 蔗糖溶液 氧化铝 二氧化硫
盐酸 水煤气 硫酸 干冰 B. 蒸馏水 蔗糖溶液 氧化铝 二氧化硫
C. 胆矾 氢硫酸 铁 碳酸钙 D. 液氧 波尔多液 氨气 蔗糖
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省盐城市高二上学期期中考试化学试卷(解析版) 题型:选择题
某些装修材料会缓慢释放出某种化学物质,可引起过敏性皮炎、免疫功能异常,这种化学物质 可能是
可能是
A.Rn B.SO2 C.HCHO D.CO
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省枣阳市高一上学期期中考试化学试卷(解析版) 题型:选择题
在pH=1的无色溶液中,下列各离子组因发生氧化还原反应而不能共存的是
A.NH4+ K+ Na+ CO32- NO3-
B.K+ Na+ Fe2+ SO42- NO3-
C.NH4+ K+ Na+ HCO3- [Al(OH)4]-
D.NH4+ K+ Na+ NO3- I-
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高二上12月月考化学试卷(解析版) 题型:选择题
对于xA(g)+yB(g)  zC(g)+wD(g)的平衡体系,当升高温度时,体系的平均相对分子质量从26变为29,则下列说法中正确的是
zC(g)+wD(g)的平衡体系,当升高温度时,体系的平均相对分子质量从26变为29,则下列说法中正确的是
A.x+y>z+w, 正反应是放热反应 B.x+y>z+w,正反应是吸热反应
C.x+y<z+w,逆反应是放热反应 D.x+y<z+w,正反应是吸热反应
查看答案和解析>>
科目:高中化学 来源:2016届黑龙江省高三上学期第二次检测化学试卷(解析版) 题型:填空题
Cl2是重要的化工原料。
(1)写出用Cl2制备漂白液的离子方程式______________________。

(2)图1所示的催化剂循环可实验用O2将HCl转化为Cl2,其中反应①为2HCl(g)+CuO(s) H2O(g)+CuCl2(s) ΔH1,反应②消耗1mol O2的反应热为△H2,则总反应生成1mol Cl2(g)的焓变为 (用ΔH1和ΔH2表示)。
H2O(g)+CuCl2(s) ΔH1,反应②消耗1mol O2的反应热为△H2,则总反应生成1mol Cl2(g)的焓变为 (用ΔH1和ΔH2表示)。
(3)实验室模拟用O2将HCl转化为Cl2的总反应
①实验测得在一定压强下,总反应的HCl平衡转化率随温度变化的ɑHCl—T曲线如图2所示,则总反应的△H_________0 ,(填“>”、“﹦”或“<”);A、B两点的平衡常数K(A)与K(B)中较大的是 ,简要说明理由: 。
②在上述实验中若压缩体积使压强增大,在图2中画出相应ɑHCl—T曲线的示意图。
③为提高HCl的平衡转化率下列措施中可行的是 。
A.增大n(HCl) B.增大n(O2) C.使用更好的催化剂 D.移去H2O
查看答案和解析>>
科目:高中化学 来源:2016届辽宁省高三上学期期中测试化学试卷(解析版) 题型:选择题
一定温度下,在一个容积为1 L的密闭容器中,充入1 mol H2(g)和1 mol I2(g),发生反应H2(g)+I2(g) 2HI(g),经充分反应达到平衡后,生成的HI(g)占气体体积的50%,在该温度下,在另一个容积为2L的密闭容器中充入1 mol HI(g)发生反应HI(g)
2HI(g),经充分反应达到平衡后,生成的HI(g)占气体体积的50%,在该温度下,在另一个容积为2L的密闭容器中充入1 mol HI(g)发生反应HI(g)
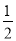 H2(g)+
H2(g)+ 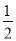 I2(g),则下列判断正确的是
I2(g),则下列判断正确的是
A.后一反应的平衡常数为1
B.后一反应的平衡常数为0.5
C.后一反应达到平衡时,H2的平衡浓度为0.25 mol·L-1
D.后一反应达到平衡时,HI(g)的平衡浓度为0.5 mol·L-1
查看答案和解析>>
科目:高中化学 来源:2015-2016学年贵州遵义航天中学高二上第三次月考化学卷(解析版) 题型:?????
对于可逆反应2AB3(g) 2A(g) + 3B2(g) △H>0,下列图像不正确的是( )
2A(g) + 3B2(g) △H>0,下列图像不正确的是( )
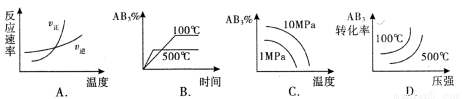
查看答案和解析>>
科目:高中化学 来源:2016届江苏省高三上期中测试化学试卷(解析版) 题型:选择题
人工光合系统装置(如图)可实现以CO2和H2O合成CH4。下列说法不正确的是

A.该装置为原电池,且铜为正极
B.电池工作时,H+向Cu电极移动
C.GaN电极表面的电极反应式为:2H2O-4e-=O2+4H+
D.反应CO2+2H2O CH4+2O2中每消耗1molCO2转移4mole-
CH4+2O2中每消耗1molCO2转移4mole-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com