
某温度下,反应SO2(g)+ O2(g)⇌SO3(g)的平衡常数K1=50,在同一温度下,反应2SO3(g)⇌2SO2(g)+O2(g)的平衡常数K2的值为( )
O2(g)⇌SO3(g)的平衡常数K1=50,在同一温度下,反应2SO3(g)⇌2SO2(g)+O2(g)的平衡常数K2的值为( )
|
| A. | 2500 | B. | 100 | C. | 4×10﹣4 | D. | 2×10﹣2 |
考点:
化学平衡的计算;化学平衡常数的含义.
专题:
化学平衡专题.
分析:
平衡常数指可逆反应达到平衡时各生成物浓度的化学计量数次幂的乘积与各反应物浓度的化学计量数次幂的乘积相比所得的比值.由此可知:相同温度下,①对同一可逆反应逆反应平衡常数与正反应平衡常数的关系是互为倒数.②化学计量数变为原来的n倍,平衡常数变为原来的n次方.
解答:
解:某温度下,SO2(g)+ O2(g)
O2(g) SO3 (g) 的平衡常数K1=50,
SO3 (g) 的平衡常数K1=50,
所以相同温度下2SO2(g)+O2(g) 2SO3 (g) 的平衡常数k=(K1)2=502=2500,
2SO3 (g) 的平衡常数k=(K1)2=502=2500,
在同一温度下,反应2SO3(g) 2SO2(g)+O2(g)的平衡常数K2=
2SO2(g)+O2(g)的平衡常数K2= =
= =4×10﹣4.
=4×10﹣4.
故选:C
点评:
考查平衡常数及计算,难度中等,关键在于利用数学方法推出:相同温度下,①对同一可逆反应逆反应平衡常数与正反应平衡常数的关系是互为倒数.②化学计量数变为原来的n倍,平衡常数变为原来的n次方.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
在某100 mL混合酸中,HNO3的物质的量浓度为0.4 mol·L-1,H2SO4的物质的量浓度为0.2 mol·L-1,向其中加入2.56 g铜粉微热,待充分反应后,溶液中Cu2+的物质的量浓度约为( )
A.0.15 mol·L-1 B.0.3 mol·L-1 C.0.25 mol·L-1 D.无法计算
查看答案和解析>>
科目:高中化学 来源: 题型:
在200 mL某硫酸盐溶液中,含有1.5NA个硫酸根离子(NA表示阿伏加德罗常数的值),同时含有NA个金属离子。则该硫酸盐的物质的量浓度为 ( )
A.1 mol·L-1 B.2.5 mol·L-1
C.5 mol·L-1 D.2 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
医学上常用酸性高锰酸钾溶液和草酸溶液的反应来测定血钙的含量。回答下列问题:

 H++
H++ 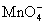 + H2C2O4==== CO2↑+ Mn2++
+ H2C2O4==== CO2↑+ Mn2++
(1)配平以上离子方程式,并在 中填上所需的微粒。
(2)该反应中的还原剂是 。
(3)反应转移了0.4 mol电子,则消耗KMnO4的物质的量为 mol。
(4)测定血钙的含量的方法:取2 mL血液用蒸馏水稀释后,向其中加入足量(NH4)2C2O4溶液,反应生成CaC2O4沉淀,将沉淀用稀硫酸溶解得到H2C2O4后,再用KMnO4溶液滴定。
①稀硫酸溶解CaC2O4沉淀的化学方程式是 。
②溶解沉淀时 (“能”或“不能”)用稀盐酸,原因是 。
③若消耗了1.0×10-4mol·L-1的KMnO4溶液20.00 mL,则100 mL该血液中含钙
g。
查看答案和解析>>
科目:高中化学 来源: 题型:
以硫酸铜溶液作电解液,对含有杂质Fe、Zn、Ag的粗铜进行电解精炼.下列叙述正确的是( )
①粗铜与直流电源负极相连
②阴极发生的反应为Cu2++2e﹣═Cu
③电路中每通过3.01×1023个电子,得到的精铜质量为16g
④杂质Ag以Ag2SO4的形式沉入电解槽形成阳极泥.
|
| A. | ①③ | B. | ②③④ | C. | ③④ | D. | ②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
高温下,某反应达平衡,平衡常数K=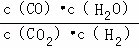 .恒容时,温度升高,H2浓度减小.下列说法正确的是( )
.恒容时,温度升高,H2浓度减小.下列说法正确的是( )
|
| A. | 该反应的焓变为正值 |
|
| B. | 恒温恒容下,增大压强,H2浓度一定减小 |
|
| C. | 升高温度,逆反应速率减小,平衡常数K增大 |
|
| D. | 该反应化学方程式为CO+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中错误的是( )
|
| A. | 从1L 1mol•L﹣1的NaCl溶液中取出10mL,其浓度仍是1mol•L﹣1 |
|
| B. | 制成0.5L 10mol•L﹣1的盐酸,需标准状况下氯化氢气体112L |
|
| C. | 0.5L 2mol•L﹣1 BaCl2溶液中,Ba2+和Cl﹣总数为3×6.02×1023 |
|
| D. | 10g 98%硫酸(密度为1.84g•cm﹣3)与10mL 18.4 mol•L﹣1硫酸的浓度是不同的 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中正确的是
A.液溴易挥发,在存放液溴的试剂瓶中应加水封
B.能使润湿的淀粉KI试纸变成蓝色的物质一定是Cl2
C.某溶液加入CCl4,CC14层显紫色,证明原溶液中存在I−
D.某溶被加入BaCl2溶液,产生不溶于稀硝酸的白色沉淀,该溶液一定含有Ag+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com