
| A、CH2Cl2有两种同分异构体 |
| B、乙酸和油脂都能与氢氧化钠溶液反应 |
| C、可以用水来鉴别苯和CCl4 |
| D、乙烯和甲烷可用酸性高锰酸钾溶液鉴别 |


科目:高中化学 来源: 题型:
| A、中和滴定时,锥形瓶不用润洗 |
| B、用试纸检验气体性质时,需先将试纸湿润,再检验 |
| C、FeBr2溶液中通入少量Cl2,再加入CCl4,CCl4层不变色 |
| D、向盐酸酸化的Ba(NO3)2溶液中通入SO2,不会产生沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用10 mL 量筒量取5.2 mL盐酸 |
| B、向小试管中加入100mL稀盐酸 |
| C、用托盘天平称取25.12gNaCl固体 |
| D、用100 mL容量瓶配制50mL0.1 mol/L的盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、石英只能用于生产光导纤维 |
| B、从海水提取物质都必须通过化学反应才能实现 |
| C、“地沟油”禁止食用,但可以用来制肥皂 |
| D、镀锡的钢铁器件既能增加美观.又可在镀层局部破损后防止器件的损耗 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
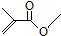 分子式:
分子式: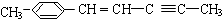 分子中最多有
分子中最多有查看答案和解析>>
科目:高中化学 来源: 题型:
| A、工业上在高温下用CO还原含Fe2O3的铁矿石炼铁 |
| B、铁在纯氧中燃烧或高温下和水蒸气反应均能得到Fe2O3 |
| C、工业上可用磁性氧化铁制成电讯器材 |
| D、明矾和硫酸铁溶液均可用作净水剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、KOH(aq)+
| ||||
| B、2KOH(s)+H2SO4(aq)=K2SO4(aq)+2H2O (l);△H=-114.6kJ/mol | ||||
| C、2KOH(aq)+H2SO4=K2SO4(aq)+H2O (l);△H=+114.6kJ/mol | ||||
D、KOH (aq)+
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com