
| A.KCl | B.Na2S? |
| C.Na2O | D.K2S |
科目:高中化学 来源:不详 题型:单选题
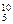 B、
B、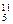 B,硼元素的近似相对原子质量为10.80,则对硼元素中
B,硼元素的近似相对原子质量为10.80,则对硼元素中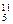 B 质量分数的判断正确的是
B 质量分数的判断正确的是查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| 实验方案 | 实验现象 | ||||
| 1.用砂纸擦后的镁带与沸水反应,再向反应后溶液中滴加酚酞溶液 2.向新制的H2S饱和溶液中滴加新制的氯水 3.钠与滴有酚酞的冷水反应 4.镁带与2 mol·L-1盐酸反应 5.铝条与2 mol·L-1盐酸反应 6.向AlCl3溶液中滴加NaOH溶液至过量 |
F.生成淡黄色沉淀 |
| 实验方案* | 实验现象* | 有关化学方程式 |
| | | |
| | | |
| | | |
| | | |
| | | |
| | | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.元素R能与氧组成RO2化合物 |
| B.化合物RO2在反应中既可作氧化剂也可作还原剂,其化合物不稳定 |
| C.化合物H2R不能燃烧,也不易分解 |
| D.元素R是一种两性元素 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.碱金属 | B.第ⅡA族元素 |
| C.过渡元素 | D.金属与非金属分界线附近的元素 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com