
【题目】已知Ksp(CaCO3)=2.8×10-9及表中有关信息:
弱酸 | CH3COOH | H2CO3 |
电离平衡常数(常温) | Ka=1.8×10-5 | Ka1=4.3×10-7; Ka2=5.6×10-11 |
下列判断正确的是
A. 向Na2CO3溶液中滴入酚酞,溶液变红,主要原因是CO32-+2H2O![]() H2CO3+2OH-
H2CO3+2OH-
B. 常温时,CH3COOH与CH3COONa混合溶液的pH=6,则 =18
=18
C. NaHCO3溶液中:c(OH-)-c(H+)=c(H2CO3)-c(CO32-)
D. 2×10-4 mol/L的Na2CO3溶液与CaCl2溶液等体积混合出现沉淀,则CaCl2溶液的浓度一定是5.6×10-5 mol/L
【答案】C
【解析】A.弱酸根离子水解是分步进行,向Na2CO3溶液中滴入酚酞,溶液变红,主要原因是CO32-+H2O![]() HCO3-+OH-,故A错误;B. 常温时,CH3COOH与CH3COONa混合溶液的pH=6,醋酸的电离平衡表示式为K=c(CH3COO-)c(H+)/c(CH3COOH),1.8×10-5/10-6= c(CH3COO-)/c(CH3COOH),
HCO3-+OH-,故A错误;B. 常温时,CH3COOH与CH3COONa混合溶液的pH=6,醋酸的电离平衡表示式为K=c(CH3COO-)c(H+)/c(CH3COOH),1.8×10-5/10-6= c(CH3COO-)/c(CH3COOH),  =1/18,B错误;C. NaHCO3溶液中的物料守恒为:c(Na+)= c(H2CO3)+c(HCO3-) +c(CO32-),电荷守恒为:c(H+)+c(Na+)=c(OH-)+c(HCO3-) +2c(CO32-),两式联列得:c(OH-) +c(CO32-)=c(H2CO3)+c(H+),故C正确;D.已知Ksp(CaCO3)=2.8×10-9= c(CO32-) c(Ca2+),2×10-4 mol/L的Na2CO3溶液与CaCl2溶液等体积混合,c(CO32-)= 2×10-4 mol/L×/2V=1×10-4 mol/L,代入公式,得c(Ca2+)=2.8×10-5 mol/L,则原CaCl2溶液中c(Ca2+)≥2.8×10-5 mol/L×2==5.6×10-5 mol/L,故D错误。
=1/18,B错误;C. NaHCO3溶液中的物料守恒为:c(Na+)= c(H2CO3)+c(HCO3-) +c(CO32-),电荷守恒为:c(H+)+c(Na+)=c(OH-)+c(HCO3-) +2c(CO32-),两式联列得:c(OH-) +c(CO32-)=c(H2CO3)+c(H+),故C正确;D.已知Ksp(CaCO3)=2.8×10-9= c(CO32-) c(Ca2+),2×10-4 mol/L的Na2CO3溶液与CaCl2溶液等体积混合,c(CO32-)= 2×10-4 mol/L×/2V=1×10-4 mol/L,代入公式,得c(Ca2+)=2.8×10-5 mol/L,则原CaCl2溶液中c(Ca2+)≥2.8×10-5 mol/L×2==5.6×10-5 mol/L,故D错误。


 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.Na2CO3比NaHCO3溶解度大
B.Na2CO3比NaHCO3稳定
C.Na2CO3和NaHCO3都能跟石灰水反应得到白色沉淀
D.物质的量相等的Na2CO3和NaHCO3分别与足量盐酸反应得CO2物质的量之比为2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,用相同浓度的NaOH溶液,分别滴定浓度均为0.1mol·L-1的三种酸(HA、HB和HD)溶液,滴定的曲线如图所示,下列判断错误的是( )
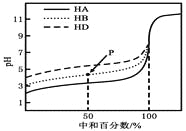
A. 三种酸的电离常数关系:KHA>KHB>KHD
B. 滴定至P点时,溶液中:c(B-)>c(Na+)>c(HB)>c(H+)>c(OH-)
C. pH=7时,三种溶液中:c(A-)=c(B-)=c(D-)
D. 当中和百分数达100%时,将三种溶液混合后:c(HA)+c(HB)+c(HD)=c(OH-)-c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上,向500℃~600℃的铁屑中通入氯气生产无水氯化铁(已知炽热铁屑与氯化氢生成氯化亚铁).现用如图所示的装置模拟上述过程进行试验.
回答下列问题:
(1)盛装浓盐酸的仪器名称为 , 进行实验时,应先点燃(选填A或C)处酒精灯.
(2)制取无水氯化铁的实验中,A中反应的离子方程式为 , 装置B中加入的试剂是 .
(3)制取的无水氯化铁中混有少量氯化亚铁,其原因是(化学方程式表示).为除去氯气中混有的少量HCl,可以在装置A、B间加入装有的洗气瓶.
(4)工业上常用石灰乳吸收制氯气的尾气制得漂白粉,漂白粉的有效成分是(填化学式).长期露置于空气中的漂白粉,加稀盐酸后产生的气体是(填数字代号).
①O2 ②Cl2 ③CO2 ④HClO.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列溶液中Cl-的物质的量浓度最大的是
A. 0.5L 0.1mol/L的NaCl溶液 B. 100mL 0.2mol/L的MgCl2溶液
C. 1L 0.2mol/L的AlCl3溶液 D. 1L 0.3 mol/L盐酸溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于下列各实验装置的叙述中,正确的是( ) 
A.装置①制备乙酸乙酯
B.装置②中X若为CCl4 , 可用于吸收NH3或HCl,并防止倒吸
C.装置③可用于干燥、收集Cl2 , 并吸收多余的Cl2
D.装置④配制一定物质的量浓度的溶液时转移液体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F是中学化学中常见的六种短周期元素,有关位置及信息如下:A的最高价氧化物对应的水化物与其氢化物反应生成离子化合物;C单质一般保存在煤油中;F的最高价氧化物对应的水化物既能与强酸反应又能与强碱反应,G单质是日常生活中用量最大的金属,易被腐蚀或损坏。请回答下列问题:
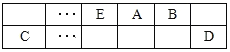
(1)A元素的氢化物水溶液能使酚酞变红的原因用电离方程式解释为_____________。
(2)同温同压下,将a L A氢化物的气体和b L D的氢化物气体先后通入一盛水的烧杯中,若所得溶液的pH=7,则a_________b(填“>"或“<”或“=”)。
(3)常温下,相同浓度F、G简单离子的溶液中滴加NaOH溶液,F、G两元素先后沉淀,F(OH)n完全沉淀的pH是4.7,G(OH)n完全沉淀的pH是2.8,则在相同条件下,溶解度较大的是:___(填化学式)。
(4)A与B可组成质量比为7:16的三原子分子,该分子释放在空气中其化学作用可能引发的后果有:_______________。
①酸雨 ②温室效应 ③光化学烟雾 ④臭氧层破坏
(5)A和C组成的一种离子化合物,能与水反应生成两种碱,该反应的化学方程式是______。
(6)用电子式表示B,C形成化合物C2B2的过程_______________。
(7)已知一定量的E单质能在B2(g)中燃烧,其可能的产物及能量关系如下图所示:请写出一定条件下EB2(g) 与E(s)反应生成EB(g)的热化学方程式__________________。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com