
Si+4HF══SiF4↑+2H2↑
Si+2NaOH+H2O══Na2SiO3+2H2↑
又知硅及其化合物间存在如下图所示的关系:
其中A是制造芯片和光电池的主要原料;B是含硅化合物中的一种气体;某些C可作干燥剂或催化剂的载体;D是一种黏合剂,能将磨砂玻璃黏合在一起;E是一种比H2CO3酸性还弱的酸。
试回答下列问题:
(1)写出A、C、E的化学式:A________、C________、E________。
(2)①~⑦反应中,属于氧化还原反应的是________,属于置换反应的是________,属于离子反应的是________。
解析:本题突破口较多,B是含硫的一种气体,说明B为SiF4,C为硅胶SiO2,D为Na2SiO3,E为H2SiO3
①~⑦反应分别是:
![]() 是氧化还原反应,也是置换反应,不是离子反应(氢氟酸是弱酸,在溶液中HF的电离微弱,不能拆为离子形式)。
是氧化还原反应,也是置换反应,不是离子反应(氢氟酸是弱酸,在溶液中HF的电离微弱,不能拆为离子形式)。
②SiO2+4HF══SiF4↑+2H2O。不是氧化还原反应,不是置换反应,也不是离子反应。
![]() 是氧化还原反应,不是置换反应,也不是离子反应。
是氧化还原反应,不是置换反应,也不是离子反应。
![]() 是氧化还原反应,是置换反应(有单质和化合物参加,也有单质和化合物生成),也是离子反应:
是氧化还原反应,是置换反应(有单质和化合物参加,也有单质和化合物生成),也是离子反应:
⑤2NaOH+SiO2══Na2SiO3+H2O 2OH-+SiO2══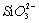 +H2O。不是氧化还原反应,也不是置换反应,是离子反应:
+H2O。不是氧化还原反应,也不是置换反应,是离子反应:
⑥Na2SiO3+2HCl══2NaCl+H2SiO3↓ 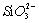 +2H+══H2SiO3↓。不是氧化还原反应,也不是置换反应,是离子反应:
+2H+══H2SiO3↓。不是氧化还原反应,也不是置换反应,是离子反应:
⑦H2SiO3![]() H2O+SiO2。不是氧化还原反应,不是置换反应,也不是离子反应。
H2O+SiO2。不是氧化还原反应,不是置换反应,也不是离子反应。
答案:(1)Si SiO2 H2SiO3(2)①③④ ①④ ④⑤⑥


科目:高中化学 来源: 题型:阅读理解

| ||
| ||
查看答案和解析>>
科目:高中化学 来源:学习高手必修一化学人教版 人教版 题型:022
已知Si能与HF(aq)和NaOH(aq)反应:
Si+4HF![]() SiF4↑+2H2↑
SiF4↑+2H2↑
Si+2NaOH+H2O![]() Na2SiO3+2H2↑
Na2SiO3+2H2↑
又知硅及其化合物间存在如下图所示的关系:
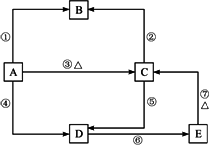
其中A是制造芯片和光电池的主要原料;B是含硅化合物中的一种气体;某些C可作干燥剂或催化剂的载体;D是一种黏合剂,能将磨砂玻璃黏合在一起;E是一种比H2CO3酸性还弱的酸.
试回答下列问题:
(1)写出A、C、E的化学式:A________、C________、E________.
(2)①~⑦反应中,属于氧化还原反应的是________,属于置换反应的是________,属于离子反应的是________.
查看答案和解析>>
科目:高中化学 来源: 题型:
已知Si能与HF(aq)和NaOH(aq)反应:Si+4HF══SiF4↑+2H2↑ Si+2NaOH+H2O══Na2SiO3+2H2↑,又知硅及其化合物间存在如下图所示的关系:
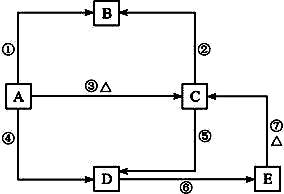
其中A是制造芯片和光电池的主要原料;B是含硅化合物中的一种气体;某些C可作干燥剂或催化剂的载体;D是一种黏合剂,能将磨砂玻璃黏合在一起;E是一种比H2CO3酸性还弱的酸。
试回答下列问题:
(1)写出A、C、E的化学式:A________、C________、E________。
(2)①~⑦反应中,属于氧化还原反应的是________,属于置换反应的是________,属于离子反应的是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com