
Na2FeO4ŹĒŅ»ÖÖøߊ§¶ą¹¦ÄÜĖ®“¦Ąķ¼Į£¬Ó¦ÓĆĒ°¾°Ź®·Öæ“ŗĆ”£Ņ»ÖÖÖʱøNa2FeO4µÄ·½·ØæÉÓĆ»Æѧ·½³ĢŹ½±ķŹ¾ČēĻĀ£ŗ2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2”ü£¬¶Ō“Ė·“Ó¦ĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ
A£®Na2O2Ö»×÷Ńõ»Æ¼Į
B£®Na2FeO4¼ČŹĒŃõ»Æ²śĪļÓÖŹĒ»¹Ō²śĪļ
C£®O2ŹĒ»¹Ō²śĪļ
D£®2 mol FeSO4·¢Éś·“Ó¦Ź±£¬·“Ó¦ÖŠ¹²ÓŠ8 molµē×Ó×ŖŅĘ
B
”¾½āĪö”æ
ŹŌĢā·ÖĪö£ŗFeŌŖĖŲÓÉ+2¼ŪÉżøßÖĮ+6¼Ū£¬ĖłŅŌFeSO4ĪŖ»¹Ō¼Į£¬Na2O2ÖŠ²æ·ÖŃõŌŖĖŲ»ÆŗĻ¼Ū½µµĶĪŖ-2¼Ū£¬²æ·ÖÉżøßÖĮ0£¬ĖłŅŌNa2O2¼ČŹĒŃõ»Æ¼ĮŅ²ŹĒ»¹Ō¼Į£¬O2ŹĒŃõ»Æ²śĪļ£¬¹ŹAĻī”¢CĻī“ķĪó£»Na2FeO4¼ČŹĒŃõ»Æ²śĪļÓÖŹĒ»¹Ō²śĪļ£¬BĻīÕżČ·£»øł¾ŻFeŌŖĖŲŗĶOŌŖĖŲµÄ»ÆŗĻ¼ŪµÄ±ä»Æ£¬æÉÖŖ2 mol FeSO4·¢Éś·“Ó¦Ź±£¬·“Ó¦ÖŠ¹²ÓŠ£Ø2”Į4mol+2mol£©=10molµē×Ó×ŖŅĘ£¬¹ŹDĻī“ķĪó”£
æ¼µć£ŗ±¾Ģāæ¼²éŃõ»Æ»¹Ō·“Ó¦¼°ĘäÓ¦ÓĆ”£


 ĆūŠ£æĪĢĆĻµĮŠ“š°ø
ĆūŠ£æĪĢĆĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016½ģŗ£ÄĻŹ”ČżŃĒŹŠøßŅ»ÉĻŃ§ĘŚĘŚÖŠæ¼ŹŌ»ÆѧŹŌ¾ķ£ØA£©£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
¾ĶÓŠ¹ŲĪļÖŹµÄ·ÖĄė»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©ĻÖÓŠŅ»ĘæAŗĶBµÄ»ģŗĻŅŗ£¬ŅŃÖŖĖüĆĒµÄŠŌÖŹČēĻĀ±ķ”£
ĪļÖŹ | ČŪµć/”ę | ·Šµć/”ę | ĆܶČ/g”¤cm-3 | ČܽāŠŌ |
A | £11£®5 | 198 | 1£®11 | A”¢B»„ČÜ£¬ĒŅ¾łŅ×ČÜÓŚĖ® |
B | 17£®9 | 290 | 1£®26 |
¾Ż“Ė·ÖĪö£¬½«AŗĶBĻą»„·ÖĄėµÄ³£ÓĆ·½·ØŹĒ£ŗ ”£
£Ø2£©ŌŚ·ÖŅŗĀ©¶·ÖŠÓĆŅ»ÖÖÓŠ»śČܼĮĢįČ”Ė®ČÜŅŗĄļµÄijĪļÖŹŹ±£¬¾²ÖĆ·Ö²ćŗó£¬Čē¹ū²»ÖŖµĄÄÄŅ»²ćŅŗĢåŹĒ”°Ė®²ć”±£¬ŹŌÉč¼ĘŅ»ÖÖ¼ņ±ćµÄÅŠ¶Ļ·½·Ø: ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016½ģÕć½Ź”øßŅ»ĻĀŃ§ĘŚĘŚÖŠæ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠŹĀŹµÓėÅØĮņĖį¾ßÓŠĒæŃõ»ÆŠŌÓŠ¹ŲµÄŹĒ
¢Ł³£ĪĀŹ±ÓĆĢśÖĘČŻĘ÷ŌĖŹäÅØĮņĖį
¢ŚĮņĖį¹¤ŅµÉś²śÖŠ£¬ÓĆÅØĮņĖįĪüŹÕSO3
¢ŪÅØĮņĖįŹ¹ÕįĢĒĢæ»Æ±äŗŚ²¢ÓŠ“óĮæĘųĢå²śÉś
¢ÜÅØĮņĖįÓĆÓŚÉś²śĮ×·Ź
¢ŻÅØĮņĖį²»ÄÜÓĆĄ“øÉŌļHBr
A£®¢Ł¢Ū¢Ü B£®¢Ł¢Ś¢Ū C£®¢Ł¢Ū¢Ż D£®¢Ś¢Ū¢Ü¢Ż
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016½ģÕć½Ź”øßŅ»ÉĻŃ§ĘŚĘŚÖŠæ¼ŹŌĄķæĘ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠĪļÖŹĶ¬Ź±ŗ¬ÓŠĀČĘų·Ö×Ó”¢ĀČĄė×ÓŗĶĀȵÄŗ¬Ńõ»ÆŗĻĪļµÄŹĒ( )
A£®ĀČĖ® B£®ŅŗĀČ C£®ĀČĖį¼Ų D£®“ĪĀČĖįøĘ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016½ģÕć½Ź”øßŅ»ÉĻŃ§ĘŚĘŚÖŠæ¼ŹŌĄķæĘ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
°¢·ü¼ÓµĀĀŽ³£ŹżŌ¼ĪŖ6.02”Į1023 mol£1£¬ĻĀĮŠŠšŹöÖŠÕżČ·µÄŹĒ( )
A£®1.01”Į105 Pa”¢25 ”ꏱ£¬2.24 L Cl2ÖŠŗ¬ÓŠµÄŌ×ÓŹżĪŖ0.2”Į6.02”Į1023
B£®0.1 L 3 mol”¤L£1 NH4NO3ČÜŅŗÖŠŗ¬ÓŠµÄNŌ×ÓŹżÄæĪŖ0.3”Į6.02”Į1023
C£®5.6 gĢś·ŪÓė×ćĮæCuSO4ČÜŅŗ·“Ӧɜ³ÉµÄĶŌ×ÓŹżĪŖ1”Į6.02”Į1023
D£®46 g NO2ŗĶN2O4µÄ»ģŗĻĪļÖŠŗ¬ÓŠµÄŌ×ÓŹżĪŖ3”Į6.02”Į1023
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016½ģÕć½Ź”øßŅ»ÉĻŃ§ĘŚĘŚÖŠæ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ŹµŃéŹŅŠčŅŖ2.0 mol”¤L-1NaOHČÜŅŗ90mL£¬Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©ÅäÖĘ¹ż³ĢÖŠ²»ŠčŅŖŹ¹ÓƵ½µÄ»ÆѧŅĒĘ÷ÓŠ £ØĢī×ÖÄø£©
A.ÉÕ± B. 100mLČŻĮæĘæ C. Ā©¶· D.½ŗĶ·µĪ¹Ü E.²£Į§°ō
£Ø2£©ÓĆĶŠÅĢĢģĘ½³ĘČ”ĒāŃõ»ÆÄĘ£¬ĘäÖŹĮæĪŖ g£»
£Ø3£©ĻĀĮŠÖ÷ŅŖ²Ł×÷²½ÖčµÄÕżČ·Ė³ŠņŹĒ £ØĢīŠņŗÅ£©£»
¢Ł³ĘČ”Ņ»¶ØÖŹĮæµÄĒāŃõ»ÆÄĘ£¬·ÅČėÉÕ±ÖŠ£¬ÓĆŹŹĮæÕōĮóĖ®Čܽā£»
¢Ś¼ÓĖ®ÖĮŅŗĆęĄėČŻĮæĘæ¾±æĢ¶ČĻßĻĀ1”Ŗ2ĄåĆ׏±£¬øÄÓĆ½ŗĶ·µĪ¹ÜµĪ¼ÓÕōĮóĖ®ÖĮ°¼ŅŗĆęÓėæĢ¶ČĻßĻąĒŠ£»
¢Ū“żĄäČ“ÖĮŹŅĪĀŗ󣬽«ČÜŅŗ×ŖŅʵ½100mLČŻĮæĘæÖŠ£»
¢ÜøĒŗĆĘæČū£¬·“ø“ÉĻĻĀµßµ¹£¬Ņ”ŌČ£»
¢ŻÓĆÉŁĮæµÄÕōĮóĖ®Ļ“µÓÉÕ±ÄŚ±ŚŗĶ²£Į§°ō2~3“Ī£¬Ļ“µÓŅŗ×ŖŅʵ½ČŻĮæĘæÖŠ£»
£Ø4£©ŌŚŹµŃéÖŠĘäĖū²Ł×÷¾łÕżČ·£¬ČēŹµŃé¹ż³Ģ֊ȱɣ²½Öč¢Ż£¬»įŹ¹ÅäÖĘ³öµÄNaOHČÜŅŗÅØ¶Č £ØĢī”°Ę«øß”±»ņ”°Ę«µĶ”±»ņ”°²»±ä”±£©£»Čō¶ØČŻŹ±ŃöŹÓæĢ¶ČĻߣ¬ŌņĖłµĆČÜŅŗÅØ¶Č 2.0 mol”¤L-1£ØĢī”°“óÓŚ”±»ņ”°Š”ÓŚ”±»ņ”°µČÓŚ”±£©”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016½ģÕć½Ź”øßŅ»ÉĻŃ§ĘŚĘŚÖŠæ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
Rn+Ąė×ÓÓŠmøöµē×Ó£¬ĖüµÄÖŹĮæŹżĪŖA£¬ŌņŌ×ÓŗĖÄŚµÄÖŠ×ÓŹżĪŖ£Ø £©
A.m +n B.A£m+n C.A£m£n D.A£«m£n
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016½ģÕć½Ź”øßŅ»ÉĻŃ§ĘŚĘŚÖŠæ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠµēĄė·½³ĢŹ½ŹéŠ““ķĪóµÄŹĒ£Ø £©
A£®CaCl2=Ca2++2Cl”Ŗ B£®H2CO3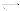 H£«£«HCO3£
H£«£«HCO3£
C£®NaHCO3£½Na£«£«H£«£«CO32£ D£®NaClO=Na++Cl O”Ŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016½ģÕć½Ź”ŗžÖŻŹŠøßŅ»ÉĻŃ§ĘŚĘŚÄ©æ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠ±ä»ÆÖŠ£¬Šč¼ÓŃõ»Æ¼Į²ÅÄÜŹµĻֵďĒ
A£®NaClO ”śNaCl B£®Na2O2 ”ś O2 C£®C ”ś CO2 D£®CaO”śCa(OH)2
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com