
����Ŀ�������仯�������ճ�����������Ӧ�ù㷺���о������仯�����Ӧ�������ش�FeSO47H2O�㷺����ҽҩ��ҵ���������Dzⶨij��Ѫ������Ч�ɷ�ΪFeSO47H2O������Ԫ�غ���������ͼ�������������������գ�

��1�������ܹ����յ���+2�۵���������+2�۵��������ױ���������Ѫ����ά����Cһ����ã�������+2���������ա��ɴ˿���֪��ά����C����____________�����������������ԭ��������
��2����������Ҫ100mL1mol��L-1��ϡ���ᣬʵ��������������Ϊ98%��Ũ���ᣨ�ܶ�Ϊ1.84g��cm-3�������ƣ�������Ͳ��ȡŨ����____________mL��
��3��������������Һ�еμ�KSCN��Һ����Һ��Ϊ��ɫ������Һ�к���____________�������ӷ��ţ���������Һ�л�����Fe2+��Ӧѡ�õ��Լ�Ϊ____________������ĸ��
A��NaCl��ҺB������KMnO4��ҺC��NaOH��Һ
��4���������������H2O2��Ŀ����____________�������ӷ���ʽ��ʾ����
��5����������һϵ�в��������ǣ��ٹ��ˢ�ϴ�Ӣ�____________����ȴ�ݳ������ز�����������Ŀ����____________��
��6������ʵ������ģ���ÿƬ��Ѫ������Ԫ�ص�����Ϊ____________g���ú�a�Ĵ���ʽ��ʾ����
���𰸡���ԭ�� 5.4 Fe3+ B 2Fe2++2H++H2O2===2Fe3++2H2O ���գ�д������������������������Ҳ���ԣ� ȷ������������ȫ�ֽ�������� 0.07a
��������
�ɲ�Ѫ����Ч�ɷֿ�֪���ˣ�����III������Һ����Ҫ�ɷ���FeSO4����Ϊ������ԭ���п�����Fe3+������H2O2�����������Խ�+2����������+3�������������X�ɲ������ɫ����Һ����֪��Fe(OH)3��������ɫ�����֪��Fe2O3��
(1)����Ϣ+2�۵��������ױ���������֪Ϊ���䲻����������Ҫ���뻹ԭ��������ά����C���л�ԭ�ԡ�
(2)��������Ũ�������ΪV����������ǰ����Ũ��������ƺ��ϡ���������һ���࣬����ʽ![]() �����V=5.4ml����Ϊ����Ͳ��ȡ�����Ա���һλС����
�����V=5.4ml����Ϊ����Ͳ��ȡ�����Ա���һλС����
(3)��KSCN��Һ����Һ��Ϊ��ɫ����Fe3+��������Ӧ��Fe2+���л�ԭ�ԣ��ɻ�ԭ����KMnO4��Һʹ֮��ɫ��B��ȷ��Fe2+������NaOH��Һ��Ӧ���ɰ�ɫ��������Fe3+Ҳ������NaOH��Һ��Ӧ�����ɺ��ɫ��������ɫ�����ᱻ�ڸǣ�C����
(4)��H2O2�����������Խ�+2����������+3��������ӦΪ2Fe2++2H++H2O2===2Fe3++2H2O����Ϊ��ʼ�������ᣬ��Һ�����ԣ�������H+��ƽ��
(5) Fe(OH)3ת��ΪFe2O3����Ҫ����ʹ֮�ֽ⡣��ΪFe(OH)3�Ƿ���ȫ�ֽ���ֱ�ӿ���������Ҫ���Ⱥ���أ���������γ���������С��0.1g��������ƽ����С�̶ȣ�������Ϊ��ȫ�ֽ��ˡ�
(6)������Ԫ���غ㣬Fe2O3�е���Ԫ���벹Ѫ���е���Ԫ������һ��������ʽ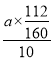 =0.07a g��
=0.07a g��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������仯�������ճ�������������;�㷺������FeSO4�Ʊ���ԭ���۵Ĺ�ҵ�������£�
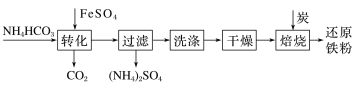
ʵ�����п���FeSO4(�����ۺ�ϡ���ᷴӦ�Ƶ�)��NH4HCO3��Һ������װ��ģ�����������е���ת�������ڡ�
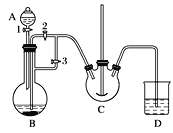
(1)װ��A������������________��װ��B��ʢ�ŵ�ҩƷ��________��
(2)ʵ������У��������ɵ�FeSO4��Һ��NH4HCO3��Һ��ϣ�����������____________________��FeSO4��ҺҪ���������Ƶ�ԭ����_____________________��
(3)������̵���ҪĿ������ȥ����FeCO3�е�����ˮ���ù����л�������FeCO3�ڿ����б�����ΪFeOOH���÷�Ӧ�Ļ�ѧ����ʽΪ_________________________________________��ȡ������FeCO3��Ʒ24.98 g����̿��Ϻ��գ����յõ���ԭ����12.32 g��������Ʒ��FeCO3����������________%(������ȡ����)��
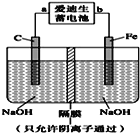
(4)��������(Na2FeO4)��һ�����;�ˮ��.����ͼװ�ÿ�����ȡ�����������ƣ�д�����õ�ⷨ��ȡ��������ʱ�������ĵ缫��Ӧʽ___________________
(5)25 ��ʱ��Ksp[Fe(OH)3]��4.0��10��38 �����¶��£���ʵ����������2.5mol/L 100mL��������Һ��Ϊʹ���ƹ����в����ֻ��ǣ���������Ҫ����10mol/L������______mL(���Լ�����������)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���й��Ŵ��Ĵ���֮һ�����ڻ�ҩ�����ڱ�ըʱ�����Ļ�ѧ��ӦΪ2KNO3+3C+S=A+N2��+3CO2��(����ƽ)
��1���ٳ�S�⣬����Ԫ�صĵ縺�ԴӴ�С����Ϊ__________��
�����������У�A�ľ�������Ϊ_______�������Թ��ۼ��ķ��ӵ�����ԭ�ӹ���ӻ�����Ϊ_____��
����֪CN-��N2��Ϊ�ȵ����壬����HCN������������������Ŀ֮��Ϊ_____��
��2��ԭ������С��36��Ԫ��Q��T�������ڱ��мȴ���ͬһ������λ��ͬһ�壬��ԭ������T��Q��2��T�Ļ�̬ԭ����Χ����(�۵���)�Ų�Ϊ______��Q2+��δ�ɶԵ�������_______��
��3����ij�������ʾ�����ԭ�ӵĶѻ���ʽ��ͼ����ʾ���侧��������ͼ����ʾ��ԭ��֮���λ�ù�ϵ��ƽ��ͼ��ͼ����ʾ�����и�ԭ�ӵ���λ��Ϊ________���õ��ʾ�����ԭ�ӵĶѻ���ʽΪ���ֻ����ѻ���ʽ�е�________��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������(�����е�����������)
���� | ��ѧ��Ӧ����ʽ | |
Na2CO3����(NaHCO3) | _________ | _________ |
NaHCO3��Һ(Na2CO3) | _________ | _________ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��20mlij��̬�������������ϣ�����ȫȼ�պ�IJ���ͨ��Ũ���ᣬ�ٻָ������£��������������50mL�������̬�������ܵ���( )
A. ���� B. ������ C. ��ϩ D. ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijѧϰС��Ϊ��֤Ũ�����ܽ�NO������NO2����ϡ���������NO�������ͼװ�ý���ʵ�飨�г���������ȥ�������������ϣ���NO��NaOH��Һ����Ӧ��NO2��NaOH��Һ�ܷ�Ӧ����Ӧ�Ļ�ѧ����ʽΪ2NO2+2NaOHNaNO3+NaNO2+H2O����
��ѡҩƷ��Ũ���ᡢ3mol��L-1ϡ���ᡢ����ˮ��Ũ���ᡢNaOH��Һ��CO2���塣�ش��������⡣

��1�����Ӻ�װ�ã��μ�Ũ����֮ǰ�IJ��������ǣ�____________������ҩƷ����װ�â��еĵ��ɼк�ͨ��CO2һ��ʱ�䣬�رյ��ɼУ���װ�â��е���ĩ�����뵹�õ���ƿ�ڡ�ͨ��CO2��Ŀ����____________��
��2��������������Ϊ70%Ũ���ᣨ�ܶ�Ϊ1.42g��cm-3������250mL3mol��L-1��ϡ���ᣬ����Ͳ���ձ�����ͷ�ι��⣬��Ҫ�õ��IJ���������____________��____________��
��3��װ�â��з�����Ӧ�Ļ�ѧ����ʽΪ____________��
��4��װ�â��в���������ͨ��ʢ��ˮ��ϴ��ƿʱ������Ӧ�Ļ�ѧ����ʽΪ____________��
��5������ʵ����ƣ�װ�â���ʢ�ŵ��Լ���____________��
��6����ʵ��ʱӦ�����к������ŷŵ������У�װ�â���ʢ�ŵ�ҩƷ��____________��
��7����֤Ũ�����ܽ�NO������NO2����ϡ���������NO��ʵ��������____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ڲ�ͬ�ܼ�����NaOH������ͬ���͵ķ�Ӧ�����ɲ�ͬ�ķ�Ӧ���ijͬѧ��������������ʣ���ͼʵ��װ��(����̨���ƾ�����)��֤ȡ����Ӧ����ȥ��Ӧ�IJ������һ�����̽����
ʵ����������Թ��м���5 mL 1 mol/L NaOH��Һ��5 mL �����飬��
ʵ�����II�����Թ���ͼ�̶���ˮԡ���ȡ�
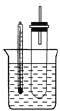
(1)��ˮԡ���ȶ���ֱ���þƾ��Ƽ��ȵ�ԭ����_______________________��
(2)�۲쵽__________________________����ʱ��������������NaOH��Һ����ȫ��Ӧ��
(3)�������������Ҵ��Ľṹ�����õIJ�����___________________________________��
(4)Ϊ֤����������NaOH�Ҵ���Һ�з���������ȥ��Ӧ��������Ƶ�ʵ�鷽���У���Ҫ�������__________������ķ�����____________(��˵�������õ��Լ�����ʵ�������Ԥ�������ʵ������)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��д�����з�Ӧ�Ļ�ѧ����ʽ����ָ����Ӧ���͡�
��1���屽���Ʊ�_________________________________________________��_____________����
��2���üױ��Ʊ�TNT _____________________________________________��_____________����
��3���ɱ�ϩ�Ʊ��۱�ϩ____________________________________________��_____________����
��4�����������������Ƶ��Ҵ���Һ����______________________________��_____________����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʵĵ���ƽ�⡢�����ˮ��ƽ�����������ܽ�ƽ������ڻ�ѧƽ�⡣����Ҫ��ش����}��
(1)����������������ˮ�����侻ˮ��ԭ����_____________(�����ӷ���ʽ��ʾ)��
(2)�����£�ȡ0.2 mol/L HCl��Һ��0.2mol/L MOH��Һ�������ϣ���û�Ϻ���Һ��pH=5����PH=13��MOH��Һ��Ũ��_______0.1mol/L(�������)��
(3)0.1mol/L��NaHA��Һ�������Һ�Լ��ԡ���
�� ����Һ�� c(H2A)_______________c(A2-)(�������)��
�� ���������жϵ�������_____________(�����ֽ���)��
(4)��Cr2O72-�ķ�ˮ���Խϴ�ij������ˮ�к�5.0��10-3 mol/L��Cr2O72-��Ϊ��ʹ��ˮ���ŷŴ�꣬�������´�����
![]()
�̷�ΪFeSO4 7H2O����Ӧ(I)��Cr2O72-��FeSO4�����ʵ���֮��Ϊ___________����������������ķ�ˮ��c(Cr3+)=6.0��10-7mol/L��������ķ�ˮ�� pH=_______��{Ksp[Cr(OH)3]=6.0��10-31}
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com