
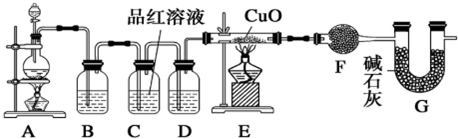
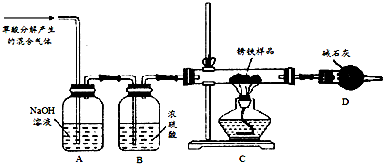
分析 A是制取气体的装置,制备的气体中有二氧化硫、氢气、水蒸汽,B装置是除去二氧化硫,可以用氢氧化钠等碱液吸收;C装置是检验二氧化硫是否除尽,D装置是浓硫酸,吸水干燥作用;E装置是用还原性气体还原氧化铜,F装置无水硫酸铜,检验是否有水生成;G是防止空气中H2O进入干燥管而影响杂质气体的检验,
(1)该仪器名称是分液漏斗;装置D中为浓硫酸干燥气体的作用;
(2)锌和稀硫酸反应生成硫酸锌和氢气;
(3)①二氧化硫属于酸性氧化物,能被碱液吸收;具有还原性,能被强氧化性溶液吸收;
②氢气具有还原性,能还原氧化铜,且生成水,水能使无水硫酸铜变蓝色,F中为硫酸铜,G是防止空气中水蒸气进入装置F运行现象观察.
解答 解:(1)该仪器名称是分液漏斗,D装置是浓硫酸,吸水干燥作用,
故答案为:分液漏斗;浓硫酸;
(2)随着硫酸浓度降低,锌和稀硫酸反应生成硫酸锌和氢气,离子方程式为Zn+2H+═Zn2++H2↑,故答案为:Zn+2H+═Zn2++H2↑;
(3)①二氧化硫属于酸性氧化物,能被碱液吸收;具有还原性,能被强氧化性溶液吸收,氢氧化钠溶液呈碱性,高锰酸钾溶液具有强氧化性,所以可以用氢氧化钠溶液和高锰酸钾溶液吸收二氧化硫,故选B,
故答案为:B;
②氢气具有还原性,能将黑色的CuO还原为红色的Cu,且生成水,水能使无水硫酸铜变蓝色,所以如果有氢气,看到的现象是:装置E中黑色粉末变红色,F中无水硫酸铜变蓝色,G的作用是防止空气中H2O进入干燥管而影响杂质气体的检验.;
故答案为:防止空气中H2O进入干燥管而影响杂质气体的检验.
点评 本题考查了探究实验,明确实验原理是解本题关键,根据物质的性质来分析解答,注意二氧化硫的漂白性,题目难度中等.


 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(NO)=0.0010mol•L-1•s-1 | B. | v(O2)=0.0010mol•L-1•s-1 | ||
| C. | v(NH3)=0.0100mol•L-1•s-1 | D. | v(H2O)=0.045mol•L-1•s-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.8gD2O 分子中含有的质子数为 NA | |
| B. | 常温下,7.8gNa2O2中含有的阴离子个数为 0.1NA | |
| C. | 标准状况下,11.2L 18O2中所含中子数为 8NA | |
| D. | 25℃时,2.24 LCO2分子中共用电子对数目为 0.4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金刚石比石墨稳定 | |
| B. | 石墨比金刚石稳定 | |
| C. | 含 1mol 碳原子的石墨比含 1mol 碳原子的金刚石总能量高 | |
| D. | 石墨和金刚石互为同位素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 因水分子间存在氢键,所以水加热到很高的温度都难以分解 | |
| B. | 1mol 冰中最多含有 4×6.02×1023个氢键,水分子间的氢键可表示为 O-H…O | |
| C. | 在“H2O(s)→H2O(l)→H2+O2”的变化过程中,被破坏的主要作用依次是氢键、极性键 | |
| D. | 等质量的水和冰,因水结冰后氢键数目变少,所以冰的密度比水小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 因为 H-F 的键能大于 H-Cl,所以 HF 沸点高于 HCl | |
| B. | SO3是由极性键构成的非极性分子 | |
| C. | 氯化钠和氯化铯晶体中氯离子的配位数相同 | |
| D. | 第一电离能大小比较 Br>Se>As |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高一上10月月考化学试卷(解析版) 题型:选择题
某同学配制一定物质的量浓度的NaOH溶液时,造成所配溶液浓度偏高的原因是( )
A. 用带游码的托盘天平称2.4g NaOH时误用了“左码右物”的方法
B. 所用NaOH已经潮解
C. 有少量NaOH溶液残留在烧杯里
D. 向容量瓶中加水未到刻度线
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com