
分析 甲烷与氯气光照下发生取代反应生成一氯甲烷、二氯甲烷、三氯甲烷和四氯化碳和HCl,其中有机产物中一氯甲烷为气体,据此分析.
解答 解:甲烷与氯气光照下发生取代反应生成一氯甲烷、二氯甲烷、三氯甲烷和四氯化碳和HCl,其中有机产物中一氯甲烷为气体,其它三种有机产物均为液态,故甲烷与氯气发生反应生成气态有机物的化学方程式为:CH4+Cl2$\stackrel{光照}{→}$CH3Cl+HCl,故答案为:CH4+Cl2$\stackrel{光照}{→}$CH3Cl+HCl.
点评 本题考查有机物的化学方程式的书写,为基础性习题,把握有机物的性质为解答的关键,注重基础知识的夯实,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
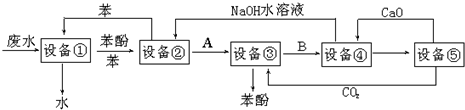
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 化学兴趣小组设定以下实验方案,测定某已变质为碳酸钠的小苏打样品中NaHCO3的质量分数.
化学兴趣小组设定以下实验方案,测定某已变质为碳酸钠的小苏打样品中NaHCO3的质量分数.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 弱酸酸式盐NaHB在水溶液中水解:HB-+H2O?H3O++B2- | |
| B. | 电解盐酸:2C1-+2H2O$\frac{\underline{\;通电\;}}{\;}$H2↑+Cl2↑+2OH- | |
| C. | 氢氧燃料电池在碱性介质中的正极反应式:O2+2H2O+4e一=4OH- | |
| D. | NaHCO3的电离:NaHCO3?Na++HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
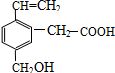 某有机物的结构为图所示,这种有机物具有的性质是( )
某有机物的结构为图所示,这种有机物具有的性质是( )| A. | ①②④ | B. | ①②③④ | C. | ②③④⑤ | D. | ①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 增大c(CH3COCH3) | B. | 增大c(I2) | C. | 升高温度 | D. | 增大压强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④ | B. | ②③⑤ | C. | ①③⑥ | D. | ①②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
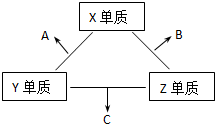 X、Y、Z三种短周期元素,它们的原子序数之和为16.X、Y、Z三种元素的常见单质在常温下都是无色气体,在适当条件下可发生如下变化:
X、Y、Z三种短周期元素,它们的原子序数之和为16.X、Y、Z三种元素的常见单质在常温下都是无色气体,在适当条件下可发生如下变化: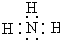 ,C分子的结构呈三角锥形.
,C分子的结构呈三角锥形.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com