
【题目】氧化镁在医药、建筑等行业应用广泛。硫酸镁还原热解制备高纯氧化镁是一种新的探索。以菱镁矿(主要成分为MgCO3,含少量FeCO3)为原料制备高纯氧化镁的实验流程如下:
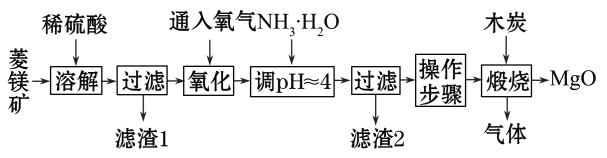
(1)通入O2氧化时,发生反应的离子方程式为________________________。
(2)滤渣2的成分是________(填化学式)。
(3)流程图中“操作步骤”为______________________、过滤等操作,得到MgSO4·7H2O晶体。对MgSO4·7H2O晶体直接加热________(填“能”或“不能”)得到无水MgSO4固体。
(4)长时间加热MgCO3悬浊液后生成Mg(OH)2,该反应的化学方程式为__________________________。
(5)已知酸碱指示剂百里酚蓝变色的pH范围如表所示:
pH | <8.0 | 8.9~9.6 | >9.6 |
颜色 | 黄色 | 绿色 | 蓝色 |
25 ℃时,向Mg(OH)2的饱和溶液中滴加2滴百里酚蓝指示剂,溶液所呈现的颜色为__________[25 ℃时,Ksp[Mg(OH)2]=5.6×10-12]。
【答案】(1)4Fe2++O2+4H+===4Fe3++2H2O
(2)Fe(OH)3
(3)蒸发浓缩、冷却结晶 能
(4)MgCO3+H2O![]() Mg(OH)2+CO2↑ (5)蓝色
Mg(OH)2+CO2↑ (5)蓝色
【解析】氧气是氧化剂,找出流程中的还原剂只能为Fe2+,通入氧气后溶液中为Fe2+、Mg2+,加入氨水由产品MgO可知Mg2+没有沉淀,Fe3+生成Fe(OH)3沉淀;(3)操作步骤的目的是从硫酸镁溶液中得到MgSO4·7H2O晶体,MgSO4·7H2O晶体受热易失去结晶水,所以不能蒸干;依据MgSO4+2H2O![]() Mg(OH)2+H2SO4,硫酸不挥发,所以水解不能进行到底;(5)由酸碱指示剂可知此题应该求溶液中的pH。Mg(OH)2(s)
Mg(OH)2+H2SO4,硫酸不挥发,所以水解不能进行到底;(5)由酸碱指示剂可知此题应该求溶液中的pH。Mg(OH)2(s) ![]() Mg2+(aq)+2OH-(aq),可知c(OH-)=2c(Mg2+),Ksp[Mg(OH)2]=
Mg2+(aq)+2OH-(aq),可知c(OH-)=2c(Mg2+),Ksp[Mg(OH)2]=![]() c3(OH-)=5.6×10-12,c(OH-)=
c3(OH-)=5.6×10-12,c(OH-)=![]() ×10-4mol·L-1,pH>10。
×10-4mol·L-1,pH>10。


科目:高中化学 来源: 题型:
【题目】常温下,用0.100 0 mol·L-1NaOH溶液滴定20.00 mL 0.100 0mol·L-1CH3COOH溶液所得滴定曲线如下图。下列说法正确的是( )

A.点①所示溶液中:c(CH3COO-)+c(OH-)=c(CH3COOH)+c(H+)
B.点②所示溶液中:c(Na+)=c(CH3COOH)+c(CH3COO-)
C.点③所示溶液中:c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
D.滴定过程中可能出现:c(CH3COOH)>c(CH3COO-)>c(H+)>c(Na+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若ABn型分子的中心原子A上没有未用于形成共价键的孤对电子,运用价层电子对互斥模型,下列说法正确的是( )
A.若n=2,则分子的立体构型为V形 B.若n=3,则分子的立体构型为三角锥形
C.若n=4,则分子的立体构型为正四面体形 D.以上说法都不正确
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为向25 mL 0.1 mol·L-1NaOH溶液中逐滴滴加0.2 mol·L-1CH3COOH溶液过程中溶液pH的变化曲线。请回答:
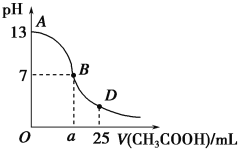
(1)B点溶液呈中性,有人据此认为,在B点时NaOH与CH3COOH恰好完全反应,这种看法是否正确?______(填“是”或“否”)。若不正确,则二者恰好完全反应的点是在AB区间还是BD区间内?______区间(若正确,此问不答)。
(2)关于该滴定实验,从下列选项中选出最恰当的一项________(填字母)。
锥形瓶中溶液 | 滴定管中溶液 | 选用指示剂 | 选用滴定管 | |
A | 碱 | 酸 | 酚酞 | (乙) |
B | 酸 | 碱 | 甲基橙 | (甲) |
C | 碱 | 酸 | 酚酞 | (甲) |
D | 酸 | 碱 | 酚酞 | (乙) |

(3)AB区间,c(OH-)>c(H+),则c(OH-)与c(CH3COO-)大小关系是________。
A.c(OH-)大于c(CH3COO-)
B.c(OH-)小于c(CH3COO-)
C.c(OH-)等于c(CH3COO-)
D.上述三种情况都可以
(4)在D点时,溶液中c(CH3COO-)+c(CH3COOH)________span>(填“>”“<”或“=”)2c(Na+)。Ⅱ.t ℃时,某稀硫酸溶液中c(H+)=10-a mol·L-1,c(OH-)=10-b mol·L-1,已知a+b=13。
(5)该温度下水的离子积常数Kw的数值为________。
(6)该温度下(t ℃),将100 mL 0.1 mol·L-1的稀H2SO4与100 mL 0.4 mol·L-1的NaOH溶液混合(溶液体积变化忽略不计),溶液的pH=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下面列出了几组物质,请将正确的序号填写在空格上。
①金刚石与“足球烯”C60; ②HCHO和CH3CHO; ③CH3CH2OH和CH3OCH3;④CH4和CH3CH2CH3;⑤D与T ; ⑥CH2=CH—CH2—CH3和CH3—CH=CH—CH3;⑦氧气(O2)与臭氧(O3)
同位素_________________;同系物_____________ ;
同素异形体_____________;同分异构体______________。
(2)现有下列六种有机物a.乙烷 b.乙烯 c.苯 d.乙醇 e.乙酸 f.CH2===CH—COOH g.CH2OH(CHOH)4CHO h.乙酸乙酯
①能与Na和NaOH溶液都反应的是_____________。
②分子内所有原子一定在同一平面上的有___________。
③常温下可能与溴水发生加成反应的有_____________。
④在一定条件下能发生酯化反应的有_______________。
⑤能与新制Cu(OH)2悬浊液反应的有________________。
⑥能发生水解反应的有______________。
(3)现有 A:CH3CH2OH; B:CH2OH—CH2OH;
C:CH2OH—CH(OH)—CH2OH三种有机物:
①等物质的量的这三种有机物完全燃烧耗氧量之比为______________;
②写出A与金属钠反应的化学方程式:_____________________________。
③等物质的量的这三种有机物与足量金属钠反应,同温同压下产生氢气的体积比为:__________________________。
④写出B在铜作催化剂的条件下与氧气反应的方程式:_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】每到冬天就会出现大雾天气,能见度不到10米,致使汽车行驶受阻,下列关于雾的说法正确的是( )
A.无法确定雾中水滴的直径大小 B.不会产生丁达尔现象
C.雾中水滴的直径在1nm~100nm间 D.雾中水滴的直径小于1nm
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向溶液中分别通入足量的相应气体后,下列各组离子还能大量存在的是( )
A.氯气:K+、Na+、SiO32﹣、NO3﹣
B.二氧化硫:Na+、NH4+、SO32﹣、C1﹣
C.硫化氢:H+、K+、MnO4﹣、SO42﹣
D.氨气:K+、Na+、AlO2﹣、CO32﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】光气(COCl2)在塑料、制革、制药等工业中有许多用途,工业上采用高温下CO与Cl2在活性炭催化下合成。
(1)实验室中常用来制备氯气的化学方程式为__________________________________。
(2)实验室中可用氯仿(CHCl3)与双氧水直接反应制备光气,其反应的化学方程式为________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com