
【题目】某有色金属研究室对从银锰精矿中提取单质银的方法进行改良创新,从而更高效地实现锰和银的分离。其简易流程如下图。已知:银锰精矿主要成分为MnO2和银单质。

(1)操作1与操作2所对应的分离方法是__________________。
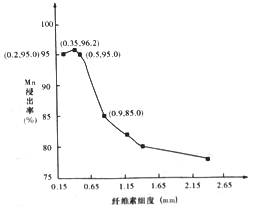
(2)通过对“浸出1”步骤中纤维细度的控制,绘制出一定时间内纤维素-Mn浸出率图象如上图所示,实际生产中应控制细度________mm较为合适,理由是_________。
(3)在“浸出1”步骤中,纤维素会先水解为单糖,请写出该单糖(用分子式表达)与银锰精矿反应的离子方程式:_______________________。
(4)浸出液2的主要成分为[Ag(CN)2]-,使用情性电极电解浸出液2,请写出阴极的电极方程式:________。本流程中可循环使用的物质为_________________。
(5)通过上述流程,浸出液1中通常还含有少量银离子,充分提取银,可对MnSO4·H2O晶体进行洗涤,请简述洗涤的方法_____________________________。将洗涤液与母液合并,加入盐酸,过滤后再经过以下步骤可回收大部分浸出液1中的银。试剂a是______________。
![]()
【答案】 过滤 0.5 细度为0.35 mm时,对生产工艺要求更高,但浸出率提升不明显;细度增大时,浸出率降低 C6H12O6+12MnO2+24H+==12Mn2++6CO2↑+18H2O [Ag(CN)2]- +e-==Ag+2CN- NaCN、O2 向过滤器中加冰水(或蒸溜水),至恰好浸没沉淀,待水自然流尽,重复以上操作23次 氨水
【解析】(1)操作1与操作2均为将不溶固体从溶液中分离出来,应选择过滤操作;
(2) 因纤维细度为0.35 mm时,对生产工艺要求更高,但浸出率提升不明显;纤维细度增大时,浸出率降低,故应控制细度0.5mm较为合适;
(3)纤维素水解生成的单糖为葡萄糖,在酸性条件下葡萄糖被MnO2氧化为CO2,同时溶液中得到Mn2+,根据电子守恒、电荷守恒及原子守恒,得此反应的离子方程式C6H12O6+12MnO2+24H+==12Mn2++6CO2↑+18H2O;
(4)[Ag(CN)2]-在阴极得电子发生还原反应,生成Ag,其电极方程式[Ag(CN)2]- +e-==Ag+2CN-;同时阳极产物为O2,则通过电解得到的NaCN、O2 均可循环使用;
(5)为减小MnSO4·H2O晶体的溶解损失,洗涤时可向过滤器中加冰水,至恰好浸没沉淀,待水自然流尽,重复以上操作23次即可;洗涤液与母液合并,加入盐酸,生成AgCl,利用浓氨水可溶解AgCl得到银氨溶液,再与葡萄糖发生银镜反应获得Ag,故试剂a是氨水。


 互动英语系列答案
互动英语系列答案科目:高中化学 来源: 题型:
【题目】明代名臣于谦作诗“凿开混沌得乌金,藏蓄阳和意最深。爝火燃回春浩浩,洪炉照破夜沉沉……”,诗中所写“乌金”是( )
A. 焦炭 B. 煤炭 C. 磁铁矿 D. 软锰矿
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学用语是学习化学的重要工具,是国际通用的化学语言。
(1)请用化学用语填空:
①人体缺乏后会引起贫血的元素____________;②两个氢原子____________。;③三个二氧化硫分子_____________;④四个碳酸根离子____________。
(2)在符号“![]() O”中H正上方的“+1”表示____________,H右下角的“2”表示____________。
O”中H正上方的“+1”表示____________,H右下角的“2”表示____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】150℃时,将1L混合烃与9L氧气混合没在密闭容器内充分燃烧,当恢复至150℃,体积恒定时,容器内压强增大8%,则该混合烃的组成是
A. 甲烷与乙烷的体积比是1∶4 B. 丙炔与乙炔的体积比是1∶4
C. 乙烯与丁烷的体积比是1∶4 D. 乙烯与丁烯的体积比是1∶4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A~G是几种烃的分子球棍模型(如图),据此回答下列问题:

(1)常温下含碳量最高的气态烃是 (填字母).
(2)能够发生加成的烃有 种.
(3)一卤代物种类最多的是 (填写字母).
(4)写出实验室制D的化学方程式 .
(5)写出F发生硝化反应的化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某固定体积的密闭容器中,加入—定量的A达化学平衡: aA(g)![]() B(g)+c(g),在温度不变的条件下,再充入一定量的A物质,重新达到平衡时,下列判断中正确的是
B(g)+c(g),在温度不变的条件下,再充入一定量的A物质,重新达到平衡时,下列判断中正确的是
A. 若a=b+c时,B的物质的量分数变大 B. 若a=b+c时,B的物质的量分数不变
C. 若a>b+c时,A的转化率不变 D. 若a<b+c时,A的转化率变大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】处理含铬废水的方法较多
Ⅰ.某工业废水中主要含有Cr3+,同时还含有少量的Cu2+、Fe2+、Fe3+和Al3+等,且酸性较强。为回收利用,通常采用如下流程处理:
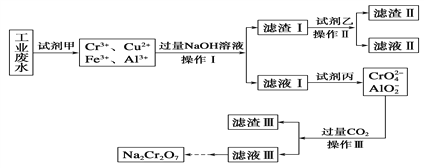
已知: Cr(OH)3―→NaCrO2―→Na2CrO4―→Na2Cr2O7
请回答:
(1)操作Ⅰ的名称为____________,上述操作Ⅰ、Ⅱ、Ⅲ相同,进行该实验操作所需要的主要玻璃仪器除烧杯、漏斗外,还有__________。
(2)滤渣Ⅰ的主要成分为________(写化学式),试剂乙的名称为__________。
(3)加入试剂甲的目的是____________________________________________________。
(4)废水处理流程中生成滤渣Ⅲ的离子方程式为________________________________。
Ⅱ.酸性条件下,六价铬主要以Cr2O![]() 形式存在。工业上用以下方法处理含Cr2O
形式存在。工业上用以下方法处理含Cr2O![]() 的废水:①往废水中加入适量的NaCl,搅拌均匀;②用Fe为电极进行电解,还原Cr2O
的废水:①往废水中加入适量的NaCl,搅拌均匀;②用Fe为电极进行电解,还原Cr2O![]() ;③经过一段时间,最后有Cr(OH)3和Fe(OH)3沉淀产生过滤回收沉淀,废水达到排放标准。
;③经过一段时间,最后有Cr(OH)3和Fe(OH)3沉淀产生过滤回收沉淀,废水达到排放标准。
(5) 在②步中,电解法除铬的原理是(写出涉及的主要电极反应式和离子方程式)_____________________________________________________________。
(6)已知某含Cr2O![]() 的酸性工业废水中铬元素的含量为104.5 mg·L-1,处理后铬元素最高允许排放浓度为0.5 mg·L-1。处理该废水1 000 m3并达到排放标准至少消耗铁的质量为________kg。
的酸性工业废水中铬元素的含量为104.5 mg·L-1,处理后铬元素最高允许排放浓度为0.5 mg·L-1。处理该废水1 000 m3并达到排放标准至少消耗铁的质量为________kg。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com