
| KW |
| C(H+) |
| 10-12 |
| 0.1 |


科目:高中化学 来源: 题型:
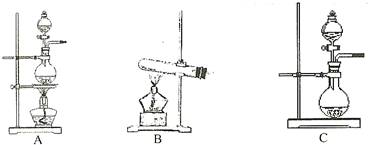
| 编号 | 实验内容 | 实验原理 | 发生装置 |
| ① | 制氧气 | H2O2→O2 | |
| ② | 制氨气 | NH4Cl→NH3 | |
| ③ | 制氯气 | HCL→Cl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 含氯消毒剂和过氧化物等强氧化性消毒剂可用于环境杀菌消毒.
含氯消毒剂和过氧化物等强氧化性消毒剂可用于环境杀菌消毒.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| t/s | 0 | 2 | 4 | 6 | 8 |
| n(Cl2)/mol | 0 | 0.30 | 0.39 | 0.40 | 0.40 |
| A、生成Cl2的平均反应速率,0~2s比2~4s快 |
| B、0~2s COCl2的平均分解速率为0.15mol?L-1?s-1 |
| C、6s时,反应达到最大限度 |
| D、该条件下,COCl2的最大转化率为40% |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com