
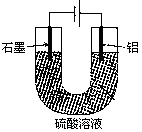
| A.阳极电极方程式为: Al—3e—+6OH—=Al2O3+H2O |
| B.随着电解的进行,溶液的pH逐渐增大 |
| C.当阴极生成气体3.36L(标况)时,阳极增重2.4g |
| D.电解过程中H+移向Al电极 |
 Al2O3+3H2↑,H2O减少,溶液的pH逐渐减小,错误;C、阴极反应为:2H++2e?=H2↑,H2的物质的量为3.36L÷22.4L/mol=0.15mol,则转移电子为:2×0.15mol=0.3mol,阳极反应为:根据差量法进行计算:设阳极增重的质量为x,
Al2O3+3H2↑,H2O减少,溶液的pH逐渐减小,错误;C、阴极反应为:2H++2e?=H2↑,H2的物质的量为3.36L÷22.4L/mol=0.15mol,则转移电子为:2×0.15mol=0.3mol,阳极反应为:根据差量法进行计算:设阳极增重的质量为x,

科目:高中化学 来源:不详 题型:填空题
| 物 质 | 开始沉淀 | 沉淀完全 |
| Fe(OH)3 | 2.7 | 3.7 |
| Fe(OH)2 | 7.6 | 9.6 |
| Mn(OH)2 | 8.3 | 9.8 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.4:1 | B.3:1 | C.2:1 | D.任意比 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.0.1mol | B.0.2mol | C.0.4mol | D.0.8mol 1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.电能全部转化为化学能 |
| B.粗铜接电源正极,发生还原反应 |
| C.溶液中Cu2+向阳极移动 |
| D.利用阳极泥可回收Ag、Pt、Au等金属 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
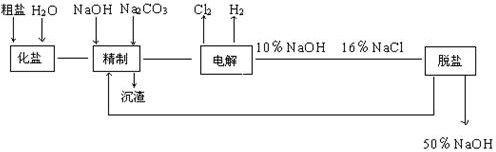
 含量较高,必须添加钡式剂除去SO
含量较高,必须添加钡式剂除去SO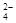 ,该钡试剂可以是(选填A.B.c,多选扣分)
,该钡试剂可以是(选填A.B.c,多选扣分) 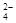 ,加入试剂的合理顺序为(选填a,b,c多选扣分)
,加入试剂的合理顺序为(选填a,b,c多选扣分)
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
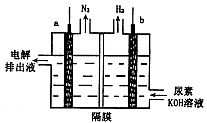
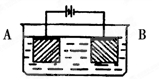
| A.电解时,b极是阴极放出H2,发生氧化反应 |
| B.溶液中OH—逐渐向b极移动 |
C.电解时,a极的电极反应式为: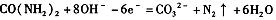 |
| D.若在b极产生标况下224mL氢气,则消耗尿素2g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com