
已知:NH3·H2O(aq)与H2SO4(aq)反应生成1 mol正盐的ΔH=-24.2 kJ·mol-1;强酸、强碱的稀溶液反应的中和热为ΔH=-57.3 kJ·mol-1。则NH3·H2O在水溶液中电离的ΔH等于( )
A.-69.4 kJ·mol-1 B.-45.2 kJ·mol-1
C.+69.4 kJ·mol-1 D.+45.2 kJ·mol-1
科目:高中化学 来源: 题型:
甲、乙、丙是三种不含相同离子的可溶性强电解质。它们所含离子如下表所示:
| 阳离子 | NH |
| 阴离子 | OH-、NO |
取等质量的三种化合物配制相同体积的溶液,其溶 质物质的量浓度:c(甲)>c(乙)>c(丙),则乙物质可能是( )
质物质的量浓度:c(甲)>c(乙)>c(丙),则乙物质可能是( )
①MgSO4 ②NaOH ③(NH4)2SO4 ④Mg(NO3)2 ⑤NH4NO3
A.①② B.③④
C.③⑤ D.①⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、W是原子序数依次增大的四种短周期元素,甲、乙、丙、丁、戊是由其中的两种或三种元素组成的化合物,己是由Z元素形成的单质。已知:甲+乙===丁+己,甲+丙===戊+己; 0.1 mol·L-1丁溶液的pH为13(25 ℃)。下列说法正确的是( )
A.原子半径:W>Y>Z>X
B.Y元素在周期表中的位置为第3周期第ⅣA族
C.1 mol甲与足量的乙完全反应共转移1 mol电子
D.化合物甲中只有离子键
查看答案和解析>>
科目:高中化学 来源: 题型:
将盛有NH4HCO3粉末的小烧杯放入盛有少量醋酸的大烧杯中。然后向小烧杯中加入盐酸,反应剧烈,醋酸逐渐凝固。由此可见( )
A. NH4HCO3和盐酸的反应是放热反应
B.该反应中,热能转化为产物内部的能量
C.反应物的总能量高于生成物的总能量
D.反应的热化学方程式为:NH4HCO3+HCl===NH4Cl+CO2↑+H2O ΔH=+Q
查看答案和解析>>
科目:高中化学 来源: 题型:
已知单质硫在通常条件下以S8(斜方硫)的形式存在,而在蒸气状态时,含有S2、S4、S6及S8等多种同素异形体,其中S4、S6和S8具有相似的结构特点,其结构如下图所示:
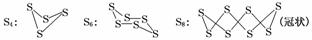
在一定条件下,S8(s)和O2(g)发生反应依次转化为SO2(g)和SO3(g)。反应过程和能量关系可用下图简单表示(图中的ΔH表示生成1 mol产物的数据)。
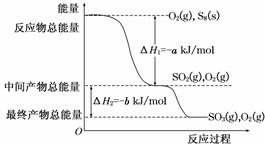
(1)写出表示S8燃烧热的热化学方程式_________________________________
____________。
(2)写出SO3分解生成SO2和O2的热化学方程式______________________________
________________________________________________________________________。
(3)化学上规定,拆开或形成1 mol化学键吸收或放出的能量称为该化学键的键能,单位kJ·mol。若已知硫氧键的键能为d kJ·mol-1,氧氧键的键能为e kJ·mol-1,则S8分子中硫硫键的键能为____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组物质稀溶液相互反应。无论前者滴入后者,还是后者滴入前者,反应现象都相同的是 ( )
A.Ca(HCO3)2溶液与Ca(OH)2溶液 B.AlCl3溶液与NaOH溶液[
C.KAlO2溶液与KHSO4溶液 D.2%的硝酸银溶液和2%的氨水
查看答案和解析>>
科目:高中化学 来源: 题型:
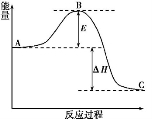 N2(g)+3H2(g)
N2(g)+3H2(g) 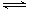 2NH3(g)反应过程的能量变化如下图所示。已知生成1 mol NH3(g)的ΔH=-46 kJ·mol-1。请回答下列问题:
2NH3(g)反应过程的能量变化如下图所示。已知生成1 mol NH3(g)的ΔH=-46 kJ·mol-1。请回答下列问题:
(1)图中A、C分别表示 、 ;若该反应使用催化剂,会使图中B点升高还是降低? 。
(2)图中ΔH= kJ·mol-1。
(3)已知恒容时,该体系中各物质浓度随时间变化的曲线如图所示。
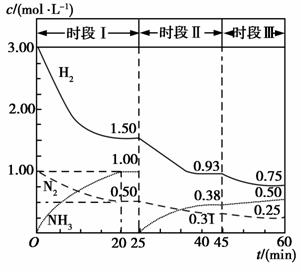
①在0.5 L容器中发生反应,前20 min内,v(NH3)=________,放出的热量为________。
②45 min时采取的措施是_______________________。
③比较I、II、III时段的化学平衡常数(分别用K1、K2、K3表示)大小________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com