
分析 (1)水溶液中部分电离的电解质为弱电解质;
(2)酸碱抑制水的电离,水解的盐促进水的电离;
(3)①NH3•H2O 是弱电解质存在电离平衡,铵根离子浓度最小,
②NH4Cl 铵根离子水解溶液显酸性,
⑦NH4HCO3 溶液中碳酸氢根离子水解促进铵根离子水解,铵根离子浓度减小,
⑧NH4HSO4,溶液中氢离子抑制铵根离子水解,铵根离子浓度增大;
(4)碳酸氢根离子的水解程度大于其电离程度,溶液呈碱性,则c(OH-)>c(H+)、c(Na+)>c(HCO3-),据此判断碳酸氢钠溶液中的离子浓度大小;
(5)溶液中存在电荷守恒,c(Na+)+c(H+)=c(OH-)+2c(SO42-),当溶液中c(Na+)=2c(SO42-)时,c(H+)=c(OH-)溶液显中性,氢离子物质的量和氢氧根离子物质的量相同.
解答 解:(1)属于弱电解质的是水溶液中存在电离平衡的化合物,①NH3•H2O,⑤CH3COOH 溶液中存在电离平衡,属于弱电解质,故答案为:①⑤;
(2)上述物质溶于水时,水的电离程度会减小的是①NH3•H2O 是碱抑制水的电离,⑤CH3COOH 是弱酸抑制水的电离,⑧NH4HSO4电离出氢离子抑制水的电离,
故答案为:①⑤⑧;
(3)①NH3•H2O 是弱电解质存在电离平衡,铵根离子浓度最小,
②NH4Cl 铵根离子水解溶液显酸性,
⑦NH4HCO3 溶液中碳酸氢根离子水解促进铵根离子水解,铵根离子浓度减小,
⑧NH4HSO4,溶液中氢离子抑制铵根离子水解,铵根离子浓度增大;
溶液中铵根离子浓度由大到小的顺序是⑧②⑦①,
故答案为:⑧②⑦①;
(4)碳酸氢钠溶液中,碳酸氢根离子的水解程度大于其电离程度,溶液呈碱性,则c(OH-)>c(H+)、c(Na+)>c(HCO3-),溶液中离子浓度大小为:c(Na+)>c(HCO3-)>c(OH-)>c(H+)>c(CO32-),
故答案为:c(Na+)>c(HCO3-)>c(OH-)>c(H+)>c(CO32-);
(5)设pH=4的H2SO4溶液XL和pH=9的NaOH溶液YL混合,当溶液中c(Na+)=2c(SO42-)时,c(H+)=c(OH-)溶液显中性,混合液的pH=7,pH=4的H2SO4溶液,c(H+)=1×10-4mol/L,pH=9的NaOH溶液,根据Kw=c(OH-)×c(H+),c(OH-)=$\frac{1{0}^{-14}}{1{0}^{-9}}$mol/L=1×10-5mol/L,若所得混合液为中性,酸碱恰好完全反应,n(H+)=n(OH-),则有1×10-4mol/L×XL=1×10-5mol/L×YL,X:Y=1:10,
故答案为:1:10.
点评 本题考查了弱电解质电离平衡、盐类水解应用、电解质溶液中离子浓度大小比较,酸碱反应溶液酸碱性判断,掌握基础是解题关键,题目难度中等.


 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,NA个H2和O2的混合气体的体积约为22.4 L | |
| B. | 1mol SiO2晶体中,含有2NA个Si-O键 | |
| C. | 0.1 mol Cl2溶解于一定体积的水中,转移电子数为0.2NA | |
| D. | 标准状况下,11.2 L H2O所含分子数为0.5 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
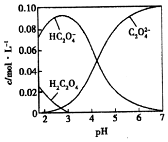 H2C2O4为二元弱酸.20℃时,配制一组c(H2C2O4)+c(HC2O4-)+c(C2O42-)=0.100mol•L-1的H2C2O4和NaOH混合溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如图所示.下列指定溶液中微粒的物质的量浓度关系一定正确的是( )
H2C2O4为二元弱酸.20℃时,配制一组c(H2C2O4)+c(HC2O4-)+c(C2O42-)=0.100mol•L-1的H2C2O4和NaOH混合溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如图所示.下列指定溶液中微粒的物质的量浓度关系一定正确的是( )| A. | pH=2.5的溶液中:c(H2C2O4)+c(C2O42-)>c(HC2O4-) | |
| B. | c(Na+)=0.100 mol•L-1的溶液中:c(H+)+c(H2C2O4)=c(OH-)+c(C2O42-) | |
| C. | c(HC2O4-)=c(C2O42-)的溶液中:c(Na+)>0.100 mol•L-1+c(HC2O4-) | |
| D. | pH=7.0的溶液中:c(Na+)=2(C2O42-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 苯甲醛 | 苯甲醇 | 苯甲酸 | 苯 | |
| 沸点/℃ | 178 | 205 | 249 | 80 |
| 熔点/℃ | 26 | -15 | 122 | 5.5 |
| 苯甲酸在水中的溶解度 | ||
| 17℃ | 25℃ | 100℃ |
| 0.21g | 0.34g | 5.9g |


查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | x>0 a<0 | |
| B. | b<o c<o | |
| C. | x=3a-b-c | |
| D. | 1mol碳(s)在空气中不完全燃烧生成CO的焓变小与akJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:W>Z>Y>X>M | |
| B. | 将XZ2通入W单质与水反应后的溶液中,一定只生成碳酸钠、碳酸氢钠 | |
| C. | 由X、Y、Z、M四种元素形成的化合物中一定有共价键可能有离子键 | |
| D. | CaX2、CaM2、CaZ2等3种化合物中,阳离子和阴离子个数比均为1:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
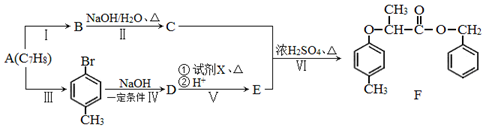
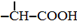 $→_{红磷、△}^{Cl_{2}}$
$→_{红磷、△}^{Cl_{2}}$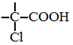
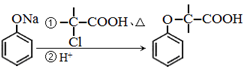
 +NaOH $→_{△}^{水}$
+NaOH $→_{△}^{水}$ +NaCl.
+NaCl. .
.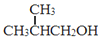 为原料制取
为原料制取 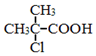 的合成路线图.
的合成路线图.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
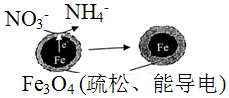
| A. | 能量转化形式主要为化学能转化为电能 | |
| B. | 电极材料分别为Fe和Fe3O4 | |
| C. | 负极反应为:NO3-+8e-+l0H+═NH4++3H2O | |
| D. | 该原理的总反应可表示为:NO3-+3Fe+2H++H2O═NH4++Fe3O4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 抗酸药能中和胃里过多的盐酸,缓解胃部不适 | |
| B. | 柠檬因为有酸味,所以属于酸性食品 | |
| C. | 目前加碘食盐中碘元素以KIO3形式存在 | |
| D. | 利用油脂在碱性条件下的水解,可以制甘油和肥皂 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com