
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
胡椒酚A是植物挥发油中的一种成分。对其分子组成结构的研究发现:A的相对分子质量不超过150;其中碳的质量分数为80.60﹪, 氧的质量分数为11.94﹪,A在空气中完全燃烧后产物只有CO2和H2O。
(1)A的分子式为
(2)红外光谱发现A中不含甲基,A遇FeCl3溶液呈紫色,会使溴水褪色且1molA与足量浓溴水反应时最多可消耗3molBr2。另外A在适当条件下与硝酸反应生成的一硝基取
代物只有两种,试写出A的结构简式
(3)在下面横线写出符合下列条件的A的一种同分异构体的结构简式:①苯环上含有两个取代基,②取代基位置与A相同,③能发生银镜反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
用下图所示装置进行实验,下列对实验现象的解释不合理的是
| ①中试剂 | ①中现象 | 解 释 | |
| A | Ba(NO3)2溶液 | 生成白色沉淀 | SO32-与Ba2+生成白色BaSO3沉淀 |
| B | 品红溶液 | 溶液褪色 | SO2具有漂白性 |
| C | 紫色石蕊溶液 | 溶液变红 | SO2与水反应生成酸 |
| D | 酸性KMnO4溶液 | 紫色褪去 | SO2具有还原性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
考生选做该题,得分计入总分,若化学考生总分超过100分,按100计分)
由氢气和氯气组成的混合气体,经光照充分反应后,通入100mL,1mol/LNaOH溶液中,溶液中某种离子的物质的量(图甲)和溶液的导电性(图乙)随着混合气体通入体积的变化而变化。
(1)图甲曲线表示溶液中__________离子的变化。
(2)对溶液进行导电性实验时,发现当通入的混合气体体积大于V1时,随着混合气体的通入,溶液导电性明显增强,引起增强的主要阴阳离子是________。
(3)当图甲中n1=0.02 mol 时,光照前的混合气体中H2和Cl2的物质的量之比为_____________

查看答案和解析>>
科目:高中化学 来源: 题型:
对下列实验现象的原因分析不正确的一项是
| 选项 | 实验现象 | 原因分析 |
| A | 浓硫酸遇湿润的蓝色石蕊试纸,先变红,后变黑 | 硫酸有酸性,使石蕊变红,浓硫酸有脱水性,使试纸炭化变黑 |
| B | 新制氯水中滴加石蕊试液,溶液先变红,后褪色 | 氯气与水反应生成HCl、HClO,HCl显强酸性,使石蕊变红,HClO具有强氧化性,使其褪色 |
| C | SO2通入溴水中,溴水褪色 | SO2具有漂白性,使其褪色 |
| D | 向湿润蔗糖中加入浓硫酸,固体迅速变黑,后体积急剧膨胀 | 在浓硫酸脱水作用下,蔗糖被炭化,炭与浓硫酸反应生成了CO2、SO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应的离子方程式书写不正确的是
A.二氧化硅与强碱溶液反应:SiO2+2OH-==SiO32-+H2O
 B.氯水与SO2溶液反应:Cl2+SO2+2H2O==4H++ClO-+SO32-
B.氯水与SO2溶液反应:Cl2+SO2+2H2O==4H++ClO-+SO32-
C.二氧化锰与浓盐酸反应:MnO2+4H++2Cl-==Mn2++2H2O+Cl2↑
D.将二氧化氮气体通入水中:2NO2+H2O==H++NO3-+NO
查看答案和解析>>
科目:高中化学 来源: 题型:
2014年初,雾覆天气多次肆虐我国中东部地区。加强汽车尾气排放监测和燃煤企业的治理对于减少雾霾具有重要的意义。
(1)利用原电池工作原理测定汽车尾气中CO的浓度,其装置如图所示。该电池中电解质为熔融碳酸盐,CO32-在固体介质中可以自由移动,气体A为 ,正极发生的电极反应式 。
 (2)某化学兴趣小组用下图所示流程,测定标准状况下体积为V L的燃煤烟气中SO2的含量:
(2)某化学兴趣小组用下图所示流程,测定标准状况下体积为V L的燃煤烟气中SO2的含量:
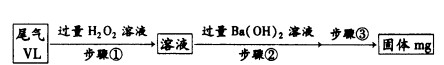
尾气中SO2的体积分数为 (用含有V、m的代数式表示)。
(3)已知常温下弱电解质的电离平衡常数如下
| NH3·H2O | Kb=1.8×10-5mol·L-1 |
| H2SO3 | Ka1=1.2×10-2mol·L-1 Ka2=1.3×10-8mol·L-1 |
 ①若用氨水吸收工业废气中的SO2,当吸收液失去吸收能力时,则此时溶液呈 性(填“酸”“碱”或“中”)。
①若用氨水吸收工业废气中的SO2,当吸收液失去吸收能力时,则此时溶液呈 性(填“酸”“碱”或“中”)。
②在通入废气的过程中,水的电离程度如何变化 。当恰好形成正盐时,溶液中离子浓度的大小关系为 。
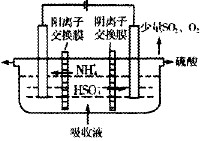
③可通过电解法使吸收液再生而循环利用(电极均为石墨电极),并生成化工原料硫酸。其工作示意图见右图。试写出生成硫酸的电极反应式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com