
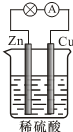
| A. | 负极的反应式为2H++2e-═H2↑ | |
| B. | 电子由Zn经外电路流向Cu,再经硫酸溶液流回Zn | |
| C. | 反应一段时间后,溶液的酸性增强 | |
| D. | 硫酸既提供反应物,又起导电作用 |
分析 锌、铜和稀硫酸组成的原电池中,锌作负极,负极上锌失电子发生氧化反应;铜作正极,正极上氢离子得电子发生还原反应;电子从负极沿导线流向正极,据此分析.
解答 解:A、锌作负极,负极上锌失电子发生氧化反应,电极反应式为Zn-2e-═Zn2+,故A错误;
B、电子从负极锌沿导线流向正极铜,但不经过硫酸溶液,故B错误;
C、锌、铜和稀硫酸组成的原电池中,活泼金属锌作负极,铜作正极,正极氢离子得电子生成氢气,所以消耗氢离子,则溶液的酸性减弱,故C错误;
D、锌、铜和稀硫酸组成的原电池中,硫酸既提供反应物,又起导电作用,故D正确;
故选D.
点评 本题考查了原电池原理,难度不大,注意把握正负极的判断和电极方程式的书写,注意溶液中酸性的变化.


科目:高中化学 来源: 题型:选择题
| A. | 锌和稀硫酸反应 | B. | 稀硫酸滴入紫色石蕊试液 | ||
| C. | 浓硫酸用作干燥剂 | D. | 浓硫酸与铜在加热的条件下反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ⑤ | ⑥ | ⑩ | |||||
| 3 | ① | ③ | ④ | ⑦ | ⑧ | ⑨ | ||
| 4 | ② |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在pH=l的溶液中:SO32-、NH4+、ClO-、Cl- | |
| B. | 有SO42-存在的溶液中:Na+、Mg2+、Ba2+、I- | |
| C. | 有NO3-存在的强酸性溶液中:NH4+、Ba2+、Fe2+、Br- | |
| D. | 在c(H+)=1.0×10-13mol•L-1的溶液中:Na+、SO42-、AlO2-、SO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子半径:Cl->Mg2+>Na+ | B. | 热稳定性:HF>H2O>H2S | ||
| C. | 酸性:HClO4>H2SO4>H3PO4 | D. | 非金属性:Cl>Br>I |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HX、HZ、HY | B. | HY、HZ、HX | C. | HZ、HY、HX | D. | HX、HY、HZ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com