
 短周期元素A、B、C、D 在元素周期表中的位置如右图所示,其中C 的原子序数是A 的2 倍,下说法正确的是( )
短周期元素A、B、C、D 在元素周期表中的位置如右图所示,其中C 的原子序数是A 的2 倍,下说法正确的是( )| A. | 原子半径:D>C>B | B. | 非金属性:B>C>A | ||
| C. | 最高正化合价:D>C>B | D. | 气态氢化物的稳定性:B>C>D |
分析 由短周期元素A、B、C、D 在元素周期表中的位置,A、C位于同主族,C 的原子序数是A 的2 倍,则A为O、C为S,结合位置可知,B为P、D为Cl,以此来解答.
解答 解:由上述分析可知,A为O,B为P,C为S,D为Cl,
A.同周期从左向右原子半径减小,则原子半径:B>C>D,故A错误;
B.同周期从左向右非金属性增强、同主族从上到下非金属性减弱,则非金属性为A>C>B,故B错误;
C.第三周期从左向右最高正化合价增大,则最高正化合价:D>C>B,故C正确;
D.非金属性越强,对应氢化物越稳定,则稳定性为D>C>B,故D错误;
故选C.
点评 本题考查原子结构与元素周期律,为高频考点,把握元素的位置、原子序数来推断元素为解本题关键,侧重分析与应用能力的考查,注意规律性知识的应用,题目难度不大.


 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源: 题型:选择题
| A. | 金刚石和石墨 | B. | ${\;}_1^1$H和${\;}_1^2$H | ||
| C. | CH3CH2OH和CH3OCH3 | D. | CH4和C2H6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石油裂化主要得到乙烯 | |
| B. | 石油分馏是化学变化,可得到汽油、煤油 | |
| C. | 煤制煤气是物理变化,是高效、清洁地利用煤的重要途径 | |
| D. | 煤干馏主要得到焦炭、煤焦油、粗氨水和焦炉气 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 甲醇是一种优质燃料,可制作燃料电池.
甲醇是一种优质燃料,可制作燃料电池.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HF的电子式为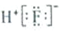 | |
| B. | 质子数为35,中子数为45的溴原子:${\;}_{35}^{80}$Br | |
| C. | Na2O2的电子式为: | |
| D. | 氯原子的结构示意图为: |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CCl4 | B. | 蒸馏水 | C. | 浓硫酸 | D. | AgNO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 W、X、Y、Z是四种常见的短周期主族元素,其原子半径随原子序数的变化如图所示.已知W的一种核素的质量数为18,中子数为10;X是短周期元素中原子半径最大的元素(不考虑稀有气体的原子半径);Y的单质呈黄色,常见于火山口附近.下列说法正确的是( )
W、X、Y、Z是四种常见的短周期主族元素,其原子半径随原子序数的变化如图所示.已知W的一种核素的质量数为18,中子数为10;X是短周期元素中原子半径最大的元素(不考虑稀有气体的原子半径);Y的单质呈黄色,常见于火山口附近.下列说法正确的是( )| A. | 氧化物的水化物酸性:Y<Z | |
| B. | 简单离子半径:W<X<Z | |
| C. | W的简单气态氢化物的沸点高于同族其它元素的简单气态氢化物 | |
| D. | 将标况下等体积的Z单质与Y的低价氧化物同时通入品红溶液中,品红溶液迅速褪色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com