
| A. | 氧化镁 | B. | 氧化铁 | C. | 二氧化锰 | D. | 氧化镍 |
 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案科目:高中化学 来源: 题型:选择题

| A. | X 难溶于乙醇 | |
| B. | 酒中少量的丁酸能抑制 X 的水解 | |
| C. | X 完全燃烧后生成CO2和H2O的物质的量比为 1:2 | |
| D. | 分子式为 C4H8O2且官能团与 X 相同的物质共有 5 种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 平衡后的压强为起始压强的1.25倍 | |
| B. | 平衡时混合气体的平均相对分子质量为64 | |
| C. | 混合气体的密度自始至终保持不变 | |
| D. | 取和SO3等质量的SO2和O2的混合气体,从逆反应开始并达到平衡,在相同条件下各物质的浓度与原来的平衡浓度一定相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2 个 | B. | 3个 | C. | 4个 | D. | 5个 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
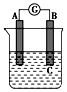 如图所示装置,电流表指针发生偏转,同时A极逐渐变粗,B极逐渐变细,C为电解质溶液,则A、B、C应是下列各组中的( )
如图所示装置,电流表指针发生偏转,同时A极逐渐变粗,B极逐渐变细,C为电解质溶液,则A、B、C应是下列各组中的( )| A. | A是Zn,B是Cu,C为稀硫酸 | B. | A是Cu,B是Zn,C为稀硫酸 | ||
| C. | A是Cu,B是Fe,C为稀Cu(NO3)2溶液 | D. | A是Fe,B是Ag,C为稀AgNO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 物质 | 使用的试剂 | 主要操作 |
| A | 乙醇(水) | 氧化钙 | 蒸馏 |
| B | 乙酸乙酯(乙酸) | 饱和氢氧化钠溶液 | 分液 |
| C | 苯(苯酚) | 浓溴水 | 过滤 |
| D | 乙烷(乙烯) | 酸性高锰酸钾溶液 | 洗气 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 操作步骤 | 预期现象 |
| ①取少量样品于试管中,加入足量的3mol/LH2SO4,充分振荡,将所得澄清的溶液分装在两支试管中. | |
| ②向一支试管中加入足量铁粉,充分振荡;再加入足量3mol/LH2SO4,充分振荡. | 若出现红色固体,则含有CuO. |
| ③向另一支试管中加入0.01mol/L酸性KMnO4溶液. | 若溶液紫红色褪去则含有FeO. |

查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 滴定次数 | 标准溶液的体积/mL | 待测溶液的体积 | |
| 滴定前刻度/mL | 滴定后刻度/mL | ||
| 1 | 25.00 | 1.02 | 21.04 |
| 2 | 25.00 | 2.00 | 21.98 |
| 3 | 25.00 | 0.20 | 20.20 |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com