
| A. | 化学反应中的能量变化,通常表现为热量的变化 | |
| B. | 反应物的总能量高于生成物的总能量时发生放热反应 | |
| C. | Ba(OH)2•8H2O与NH4Cl的反应是吸热反应 | |
| D. | 在化学反应中需要加热的反应就是吸热反应 |
分析 A、化学反应中的能量变化,通常表现为热量的变化,还可以表现为其它形式的能量变化;
B、当反应物的总能量高于生成物的总能量时,反应放热;
C、铵盐和碱的反应为吸热反应;
D、不能根据反应条件来判断反应吸放热.
解答 解:A、化学反应中的能量变化,通常表现为热量的变化,还可以表现为其它形式的能量变化,如光能和电能的变化,故A正确;
B、当反应物的总能量高于生成物的总能量时,反应放热;当当反应物的总能量低于生成物的总能量时,反应吸热,故B正确;
C、铵盐和碱的反应为吸热反应,故Ba(OH)2•8H2O与NH4Cl的反应是吸热反应,故C正确;
D、不能根据反应条件来判断反应吸放热,需要加热的反应不一定是吸热反应,不需要加热的反应不一定放热,故D错误.
故选D.
点评 本题考查了化学反应中的能量变化,应注意的是化学反应条件与反应吸放热无关,难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用酸性高锰酸钾溶液区别乙烷和乙烯 | |
| B. | 用BaCl2除去NaOH 溶液中混有的少量Na2SO4 | |
| C. | 用KSCN溶液检验溶液中含有的Fe2+ | |
| D. | 用溶解、过滤的方法分离CaCl2和NaCl固体混合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
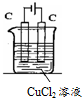 电解氯化铜溶液的化学方程式为CuCl2$\frac{\underline{\;通电\;}}{\;}$Cu+Cl2↑.电解过程中,Cu2+离子向阴极移动;Cl-在阳极失电子,发生氧化反应(填“氧化”或“还原”).电解过程中,如果有0.4mol的电子发生转移,理论上阴极的质量将增加12.8g.
电解氯化铜溶液的化学方程式为CuCl2$\frac{\underline{\;通电\;}}{\;}$Cu+Cl2↑.电解过程中,Cu2+离子向阴极移动;Cl-在阳极失电子,发生氧化反应(填“氧化”或“还原”).电解过程中,如果有0.4mol的电子发生转移,理论上阴极的质量将增加12.8g.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
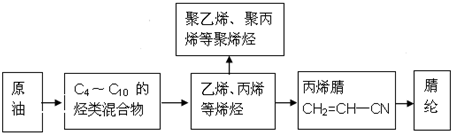
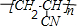 .
.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
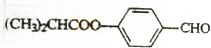 E的合成路线如下:
E的合成路线如下: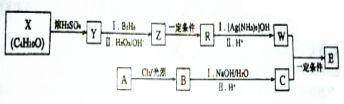
 .X→Y的反应类型是消去反应.
.X→Y的反应类型是消去反应.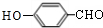 $?_{△}^{浓硫酸}$
$?_{△}^{浓硫酸}$ +H2O
+H2O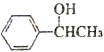 )为原料合成苯乙醛,设计合成路线:
)为原料合成苯乙醛,设计合成路线: $\stackrel{NaOH的醇溶液、加热}{→}$
$\stackrel{NaOH的醇溶液、加热}{→}$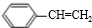 $\frac{Ⅰ.{B}_{2}{H}_{6}}{Ⅱ.{H}_{2}{O}_{2}/OH}$
$\frac{Ⅰ.{B}_{2}{H}_{6}}{Ⅱ.{H}_{2}{O}_{2}/OH}$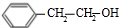 $\stackrel{Cu/△}{→}$
$\stackrel{Cu/△}{→}$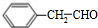 .
.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
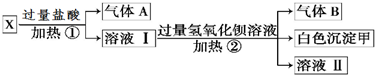
 ;溶液II中存在的阴离子为OH-、Cl-.
;溶液II中存在的阴离子为OH-、Cl-.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2的电子式: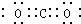 | B. | 乙炔分子的结构式H-C≡C-H | ||
| C. | H2O分子的比例模型  | D. | Clˉ离子的结构示意图: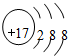 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com