
 ͼ��ʾ��ת����ϵ�У��ס��Ҽ�A��B��C��D��E��Ϊ��ѧ�����Ļ�ѧ���ʣ����мס���Ϊ�����A��B��DΪ���ʣ�
ͼ��ʾ��ת����ϵ�У��ס��Ҽ�A��B��C��D��E��Ϊ��ѧ�����Ļ�ѧ���ʣ����мס���Ϊ�����A��B��DΪ���ʣ� Fe3O4+4H2��
Fe3O4+4H2�� Fe3O4+4H2��
Fe3O4+4H2�� CO2��+2SO2��+2H2O��
CO2��+2SO2��+2H2O�� CO2��+2SO2��+2H2O��
CO2��+2SO2��+2H2O��

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
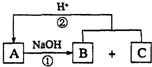 ����ͼ��ʾ��ת����ϵ�У�A��B��C����ѧ��ѧ�г��������ʣ�������ͬһ��Ԫ��R��������Ԫ����������������18���ش��������⣮��˵����ͼ�в���R�IJ��������ȥ����Ӧ�ڵIJ���֮һ��A��
����ͼ��ʾ��ת����ϵ�У�A��B��C����ѧ��ѧ�г��������ʣ�������ͬһ��Ԫ��R��������Ԫ����������������18���ش��������⣮��˵����ͼ�в���R�IJ��������ȥ����Ӧ�ڵIJ���֮һ��A���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
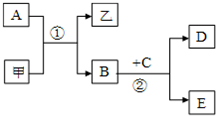 ͼ��ʾ��ת����ϵ�У��ס��Ҽ�A��B��C��D��E��Ϊ��ѧ�����Ļ�ѧ���ʣ����мס���Ϊ�����A��B��DΪ���ʣ�
ͼ��ʾ��ת����ϵ�У��ס��Ҽ�A��B��C��D��E��Ϊ��ѧ�����Ļ�ѧ���ʣ����мס���Ϊ�����A��B��DΪ���ʣ�
| ||
| ||
| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
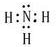
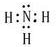
| 1 | 18 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
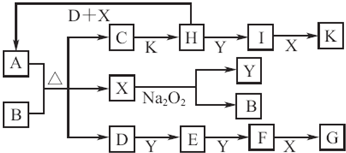
��10�֣���ͼ��ʾ��ת����ϵ�У���֪A���ɶ�����Ԫ����ɵ���ʽ�Ρ�D��Y��HΪ���壬XΪ��ɫҺ�壬G��K���dz�����ǿ�ᡣH��Na2O2�ɷ������Ϸ�Ӧ�����ɵ�����Ba2����Ӧ�����ɲ�����ϡG�İ�ɫ������һ��D�����к���10�����ӡ�
��ش��������⣺
��1���õ���ʽ��ʾX���γɹ��̣�____________________��
��2��д��D��H��X��Ӧ����A�����ӷ�Ӧ����ʽ��____________________��
��3����֪��2H��g����Y��g��![]() 2I��g����
2I��g����![]() ��������4 mol H��2 mol Y�ų�345 kJ������ʱ��H��ת������ӽ���__________������ĸ����
��������4 mol H��2 mol Y�ų�345 kJ������ʱ��H��ת������ӽ���__________������ĸ����
A��40% B��50% C��80% D��90%
��4����״������1000mLij�ܱ�������װ��440mL��C��Һ�������м���3.9g Na2O2��ַ�Ӧ��ָ���ԭ�¶ȣ���������������ѹǿ��Ϊԭ����1.5����������Һ����仯������ԭC��Һ�����ʵ���Ũ��Ϊ__________mo1��L��1����������λ��Ч���֣�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2010�����ʡ����5�µڶ���ģ�⿼�ԣ������ۺϣ���ѧ���� ���ͣ������
��10�֣���ͼ��ʾ��ת����ϵ�У���֪A���ɶ�����Ԫ����ɵ���ʽ�Ρ�D��Y��HΪ���壬XΪ��ɫҺ�壬G��K���dz�����ǿ�ᡣH��Na2O2�ɷ������Ϸ�Ӧ�����ɵ�����Ba2����Ӧ�����ɲ�����ϡG�İ�ɫ������һ��D�����к���10�����ӡ�
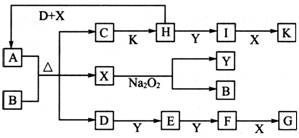
��ش��������⣺
��1���õ���ʽ��ʾX���γɹ��̣�____________________��
��2��д��D��H��X��Ӧ����A�����ӷ�Ӧ����ʽ��____________________��
��3����֪��2H��g����Y��g��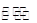 2I��g����
2I��g����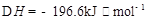 ��������4 mol H��2 mol Y�ų�345 kJ������ʱ��H��ת������ӽ���__________������ĸ����
��������4 mol H��2 mol Y�ų�345 kJ������ʱ��H��ת������ӽ���__________������ĸ����
A��40% B��50% C��80% D��90%
��4����״������1000mLij�ܱ�������װ��440mL��C��Һ�������м���3.9g Na2O2��ַ�Ӧ��ָ���ԭ�¶ȣ���������������ѹǿ��Ϊԭ����1.5����������Һ����仯������ԭC��Һ�����ʵ���Ũ��Ϊ__________mo1��L��1����������λ��Ч���֣�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com