
| 1.28g |
| 1.40g |


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ˮ | B����ĭ����� |
| C�������ɳ�� | D���ɱ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����2����1����3�� |
| B����2����3����1�� |
| C����1����2����3�� |
| D����3����2����1�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ij�������ʽ��NaHA��Һ��һ���У�c��OH-��+2c��A2-��=c��H+��+c��H2A�� |
| B��0.1mol?L-1CH3COONa��Һ��0.05mol?L-1����������Ϻ��������Һ�У�c��CH3COO-����c��CH3COOH����c��Cl-����c��H+�� |
| C�����ʵ���Ũ����ȵ�HCN��Һ��NaCN��Һ�������Ϻ����Һ�У�c��CN-��+2c��OH-��=2c��H+��+c��HCN�� |
| D��0.1mol?L-1��NH4��2Fe��SO4��2��Һ�У�c��NH4+��+c��NH3?H2O��+c��Fe2+��=0.3mol?L-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����Ư�۵���Һ��ͨ�����������������壺Ca2++2ClO-+SO2+H2O=CaSO3+��2HClO | ||||
B���ö��Ե缫��ⱥ��ʳ��ˮCl-+H2O
| ||||
| C���Ȼ�������Һ�е�������˫��ˮ2Fe2++2H++H2O2=2Fe3++2H2O | ||||
| D�������ʵ���Ũ�ȡ��������Ca��HCO3��2��Һ������������Һ���ϣ�Ca2++2HCO3-=CaCO3��+CO32-+2H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

 ���Ͱ�˾ƥ�������ƵĽṹ������һ���Ʊ���������
���Ͱ�˾ƥ�������ƵĽṹ������һ���Ʊ���������
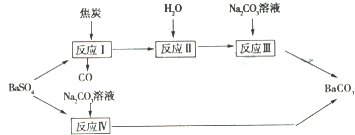
 ���������������ڼ��������·�Ӧ�Ļ�ѧ����ʽΪ
���������������ڼ��������·�Ӧ�Ļ�ѧ����ʽΪ�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com