
C��O��Na��Al��S��Cl�dz���������Ԫ��
��1��CԪ��λ��Ԫ�����ڱ��� ���ڣ��� �壻CԪ�ص�һ��ͬλ�ؿ��Բⶨ�������������ͬλ�صķ���Ϊ
��2���á����ڡ���С�ڡ����ڡ����
���Ӱ뾶 | ���� | ��ԭ�� | �õ������� |
N3- Al3+ | H2SO4 HClO4 | O2- S2- | 35Cl 37Cl |
��3���� CaCO3������HCl��Һ��Ӧʱ��ÿ����4.4 g ���壨�����������ܽ⣩������a kJ����÷�Ӧ���Ȼ�ѧ����ʽΪ ��
��������Ӧ���������ݳ���ȡ����������Һ������pH����������ε���̼������Һ�����pH�仯������ͼ��ʾ
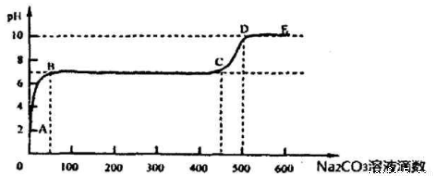
�������ӷ���ʽ��ʾB-C�η����ķ�Ӧ��
��4��������������������ȼ�ϵ�أ�д�������Ϊ����������Һʱ�����ϵĵ缫����ʽ
1���� ��IVA �� 14C����2������; С��; С��; ���ڣ�
��3�� �� CaCO3��s��+ 2HCl��aq��= CaCl2��aq��+ H2O(l) +CO2(g) ?H = -10a kJ/mol�� �� Ca2+ + CO32- = CaCO3����
��4��H2-2e-+2OH- = 2H2O��
��������
�����������1��CԪ��λ��Ԫ�����ڱ��ڶ����ڵ�IVA��CԪ�ص�һ��ͬλ�ؿ��Բⶨ�������������ͬλ�صķ���Ϊ14C����2��N3-��Al3+�ǵ��Ӳ�ṹ��ͬ�����ӣ��˵�����ƶ����Ӱ뾶��ԽС���������Ӱ뾶��N3->Al3+; ����H2SO4<HClO4; Ԫ�صķǽ�����O>S��Ԫ�صķǽ�����Խǿ������Ӧ�����ӵĻ�ԭ�Ծ�Խ�������Ի�ԭ��O2-<S2-;35Cl��37Cl����Ԫ�ص�ͬλ��ԭ�ӣ����ǻ�õ��ӵ�������ͬ����3���� CaCO3������HCl��Һ��Ӧʱ��ÿ����4.4 g ���壨�����������ܽ⣩������a kJ������n(CO2)=0.1mol����÷�Ӧ���Ȼ�ѧ����ʽΪCaCO3��s��+ 2HCl��aq��= CaCl2��aq��+ H2O(l) +CO2(g) ?H = -10a kJ/mol����������Ӧ���������ݳ���ȡ����������Һ������pH����������ε���̼������Һ�����ݲ��pH�仯���������ӷ���ʽ��ʾB-C�η����ķ�ӦΪCa2+ + CO32- = CaCO3������4��������������������ȼ�ϵ�أ��������Ϊ����������Һʱ�����ϵĵ缫����ʽ��H2-2e-+2OH- = 2H2O��������Ӧʽ�ǣ�O2+4e-+2H2O = 4OH- ,�ܷ���ʽ��2H2+O2= 2H2O��
���㣺����Ԫ�ص��ƶϡ����İ뾶�뾶�����ӵĻ�ԭ�ԱȽϡ�����Һ������ǿ���Ƚϡ����ӷ���ʽ����д��ԭ��ؽṹ����Ӧԭ����Ӧ�õ�֪ʶ��


 ��������ϵ�д�
��������ϵ�д� ��ӡ�Ļ���ʱ����ϵ�д�
��ӡ�Ļ���ʱ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015��㶫ʡ�����и�����ѧ�ڵ�һ��������⻯ѧ�Ծ��������棩 ���ͣ�ʵ����
������һ�ֻ���ԭ�ϡ�
��1����д����ҵ�Ϻϳɰ��Ļ�ѧ����ʽ��
��2��ʵ�����У��ס�����С��ѡ���˲�ͬ������ȡ�������뽫ʵ��װ�õ���ĸ��ź��Ʊ�ԭ����д���±��ո��С�
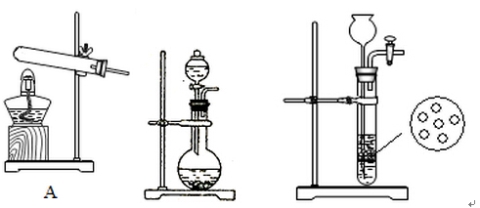
B C
| ʵ��װ�� | ʵ��ҩƷ | �Ʊ�ԭ�� |
���� | A
|
| ��Ӧ�Ļ�ѧ����ʽΪ �� |
���� |
| Ũ��ˮ���������ƹ��� | �������Ƶ����ã���ˮ�д���ƽ�⣺ |
��3�������һ��������ʵ�飬��֤NH3��H2O��������ʡ�
��
��4����ͬѧ���Ƶõİ�����������ˮ�У��õ�ϡ��ˮ���ñ�Ũ�ȵ�����ζ����ⶨ��Ũ�ȡ�ʵ�鲽�裺ȷ��ȡ10.00mLϡ��ˮ����ƿ�У�����20mLˮϡ�ͣ��μ� ��Һ��Ϊָʾ�����ʯ�������̪�����ȡ������� ���0.020������0.05������0.1980����1.5����mol?L-1����װ��50ml��ʽ�ζ��ܣ��ζ��� ��ֹͣ�ζ�����¼���ݡ��ظ��ζ�2�Ρ�ƽ����������Vml������ԭϡ��ˮ�����ʵ���Ũ��
= ��ֻ�г���ʽ���������㣩
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�찲��ʡ�������·ݻ�ѧ�¿��Ծ��������棩 ���ͣ�ѡ����
��֪�����η���E��ֱ���η���G��Ӧ����������ֱ���η���L��M (���E��G��L��M���ӵ�Ԫ��ԭ��������С��10) ����ͼ���������жϴ������

A��G������õķǽ������� B��M��ѧ���ʻ���
C��E��ʹ��ɫʯ����Һ����ɫ D��L�Ǽ��Է���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�찲��ʡͬ����ʱ�����˽�ѡ��4��1.2 ȼ������Դ�Ծ��������棩 ���ͣ������
��֪�����Ȼ�ѧ����ʽ��
��CaCO3(s) CaO(s)+CO2(g)����H=+177��7 kJ
CaO(s)+CO2(g)����H=+177��7 kJ
��C(s)+H2O(g) CO(g)+H2(g)����H=+131��3 kJ��mol-1
CO(g)+H2(g)����H=+131��3 kJ��mol-1
��HCl(l)+NaOH(l) NaCl(l)+H2O(l)����H=-57��3 kJ��mol-1
NaCl(l)+H2O(l)����H=-57��3 kJ��mol-1
��C(s)+O2(g) CO2(g)����H=-393��5 kJ��mol-1
CO2(g)����H=-393��5 kJ��mol-1
��CO(g)+O2(g) CO2(g)����H=-283 kJ��mol-1
CO2(g)����H=-283 kJ��mol-1
��2H2(g)+O2(g) 2H2O(l)����H=-571��6 kJ��mol-1
2H2O(l)����H=-571��6 kJ��mol-1
��1�������Ȼ�ѧ����ʽ�У�����ȷ���С���
��2��������Ӧ�У���ʾȼ���ȵ��Ȼ�ѧ����ʽ�С���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�찲��ʡͬ����ʱ�����˽�ѡ��4��1.2 ȼ������Դ�Ծ��������棩 ���ͣ�ѡ����
������Դ������˵���в���ȷ����(����)
A��ú��ʯ�͡���Ȼ����ȼ��������������Դ
B��ú��ʯ�͡�ˮú���ɴ���Ȼ��ֱ�ӻ�ȡ����һ����Դ
C��̫������һ����Դ������Դ����������Դ
D����ϫ����Դ��������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�찲��ʡ��У�����о��������һ��������ѧ�Ծ��������棩 ���ͣ�ѡ����
ˮ�ȷ��Ʊ�ֱ��Ϊ1~100 nm�Ŀ���Y�����������Ӧԭ��Ϊ��3Fe2+ + 2S2O32- + O2 + aOH��= Y+ S4O62- + 2H2O������˵���в���ȷ����
A��a��4
B����Y���ȷ�ɢ��ˮ���γɵ���ϵ���ж����ЧӦ
C��S2O32-�ǻ�ԭ��
D��ÿ��3 mol Fe2+ �μӷ�Ӧ����Ӧ��ת�Ƶĵ�������Ϊ5 mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�찲��ʡ��У�����о��������һ��������ѧ�Ծ��������棩 ���ͣ�ѡ����
��NaOH��Һ��μ���NH4HCO3��Һ�У�������Һ����ı仯�������и�ʾ��ͼ��ʾ�Ļ����Һ�й����ı仯������ȷ����
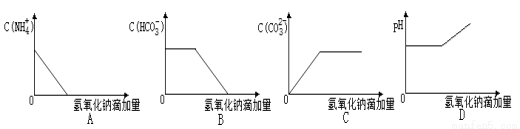
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�찲��������ѧͬ����ʱ�����˽�ѡ��4��4.1ԭ����Ծ��������棩 ���ͣ�ѡ����
��ͼ��п��ͭ��ϡ�����γɵ�ԭ��أ�ijʵ����ȤС��ͬѧ����ʵ����ڶ��鿨Ƭ�ϼ�¼���£�

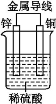
��Ƭ�ϵ�������������(����)
A���٢ڢ� B���ۢܢ� C���٢ݢ� D���ڢۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�찲��ʦ���и߶���ѧ�����п��黯ѧ�Ծ��������棩 ���ͣ�ѡ����
����ͬ�����£�T=500K������ͬ����ļ��������������г���1gSO2��1gO2�����г���2gSO2��2gO2�����������в���ȷ����( )
A����Ӧ���ʣ���>�� B��ƽ��������SO2�������������>��
C��SO2��ת���ʣ���>�� D��ƽ��ʱO2��Ũ�ȣ���>��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com