
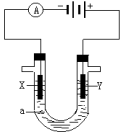
 ���ԭ���ڻ�ѧ��ҵ���й㷺Ӧ�ã���ͼ��ʾһ�����أ�װ�е��Һa��X��Y������缫�壬ͨ��������ֱ����Դ�������ش��������⣺
���ԭ���ڻ�ѧ��ҵ���й㷺Ӧ�ã���ͼ��ʾһ�����أ�װ�е��Һa��X��Y������缫�壬ͨ��������ֱ����Դ�������ش��������⣺���� ��1����ⱥ��ʳ��ˮʱ���ɵ�Դ��֪��XΪ������YΪ��������������������ʧ���ӣ��������������ӵõ��ӣ��Դ˽����⣻
��2��Y�缫�������ӷŵ���������������������ʪ��ĵ��۵⻯����ֽ���飻
��3����Ҫ�õ�ⷽ��������ͭ�����Һaѡ��CuSO4��Һ������Ӧ���Ǵ�ͭ�������Ǵ�ͭ����X�缫�Ǵ�ͭ��Y�缫�Ǵ�ͭ��������ͭ���ӷŵ磮
��� �⣺��1���͵�Դ�ĸ��������ĵ缫X�����������õ缫�������ӷ����õ��ӵĻ�ԭ��Ӧ����2H++2e-=H2����������Χ�������������������ӣ����Եη�̪��Һ��죬���������ݲ�������Һ��죬�ʴ�Ϊ�������ݣ���Һ��죻
��2����X��Y���Ƕ��Ե缫��a�DZ���NaCl��Һ��Y�缫�������ӷŵ������������缫��ӦʽΪ2Cl--2e-=Cl2�����������������ԣ����������������ɵⵥ�ʣ�����������Һ����ɫ����������������ʪ��ĵ��۵⻯����ֽ���飬
�ʴ�Ϊ��2Cl--2e-=Cl2������ʪ��ĵ��۵⻯����ֽ�ӽ������ڣ������ֽ����ɫ��˵������������
��3����Ҫ�õ�ⷽ��������ͭ�����Һaѡ��CuSO4��Һ������Ӧ���Ǵ�ͭ�������Ǵ�ͭ����X�缫�Ǵ�ͭ��Y�缫�Ǵ�ͭ�������缫��Ӧʽ��Zn-2e�TZn2+��Cu-2e-�TCu2+��������ͭ���ӷŵ磬�缫��ӦʽΪCu2++2e-=Cu��
�ʴ�Ϊ����ͭ��Zn-2e�TZn2+��Cu-2e-�TCu2+��
���� ���⿼��ԭ���ԭ�����漰�缫��Ӧʽ����д�������ļ����֪ʶ�㣬֪�����ӷŵ�˳�缫��Ӧʽ����д�����������ļ��鷽����������Ŀ�ѶȲ���


 ������ÿ�ʱ��ҵϵ�д�
������ÿ�ʱ��ҵϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Ӧֹͣ�� | |
| B�� | NO������Ӧ������O2���淴Ӧ������� | |
| C�� | c��NO����c��O2��=2��1 | |
| D�� | �������ɫ���ٱ仯 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ʹ��̪��Һ������ɫ��Һ�У�Na+��CO32-��K+��ClO- | |
| B�� | �����������Ӧ�ų���������Һ�У�K+��NO3-��Cl-��NH4+ | |
| C�� | ������ˮ�������c��H+ ��•c��OH- ��=10-20����Һ�У�Na+��Cl-��S2-��SO32- | |
| D�� | ��ɫ����Һ��K+��HCO3-��NO3-��SO42-��Fe3+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
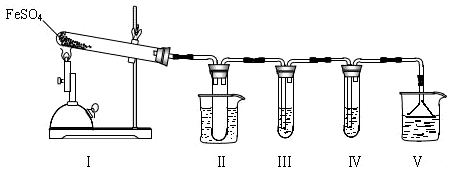
| �����Լ� | Ԥ������ͽ��� |
| װ�â���Թ��м���0.5 mol•L -1 BaCl2�� | ����������ɫ������֤����������к���SO3�� |
| װ�â����Թ��м���0.01 mol•L-1 ���� KMnO4 ��Һ����0.0l mol•L-1 ��ˮ���� | ����Һ��ɫ�����ɫ����ȥ��֤����������к���SO2������Һ��ɫ�����ɫ�������Ա仯��֤����������в���SO2 |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
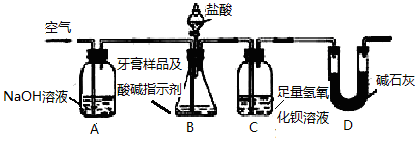
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��˾ƥ���dz��õĿ���ҩ | |
| B�� | �̬���ʳ�������������ľ�ҵȻ��ʩ�� | |
| C�� | ��ʯ����Ҫ�ɷ������Ի����� | |
| D�� | �Ӻ�ˮ�п���ȡ�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com