
工业酒精是含水约4%的液态乙醇。向工业酒精中加入生石灰,会发生化学反应[CaO+H2O====Ca(OH)2],且生成物不溶于乙醇。
(1)要在实验室中将工业酒精转化为无水乙醇,下列做法中不可取的是(填写代号)________。
A.加入过量的生石灰后过滤
B.加入过量的生石灰后蒸馏
C.加入过量的生石灰分液
(2)在你选择需要加热的实验方法中,需用的玻璃仪器除酒精灯以外,还有_____
_______;在该方法的实验步骤里,加热之前的操作是___________,并且对此要注意的问题是___________。
(3)用酒精灯作热源,在加热过程中要适当调整酒精灯的上下或左右位置,目的是 _______________________________________________________________。
.【解析】(1)CaO、Ca(OH)2是不溶于酒精、难挥发的固体,酒精是易挥发的液体。因此,可知采用蒸馏最佳。
(2)蒸馏操作中的玻璃仪器,不要答铁架台。在蒸馏操作中,为了确保馏出的蒸气及时得到冷却,要先向冷凝管内通冷却水,然后才能进行加热。为了提高冷却效果,冷却水应从冷凝管下口流入,上口流出。
(3)进行蒸馏操作时,要根据组分沸点,使蒸馏烧瓶内的支管口保持恒温。温度的显示靠温度计,温度的调节可通过控制热源的强弱来实现。
答案:(1)C (2)蒸馏烧瓶、温度计、冷凝管、牛角管、锥形瓶 向冷凝管内加冷却水 使水从冷凝管的下口进,上口出
(3)使蒸馏烧瓶内的支管口处保持某一恒温


科目:高中化学 来源: 题型:
下列各组离子在水溶液中能大量共存的是 ( )
A.Na+、Ba2+、Cl-、SO42- B. Ca2+、HCO3-、C1-、K+
C.Mg2+、Ag+、NO3-、Cl- D. H+ 、Cl- 、Na+ 、CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
空气质量越来越受到人们的关注,下表是我国部分城市空气质量周报:
| 城市 | 污染指数 | 首要污染物 | 空气质量等级 |
| 太原 | 98 | SO2 | Ⅱ |
| 青岛 | 47 | Ⅰ | |
| 兰州 | 103 | TSP | Ⅲ |
| 广州 | 90 | NOx | Ⅱ |
(注:TSP——总悬浮颗粒物;NOx——氮氧化物)
(1)由上表可知,从理论上分析最容易出现酸雨的城市是________。
(2)悬浮颗粒物不易沉降,它与空气中的SO2、O2接触时,SO2会部分转化为SO3,悬浮颗粒物所起的作用是________(填序号)。
A.氧化剂 B.还原剂 C.催化剂 D.吸附剂
(3)氮的氧化物也是大气污染物之一。目前,治理NO的方法是在一定条件下用氨把一氧化氮还原为氮气和水。科学家又设想,在相同条件下可采用价格比NH3更便宜的天然气来处理NO,达到同样效果,写出该反应的化学方程式________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
 下图为向25mL 0.1 mol·L-1 NaOH溶液中逐滴滴加0.2 mol·L-1 CH3COOH溶液过程中溶液pH的变化曲线。请回答:
下图为向25mL 0.1 mol·L-1 NaOH溶液中逐滴滴加0.2 mol·L-1 CH3COOH溶液过程中溶液pH的变化曲线。请回答:
(1)B点溶液呈中性,有人据此认为,在B点时NaOH与CH3COOH恰好完全反应,这种看法是否正确? (选填“是”或“否”)。若不正确,则二者恰好完全反应的点是在AB区间还是BD区间内? 区间(若正确,此问不答)
(2)AB区间,c(OH-)>c(H+),则c(OH-)与c(CH3COO-)大小关系是
A.c(OH-)一定大于c(CH3COO-)
B.c(OH-)一定小于c(CH3COO-)
C.c(OH-)一定等于c(CH3COO-)
D.c(OH-)大于、小于或等于c(CH3COO-)
(3)在D点时,溶液中c(CH3COO-)+c(CH3COOH) 2c(Na+)( “>”、“<”或“=”)
(4)常温下,将VmL、0.1000mol·L-1氢氧化钠溶液逐滴加入到20.00mL、0.1000mol·L-1醋酸溶液中,充分反应。回答下列问题。(忽略溶液体积的变化)
①如果溶液pH=7,此时V的取值__ ___20.00(填“>”、“<”或“=”),而溶液中c(Na+)、c(CH3COO-)、c(H+)、c(OH-)的大小关系为__________________________________。
②如果V=40.00,则此时溶液中c(OH-) -c(H+) - c(CH3COOH)= _________mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
现有三组溶液:①汽油和氯化钠溶液 ②39%的乙醇溶液 ③碘水溶液。分离以上各混合液的正确方法依次是( )
A.分液、萃取、蒸馏 B.萃取、蒸馏、分液
C.分液、蒸馏、萃取 D.蒸馏、萃取、分液
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数的值,下列说法中正确的是( )
A.62 g Na2O溶液于水后所得溶液中含有的O2-数为NA
B.标准状况下,6.72L NO2与水充分反应转移的电子数目为0.1NA
C.常温常压下,16g甲烷(12C1H4)所含的中子数为10NA
D.常温常压下,14g由N2和CO组成的混合气体含有的原子数目为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
为达到预期的实验目的,下列操作正确的是( )
A.欲配制量分数为10%的ZnSO4溶液,将10gZnSO4 7H2O溶解在90g水中
7H2O溶解在90g水中
B.欲制备Fe(OH)3胶体,向盛有沸水的烧杯中滴加FeC13饱和溶液并长时间煮沸
C.可以使用乙醇提取溴水中的溴单质
D.为鉴别KC1、A1C13和MgC12溶液,各取少量三种溶液分别滴加NaOH溶液至过量
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA代表阿伏伽德罗常数的值,下列说法正确的是( )
A.标准状况下,22.4L水所含的分子数为NA
B.17g NH3中所含的原子个数为4NA
C.1L、1mol/L的稀盐酸中含有的氯化氢分子数为NA
D.在反应2H2O2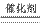 2 H2O+O2↑中每生成1mol O2转移的电子数为NA
2 H2O+O2↑中每生成1mol O2转移的电子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
近年来,科技人员研究得到一种新型材料——泡沫铝。它是把发泡剂加到熔融或固体粉末的铝合金中而制成的,其优点是硬度高,密度小(约为0.16克/厘米3~0.5克/厘米3),比木材还轻,可浮于水面,又有很大的刚性,且隔音、保温,是一种良好的建筑材料和轻质材料,可大批量投放市场。
(1)铝制成铝箔作食品包装,是利用它的( )。
A.金属光泽 B.延展性 C.导电性 D.导热性
(2)铝在空气中会被氧化生成一层致密的氧化膜(氧化物)而对铝起保护作用,但这层氧化膜(氧化物)遇到强酸或强碱都会溶解,且酸、碱均与铝制品发生反应,故不能用铝制品盛放酸性、碱性食品。
①写出铝与盐酸、NaOH溶液反应的化学方程式:________。
②等质量的A1分别加入0.3 L 1 mol/L的盐酸和NaOH溶液中,生成氢气的体积比为1∶2,则加入Al的质量为________。
A.2.7 g B.5.4 g C.8.1 g D.10 g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com