
����Ŀ���ܹ�ˮ���ij�л�������A�����ϣ��������к�̼Ϊ72.0%������Ϊ6.67%������ȫΪ�����������з����ⶨ���л����������Է��������ͷ��ӽṹ��
����һ��������������֪A����Է�������Ϊ150��
���������˴Ź����Dz��A�ĺ˴Ź���������5���壬�����֮��Ϊ1��2��2��2��3����ͼ1��
�����������ú�������Dz��A���ӵĺ��������ͼ2��


����գ�
��1��A�ķ���ʽΪ__��
��2��A�ķ�����ֻ��һ������������__(����ĸ)��
a.A����Է�������
b.A�ķ���ʽ
c.A�ĺ˴Ź�������ͼ
d.A���ӵĺ������ͼ
��3��A���ܵĽṹ��ʽΪ__��
���𰸡�C9H10O2 bc 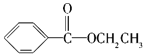 ��
��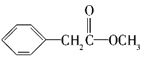 ��
��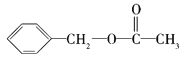
��������
(1)�����л����и�Ԫ�ص�������������Է�����������ȷ������ʽ��(2)���к���3����ԭ�ӣ����Ը����л�������ԭ����Ŀ���˴Ź�������ȷ��������Ŀ��(3)�����л���ķ���ʽ��Ϻ�������д��ڵĻ��ŷ����ṹ��ʽ��
(1) �л���A��Cԭ�Ӹ���N��C��=![]() ���л���A��Hԭ�Ӹ���N��H��=
���л���A��Hԭ�Ӹ���N��H��=![]() ���л���A��Oԭ�Ӹ���N��O��=
���л���A��Oԭ�Ӹ���N��O��=![]() �������л���A�ķ���ʽΪC9H10O2�����ʴ�Ϊ��C9H10O2��
�������л���A�ķ���ʽΪC9H10O2�����ʴ�Ϊ��C9H10O2��
(2) A�ĺ˴Ź���������5���壬˵����������5��Hԭ�ӣ������֮��Ϊ��Ӧ�ĸ���Hԭ�Ӹ���֮�ȣ��ɷ���ʽ��֪������Hԭ������������ȷ������Ŀ��������Ҫ֪��A�ķ���ʽ��A�ĺ˴Ź�������ͼ���ʴ�Ϊ��bc��
(3) ��A���ӵĺ������֪������C6H5C-��̼̼������C-H��C=O��C-O-C�Ȼ��ţ���ṹ�к������������ݺ˴Ź���������5����ԭ�ӣ��Һ���һ����������������ֻ��һ��ȡ�������Һ������������ܽṹ�� ��
�� ��
��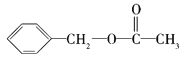 ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
�� ��
��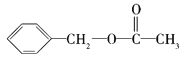 ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ˮ�к��зḻ��þ��Դ��ijͬѧ����˴�ģ�⺣ˮ���Ʊ�MgO��ʵ�鷽����

ģ�⺣ˮ�е�����Ũ��/mol��L��1 | Na�� | Mg2�� | Ca2�� | Cl�� | HCO3�� |
0.439 | 0.050 | 0.011 | 0.560 | 0.001 |
ע����Һ��ij�����ӵ�Ũ��С��1.0��10��5 mol��L��1������Ϊ�����Ӳ����ڣ�ʵ������У�������Һ������䡣Ksp[CaCO3]��4.96��10��9��Ksp[MgCO3]��6.82��10��6��Ksp[Ca(OH)2]��4.68��10��6��Ksp[Mg(OH)2]��5.61��10��12������˵����ȷ���ǣ� ��
A.������XΪCaCO3
B.��ҺM�д���Mg2����������Ca2��
C.��ҺN�д���Mg2����Ca2��
D.�����������Ϊ����4.2 g NaOH���壬������YΪCa(OH)2��Mg(OH)2�Ļ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ӻ�ۺ��������Ƕ���ʶ�ȡ�����������Ԫ�صĵ��ʼ��仯������ѧ����ѧ��ѧ����Ҫ���������������գ�
��1��Cl��Ԫ�����ڱ��е�λ��Ϊ______________���ɴ˿�֪��������������Ӧ��ˮ����Ļ�ѧʽ Ϊ��______________ ����������ӵĽṹʽΪ��_____________��
��2��Cl��S��Na����Ԫ���γɼ�������뾶�ɴ�С��˳����_______________________�������ӷ��� ��ʾ����������������Ӧ��ˮ������ֳ��˶��ص����ʣ�����ˮ��Һ�еĵ��뷽��ʽ Ϊ____________________________________________________________________________��
��3������ȵķǽ�����ǿ����ϵ��_________________���Դ�ԭ�ӽṹ�ĽǶȽ�����ԭ��______________
��4�������Լ�����ˮ��������Һ��Na2SO3��Һ��ϡ���ᡢNaOH��Һ����ˮ��Ҫ֤��Na2SO3���л�ԭ �ԣ�Ӧѡ�õ��Լ���______________�������������� ____________________��Ҫ֤��Na2SO3���������ԣ�Ӧѡ�õ��Լ���___________________����Ӧ�����ӷ���ʽ�� ________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��
��.���ڿ��淴ӦCO+H2O(g)![]() CO2+H2���ش��������⣺
CO2+H2���ش��������⣺
(1)830 Kʱ������ʼʱc(CO)=2 mol��L-1��c(H2O)=3 mol��L-1��ƽ��ʱCO��ת����Ϊ60%��ˮ������ת����Ϊ _____________;ƽ�ⳣ��K��ֵΪ _____________��
(2)830 Kʱ����ֻ����ʼʱc(H2O)��Ϊ6 mol��L-1����ˮ������ת����Ϊ_____________ ��
(3)��830 Kʱ��ijʱ�̻����ϵ�и������Ũ��Ϊc(CO2)=0.4 mol��L-1c(CO)=0.6 mol��L-1c(H2O)=3 mol��L-1��c(H2)=2 mol��L-1���ж�����ϵ�з�Ӧ���еķ���______________ (�����������������������������ﵽƽ����)��
��������ѹ�£���һ���ݻ��ɱ�������з������·�Ӧ��A(g)+B(g) ![]() C(g)
C(g)
(1)����ʼʱ����1mol A��1mol B���ﵽƽ�������a mol C����ʱA�����ʵ���Ϊ _______ mol��
(2)����ʼʱ����3mol A��3mol B���ﵽƽ�������C�����ʵ���Ϊ _______mol��
(3)����ʼʱ����x mol A2mol B��1mol C���ﵽƽ���A��C�����ʵ����ֱ�Ϊy mol��3a mol����x= ______��y= _________��
(4)����(3)��ƽ���������ټ���3mol C�����ٴδﵽƽ���C�����ʵ��������� _______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������ǹ�ҵ��������ȡ�������Ҫ;����ijͬѧ�ø�ԭ����ʵ����̽��������Ʊ������ʣ����������ͼ��ʾ��װ����
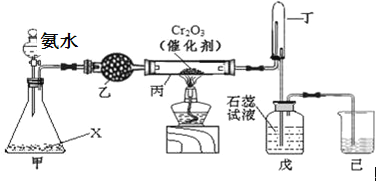
��1������Һ©���а�ˮ��Ũ��Ϊ9.0molL��1�����Ƹ�Ũ�ȵİ�ˮ100mL���õ��IJ���������100mL����ƿ���ձ����������� ��
��2����װ�ò���Ҫ���ȼ���ͬʱ������������������ƿ�ڹ���X������Ϊ ��
��3����װ�õ������� ��д������ʱ��װ�÷�����Ӧ�Ļ�ѧ����ʽΪ ��
��4�������й۲쵽 ������˵�����Ƶ�������ijͬѧ����ͼ��װ���������������Ժ����ʵ�飬û�й۲쵽�����������ʵ��ʧ�ܵĿ���ԭ�� ����θ����� ��
��5���Ľ������Ӧ����������װ�õ�����ʢˮ��ˮ���У���۲쵽�������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���¶��£���2 L�����ܱ������г���1mol A������A(g) ![]() B(g) + C(g)��Ӧ����Ӧ������c(C)��ʱ��仯����������ͼ��ʾ������˵������ȷ���ǣ� ��
B(g) + C(g)��Ӧ����Ӧ������c(C)��ʱ��仯����������ͼ��ʾ������˵������ȷ���ǣ� ��
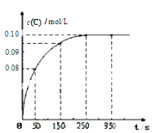
A����Ӧ�� 0 ~50 s ��ƽ������v(C)=1.6��10-3mo1/(L s)
B�����¶��£���Ӧ��ƽ�ⳣ��ֵΪ0.025
C����Ӧƽ������������г���A��B��C��1mol����ʱv(��)<v(��)
D�����������������䣬�����¶ȣ�ƽ��ʱc(B)=0.11mol/L����÷�Ӧ�ġ�H<0
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������0.1molL��1������Һ��pH=a��������ʹ��ҺpH=��a+1���Ĵ�ʩ��
A. ����Һϡ�͵�ԭ�����2��B. ���������Ĵ����ƹ���
C. ��������0.2 molL��1����D. ������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijʵ��С���о��¶ȶԻ�ѧ��Ӧ![]() ��Ӱ�죬������������ͬʱ����
��Ӱ�죬������������ͬʱ����![]() ��
��![]() �������Ϊ2L�ĺ����ܱ������У����
�������Ϊ2L�ĺ����ܱ������У����![]() �����ʵ���������ʱ��
�����ʵ���������ʱ��![]() �仯��ʵ���������£�
�仯��ʵ���������£�
ʱ�� | 0 | 20 | 40 | 60 | 80 | 100 | |
|
| 0 |
|
|
|
|
|
| 0 |
|
|
|
|
| |
����˵����ȷ���� ![]()
![]()
A. ![]() �¶��£�
�¶��£�![]() ֮�䣬
֮�䣬![]() ��ƽ����Ӧ����Ϊ
��ƽ����Ӧ����Ϊ![]()
B. ��![]() �¶��£��÷�Ӧ�п�����70minʱ�Ѵﵽƽ��״̬
�¶��£��÷�Ӧ�п�����70minʱ�Ѵﵽƽ��״̬
C. �ɱ��������Ʋ⣬![]()
D. �ɱ������ݿ�֪���¶�Խ�ߣ�![]() ��
��![]() �ķ�Ӧ��Խ��
�ķ�Ӧ��Խ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������������еķ�ӦΪ2NO2(g)��O3(g)![]() N2O5(g)��O2(g)�����˷�Ӧ�ں����ܱ������н��У����ͼ�����£����ж�Ӧ����������ȷ����(����)
N2O5(g)��O2(g)�����˷�Ӧ�ں����ܱ������н��У����ͼ�����£����ж�Ӧ����������ȷ����(����)
A.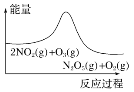 ƽ����£�NO2��������
ƽ����£�NO2��������
B.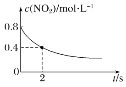 0��2 s�ڣ���(O3)��0.2 mol��L��1��s��1
0��2 s�ڣ���(O3)��0.2 mol��L��1��s��1
C.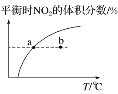 ������b��<a�㣬b�㣺����<����
������b��<a�㣬b�㣺����<����
D.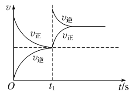 ���£�t1ʱ�ٳ���O3
���£�t1ʱ�ٳ���O3
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com