
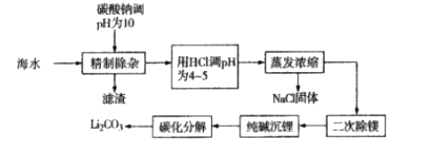
°æƒø°ø¥”∫£ÀÆ÷–÷»°≤¢÷∆±∏úÀ·ÔÆ£¨ø…“‘÷∏þ∫£ÀƵƒ◊€∫œ¿˚”√º€÷µ£¨¬˙◊„𧓵…œ∂‘úÀ·ÔƵƒ–Ë«Û°£÷∆±∏úÀ·ÔƵƒ“ª÷÷𧓒¡˜≥ûÁœ¬£∫
“—÷™£∫¢Ÿ∫£ÀÆ÷–ƒ≥–©¿Î◊”≈®∂»»Áœ¬£∫
¿Î◊” | Li+ | Mg2+ | Ca2+ | Mn2+ | Cl- |
≈®∂»(mol/L) | 0.113 | 0.049 | 0.001 | 0.010 | 0.501 |
¢⁄úÀ·ÔƵƒ»ÐΩ‚∂»£∫
Œ¬∂»(°Ê) | 0 | 10 | 30 | 50 | 70 | 90 |
»ÐΩ‚∂»(g/L) | 1.54 | 1.43 | 1.25 | 1.08 | 0.91 | 0.83 |
![]() º∏÷÷ƒ—»ÐµÁΩ‚÷ µƒ»Ð∂»ª˝(25°Ê)£∫
º∏÷÷ƒ—»ÐµÁΩ‚÷ µƒ»Ð∂»ª˝(25°Ê)£∫
ŒÔ÷ | Li2CO3 | MgCO3 | MnCO3 | CaCO3 | Mg(OH)2 |
Ksp | 2.5°¡10-2 | 6.8°¡10-6 | 2.3°¡10-11 | 2.8°¡10-9 | 6°¡10-10 |
«Îªÿ¥œ¬¡–Œ £∫
![]() æ´÷∆≥˝‘”Ω◊∂Œµƒ¬À‘¸Œ™MgCO3°¢______
æ´÷∆≥˝‘”Ω◊∂Œµƒ¬À‘¸Œ™MgCO3°¢______![]() –¥ªØ—ß Ω
–¥ªØ—ß Ω![]()
![]() ”√HClµ˜pHŒ™4°´5µƒƒøµƒ «_________°£
”√HClµ˜pHŒ™4°´5µƒƒøµƒ «_________°£
![]() ∂˛¥Œ≥˝√æπ˝≥Ã÷–£¨»Ù πMg2+≈®∂»Œ™6°¡10-4mol/L£¨”¶øÿ÷∆pHŒ™______°£
∂˛¥Œ≥˝√æπ˝≥Ã÷–£¨»Ù πMg2+≈®∂»Œ™6°¡10-4mol/L£¨”¶øÿ÷∆pHŒ™______°£
![]() ≥¡ÔÆΩ◊∂Œ£¨ µº ≤‚µ√≤ªÕ¨¥øºÓº”»Î¡øÃıº˛œ¬µƒÃºÀ·ÔÆ≥¡µÌΩ·π˚»Áœ¬±Ì£∫
≥¡ÔÆΩ◊∂Œ£¨ µº ≤‚µ√≤ªÕ¨¥øºÓº”»Î¡øÃıº˛œ¬µƒÃºÀ·ÔÆ≥¡µÌΩ·π˚»Áœ¬±Ì£∫
–Ú∫≈ |
| ≥¡µÌ÷ ¡ø(g) | Li2CO3∫¨¡ø(%) | Ôƪÿ ’¬ (%) |
0.9:2.0 | 10.09 | 92.36 | 77.67 | |
1.0:2.0 | 10.97 | 90.19 | 82.46 | |
1.1:2.0 | 11.45 | 89.37 | 85.27 | |
1.2:2.0 | 12.14 | 84.82 | 85.85 |
◊€∫œ“‘…œ–≈œ¢º∞øº¬« µº …˙≤˙ ±µƒ‘≠¡œ≥…±æ£¨”¶∞¥’’______![]() ÃÓ–Ú∫≈
ÃÓ–Ú∫≈![]() ÷–CO32-”ÎLi+ŒÔ÷ µƒ¡ø÷Ʊ»º”»Î¥øºÓ÷∆±∏úÀ·ÔÆ°£
÷–CO32-”ÎLi+ŒÔ÷ µƒ¡ø÷Ʊ»º”»Î¥øºÓ÷∆±∏úÀ·ÔÆ°£
![]() ≥¡ÔÆŒ¬∂»–Ëøÿ÷∆‘⁄
≥¡ÔÆŒ¬∂»–Ëøÿ÷∆‘⁄![]() £¨÷˜“™‘≠“Ú «______°£
£¨÷˜“™‘≠“Ú «______°£
![]() úªØ∑÷Ω‚æþÃÂπ˝≥ÃŒ™£∫¢ŸœÚúÀ·ÔÆ”ÎÀƵƒΩ¨¡œ÷–Õ®»ÎCO2∆¯Ã£¨≥‰∑÷∑¥”¶∫Û£¨π˝¬À£ª¢⁄º”»»¬À“∫ π∆‰∑÷Ω‚°£–¥≥ˆ¢⁄∑¥”¶÷–µƒªØ—ß∑Ω≥Ã Ω£∫__________°£–¥≥ˆ‘⁄úªØ∑÷Ω‚÷–ø…—≠ª∑¿˚”√ŒÔ÷ µƒµÁ◊” Ω£∫_________°£
úªØ∑÷Ω‚æþÃÂπ˝≥ÃŒ™£∫¢ŸœÚúÀ·ÔÆ”ÎÀƵƒΩ¨¡œ÷–Õ®»ÎCO2∆¯Ã£¨≥‰∑÷∑¥”¶∫Û£¨π˝¬À£ª¢⁄º”»»¬À“∫ π∆‰∑÷Ω‚°£–¥≥ˆ¢⁄∑¥”¶÷–µƒªØ—ß∑Ω≥Ã Ω£∫__________°£–¥≥ˆ‘⁄úªØ∑÷Ω‚÷–ø…—≠ª∑¿˚”√ŒÔ÷ µƒµÁ◊” Ω£∫_________°£
°æ¥∞∏°øMnCO3°¢CaCO3 ≥˝»•ÃºÀ·∏˘£¨∑¿÷π’Ù∑¢≈®Àı ±Li2CO3∫ÕNa2CO3Œˆ≥ˆ 11 ¢€ ∏√Œ¬∂»œ¬£¨ÃºÀ·ÔƵƒ»ÐΩ‚∂»∏¸–°£¨ø…“‘‘ˆº”≤˙¬ ![]() ªÚªÿ ’¬
ªÚªÿ ’¬ ![]() 2LiHCO3
2LiHCO3![]() Li2CO3+CO2°¸+H2O
Li2CO3+CO2°¸+H2O ![]()
°æΩ‚Œˆ°ø
¥”∫£ÀÆ÷–÷»°≤¢÷∆±∏úÀ·ÔÆ£¨π§“’¡˜≥õƒƒøµƒ «÷∆±∏Li2CO3£¨∫£ÀÆÕ®π˝º”»ÎúÀ·ƒ∆µ˜Ω⁄pHŒ™10£¨∆‰÷–Mg2+°¢Mn2+º∞Ca2+æ˘…˙≥…úÀ·—Œ≥¡µÌ◊˜Œ™¬À‘¸≥˝»•£¨¬À“∫÷–¥Ê‘⁄Li+£¨π˝¡øµƒÃºÀ·ƒ∆£¨‘Ÿ”√—ŒÀ·µ˜Ω⁄pHŒ™4°´5£¨≥˝»•π˝¡øµƒÃºÀ·ƒ∆£¨‘Ÿæ≠π˝∏þŒ¬≈®Àıµ√µΩNaClæßã¨∂˛¥Œ≥˝√棨¥À ±¬À“∫÷–¥Ê‘⁄Ωœ¥øµƒLi+£¨‘Ÿ”√¥øºÓ–Œ≥…Li2CO3£¨‘⁄æ≠π˝ÃºªØ∑÷Ω‚π˝≥Ã◊Ó÷’÷∆µ√Ωœ¥øµƒLi2CO3£¨æð¥À∑÷Œˆ£¨
(1)¡˜≥õƒƒøµƒ «÷∆±∏÷¥øLi+£¨‘ÚMn2+°¢Mg2+∫ÕCa2+æ˘Œ™‘”÷ ¿Î◊”£¨æ´÷∆≥˝‘”Ω◊∂Œµ˜Ω⁄pHŒ™10£¨÷˜“™≥˝»•Mg2+°¢Mn2+∫ÕCa2+£ª
(2)”√HClµ˜pHŒ™4°´5£¨¥À ±»Ð“∫Œ™À·–‘£¨»Ð“∫÷–¥Ê‘⁄π˝¡øµƒNa2CO3£ª
(3)∏˘æðMg(OH)2µƒ»Ð∂»ª˝≥£ ˝º∆À„£ª
(4)“™«Ûæ°ø…ƒÐ∏þµƒªÿ ’Li+£¨‘⁄∏þªÿ ’¬ œý≤Ó≤ª¥Û«Èøˆœ¬£¨‘Ÿøº¬« π”√Ωœ…Ÿµƒ¥øºÓ£ª
(5)≥¡ÔÆŒ¬∂»–Ëøÿ÷∆‘⁄90°Ê£¨øº¬«µΩÀÊ◊≈Œ¬∂»…˝∏þ£¨Li2CO3»ÐΩ‚∂»ΩµµÕ£ª
(6)œÚúÀ·ÔÆ”ÎÀƵƒΩ¨¡œ÷–Õ®»ÎCO2∆¯Ã£¨≥‰∑÷∑¥”¶∫Û£¨π˝¬Àµ√µΩLiHCO3£¨º”»»LiHCO3ø…“‘∑¢…˙∑÷Ω‚£¨≤˙…˙Li2CO3°¢CO2£¨µ√µΩµƒCO2ø…“‘—≠ª∑ π”√£¨∏˘æð∞À”Á¬… È–¥CO2µƒµÁ◊” Ω°£
(1)¡˜≥õƒƒøµƒ «÷∆±∏÷¥øLi+£¨‘ÚMn2+°¢Mg2+∫ÕCa2+æ˘Œ™‘”÷ ¿Î◊”£¨æ´÷∆≥˝‘”Ω◊∂Œµ˜Ω⁄pHŒ™10£¨÷˜“™≥˝»•Mg2+°¢Mn2+∫ÕCa2+£¨∑÷±–Œ≥…MgCO3°¢MnCO3∫ÕCaCO3£ª
(2)”√HClµ˜pHŒ™4°´5£¨¥À ±»Ð“∫Œ™À·–‘£¨»Ð“∫÷–¥Ê‘⁄π˝¡øµƒNa2CO3£¨ø…“‘≥˝»•π˝¡øµƒNa2CO3£¨∑¿÷π’Ù∑¢≈®Àı ±Li2CO3∫ÕNa2CO3Œˆ≥ˆ£ª
(3)∂˛¥Œ≥˝√æπ˝≥Ã÷–£¨»Ù πMg2+≈®∂»Œ™6°¡10-4mol/L£¨‘Ú¥À ±»Ð“∫÷–c(OH-)=![]() =10-3mol/L£¨À˘“‘øÿ÷∆»Ð“∫pH=11£ª
=10-3mol/L£¨À˘“‘øÿ÷∆»Ð“∫pH=11£ª
(4)“™«Ûæ°ø…ƒÐ∏þµƒªÿ ’Li+£¨‘⁄∏þªÿ ’¬ œý≤Ó≤ª¥Û«Èøˆœ¬£¨‘Ÿøº¬« π”√Ωœ…Ÿµƒ¥øºÓ£¨◊€∫œøº¬«”¶∞¥¢€Õ∂»Î¥øºÓ≤Œº”∑¥”¶£ª
(5)≥¡ÔÆŒ¬∂»–Ëøÿ÷∆‘⁄90°Ê£¨øº¬«µΩÀÊ◊≈Œ¬∂»…˝∏þ£¨Li2CO3»ÐΩ‚∂»ΩµµÕ£¨À˘“‘Œ¬∂»øÿ÷∆‘⁄90°Ê ±£¨ÃºÀ·ÔƵƒ»ÐΩ‚∂»∏¸–°£¨ø…“‘‘ˆº”≤˙¬ (ªÚªÿ ’¬ )£ª
(6)œÚúÀ·ÔÆ”ÎÀƵƒΩ¨¡œ÷–Õ®»ÎCO2∆¯Ã£¨≥‰∑÷∑¥”¶∫Û£¨π˝¬Àµ√µΩLiHCO3£¨º”»»LiHCO3ø…“‘∑¢…˙∑÷Ω‚£¨≤˙…˙Li2CO3°¢CO2£¨‘Ú∑¢…˙µƒ∑¥”¶Œ™£∫2LiHCO3![]() Li2CO3+CO2°¸+H2O£¨µ√µΩµƒCO2ø…“‘—≠ª∑ π”√£¨CO2µƒµÁ◊” ΩŒ™£∫
Li2CO3+CO2°¸+H2O£¨µ√µΩµƒCO2ø…“‘—≠ª∑ π”√£¨CO2µƒµÁ◊” ΩŒ™£∫![]() °£
°£


 ∆⁄ƒ©1æÌÀÿ÷ ΩÔ˝∆¿π¿æÌœµ¡–¥∞∏
∆⁄ƒ©1æÌÀÿ÷ ΩÔ˝∆¿π¿æÌœµ¡–¥∞∏
| ƒÍº∂ | ∏þ÷–øŒ≥à | ƒÍº∂ | ≥ı÷–øŒ≥à |
| ∏þ“ª | ∏þ“ª√‚∑—øŒ≥ÃÕ∆ºˆ£° | ≥ı“ª | ≥ı“ª√‚∑—øŒ≥ÃÕ∆ºˆ£° |
| ∏þ∂˛ | ∏þ∂˛√‚∑—øŒ≥ÃÕ∆ºˆ£° | ≥ı∂˛ | ≥ı∂˛√‚∑—øŒ≥ÃÕ∆ºˆ£° |
| ∏þ»˝ | ∏þ»˝√‚∑—øŒ≥ÃÕ∆ºˆ£° | ≥ı»˝ | ≥ı»˝√‚∑—øŒ≥ÃÕ∆ºˆ£° |
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°ø(NH4)2Cr2O7”√”⁄”–ª˙∫œ≥…¥þªØº¡£¨√Ω»æº¡£¨œ‘”∞“∫µ»°£ƒ≥ªØ—ß–À»§–°◊È∂‘(NH4)2Cr2O7µƒ≤ø∑÷–‘÷ º∞◊È≥…Ω¯––ÃΩæø°£“—÷™£∫Cr2O72£≠(≥»…´)+H2O![]() 2CrO42£≠(ª∆…´)+2H+°£ªÿ¥œ¬¡–Œ £∫
2CrO42£≠(ª∆…´)+2H+°£ªÿ¥œ¬¡–Œ £∫
(1)‘⁄ ‘πÐ÷–º”»Î…Ÿ¡ø(NH4)2Cr2O7πÃ㨵Œº”◊„¡ø≈®KOH»Ð“∫£¨’Òµ¥°¢Œ¢»»£¨π€≤ÏµΩµƒ÷˜“™œ÷œÛ «πÃûÐΩ‚°¢__________°¢__________°£
(2)Œ™ÃΩæø(NH4)2Cr2O7 (ƒ¶∂˚÷ ¡ø252g/mol)µƒ∑÷Ω‚≤˙ŒÔ£¨∞¥œ¬Õº¡¨Ω”∫√◊∞÷√£¨‘⁄A÷–º”»Î5.040g—˘∆∑Ω¯–– µ—È°£
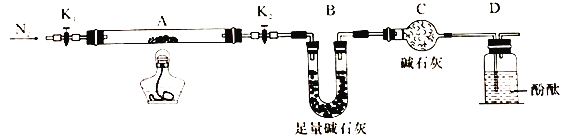
¢Ÿ“«∆˜Bµƒ√˚≥∆ «__________°£
¢⁄º”»»A÷¡∫„÷ÿ£¨π€≤ϵΩD÷–»Ð“∫≤ª±‰…´£¨Õ¨ ±≤‚µ√A°¢B÷–÷ ¡ø±‰ªØ∑÷±Œ™2.00g°¢1.44g£¨–¥≥ˆ÷ÿ∏ıÀ·Ôߺ”»»∑÷Ω‚∑¥”¶µƒªØ—ß∑Ω≥à Ω____________________°£
¢€Cµƒ◊˜”√ «__________°£
(3) µ—È “≥£”√º◊»©∑®≤‚∂®∫¨(NH4)2Cr2O7µƒ—˘∆∑÷–µ™µƒ÷ ¡ø∑÷ ˝£¨∆‰∑¥”¶‘≠¿ÌŒ™£∫2Ba2++Cr2O72£≠+H2O=2BaCrO4°˝+2H+°¢ 4NH4++6HCHO =3H++6H2O+(CH2)6N4H+[µŒ∂® ±£¨1mol(CH2)6N4H+”Î1molH+œýµ±]£¨»ª∫Û”√NaOH±Í◊º»Ð“∫µŒ∂®∑¥”¶…˙≥…µƒÀ·°£
µ—È≤Ω÷Ë£∫≥∆»°—˘∆∑2.800g£¨≈‰≥…250mL»Ð“∫£¨“∆»°25.00mL—˘∆∑»Ð“∫”⁄250mL◊∂–Œ∆ø÷–£¨”√¬»ªØ±µ»Ð“∫ πCr2O72£≠ÕÍ»´≥¡µÌ∫Û£¨º”»Î10mL20%µƒ÷––‘º◊»©»Ð“∫£¨“°‘»°¢æ≤÷√5min∫Û£¨º”»Î1°´2µŒ∑”Ù ‘“∫£¨”√0.200 mol°§L£≠1 NaOH±Í◊º»Ð“∫µŒ∂®÷¡÷’µ„°£÷ÿ∏¥…œ ˆ≤Ÿ◊˜3¥Œ°£
¢ŸºÓ ΩµŒ∂®πД√’Ù¡ÛÀÆœ¥µ”∫Û£¨÷±Ω”º”»ÎNaOH±Í◊º»Ð“∫Ω¯––µŒ∂®£¨‘ÚµŒ∂® ±”√»•NaOH±Í◊º»Ð“∫µƒÃª˝__________ (ÃÓ°∞∆´¥Û°±°¢°∞∆´–°°±ªÚ°∞ŒÞ”∞œÏ°±)£ªµŒ∂® ±±þµŒ±þ“°∂Ø◊∂–Œ∆ø£¨—€æ¶”¶π€≤Ï__________°£
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°ø”√NA¥˙±Ì∞¢∑¸º”µ¬¬Þ≥£ ˝µƒ ˝÷µ°£œ¬¡–Àµ∑®÷–£¨’˝»∑µƒ «£® £©
A.2.3gΩ Ùƒ∆”…‘≠◊”ÕÍ»´±‰≥…¿Î◊” ±£¨µ√µΩµƒµÁ◊” ˝Œ™0.1NA
B.0.2NA∏ˆ¡ÚÀ·∑÷◊””Î19.6¡◊À·£®H3PO4£©∫¨”–œýÕ¨µƒ—ı‘≠◊” ˝
C.28gµ™∆¯À˘∫¨µƒ‘≠◊” ˝Œ™NA
D.NA∏ˆ—ı∆¯∑÷◊””ÎNA∏ˆ«‚∆¯∑÷◊”µƒ÷ ¡ø±»Œ™8°√1
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°ø£®1£©Õ¨Œ¬Õ¨—πœ¬£¨Õ¨Ãª˝µƒº◊ÕÈ(CH4)∫Õ∂˛—ıªØú‘≠◊”◊Ð ˝÷Ʊ»Œ™_____£¨√Ð∂»÷Ʊ»Œ™_____°£
£®2£©‘⁄±Í◊º◊¥øˆœ¬£¨CO∫ÕCO2µƒªÏ∫œ∆¯ÃÂπ≤39.2L£¨÷ ¡øŒ™61g£¨‘Ú∆‰÷–CO2Œ™____ mol°£
£®3£©9.03°¡1023∏ˆNH3∫¨___mol«‚‘≠◊”£¨‘⁄±Í◊º◊¥øˆœ¬µƒÃª˝Œ™____L°£
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°ø‘⁄»˝∏ˆ»ðª˝æ˘Œ™2 Lµƒ√б’»ð∆˜÷–∞¥≤ªÕ¨∑Ω ΩÕ∂»Î∑¥”¶ŒÔ£¨∑¢…˙∑¥”¶£∫
CO(g)£´H2O(g) ![]() CO2(g)£´H2(g)°°¶§H£Ω£≠a kJ°§mol£≠1(a>0)
CO2(g)£´H2(g)°°¶§H£Ω£≠a kJ°§mol£≠1(a>0)
œýπÿ∑¥”¶ ˝æð»Áœ¬£∫
»ð∆˜ | »ð∆˜¿ý–Õ | ∆ ºŒ¬∂»/ | ∆ ºŒÔ÷ µƒ¡ø/mol | ∆Ω∫‚ ±H2ŒÔ÷ µƒ¡ø/mol | |||
CO | H2O | CO2 | H2 | ||||
¢Ò | ∫„Œ¬∫„»ð | 800 | 1.2 | 0.6 | 0 | 0 | 0.4 |
¢Ú | ∫„Œ¬∫„»ð | 900 | 0.7 | 0.1 | 0.5 | 0.5 | |
¢Û | 毻»∫„»ð | 800 | 0 | 0 | 1.2 | 0.8 | |
œ¬¡–Àµ∑®’˝»∑µƒ «(°°°°)
A. »ð∆˜¢Ò÷–∑¥”¶æ≠10 minΩ®¡¢∆Ω∫‚£¨0°´10 minƒ⁄£¨∆Ωæ˘∑¥”¶ÀŸ¬ v(CO)£Ω0.04 mol°§L£≠1°§in£≠1
B. »ÙœÚ»ð∆˜¢Ò∆Ω∫‚ÃÂœµ÷–‘Ÿº”»ÎCO°¢H2O°¢CO2°¢H2∏˜0.1 mol£¨∆Ω∫‚Ω´’˝œÚ“∆∂Ø
C. ¥ÔµΩ∆Ω∫‚ ±£¨»ð∆˜¢Ú÷–∑¥”¶Œ¸ ’µƒ»»¡ø–°”⁄0.1a kJ
D. ¥Ô∆Ω∫‚ ±£¨»ð∆˜¢Û÷–n(CO)<0.48 mol
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°ø(1) µ—È “≥£”√≈®¡ÚÀ·µƒ÷ ¡ø∑÷ ˝Œ™98%£¨√Ð∂»Œ™1.80 g°§mL1£¨∆‰ŒÔ÷ µƒ¡ø≈®∂» «_______°£
(2)±Í◊º◊¥øˆœ¬£¨Ω´V L A∆¯ÃÂ(ƒ¶∂˚÷ ¡øŒ™M g/mol)ÕÍ»´»Ð”⁄0.1 LÀÆ(√Ð∂»1 g/cm3)÷–£¨À˘µ√»Ð“∫µƒ√Ð∂»Œ™d g/mL£¨‘Ú¥À»Ð“∫µƒŒÔ÷ µƒ¡ø≈®∂»Œ™_______mol/L°£
A£ÆVd/(MV+2240) B£Æ1000Vd/(MV+2240) C£Æ1000VdM/(MV+2240) D£ÆMV/22.4(V+0.1)d
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°ø “Œ¬œ¬£¨[Cu(NH3)4](NO3)2”Γ∫∞±ªÏ∫œ≤¢º”»ÎCuø…÷∆µ√“ª÷÷∫⁄¬Ã…´æßð£
(1) ª˘Ã¨Cu2£´∫ÀÕ‚µÁ◊”≈≈≤º Ω «________°£
(2) ∫⁄¬Ã…´æßõƒæß∞˚»ÁÕºÀ˘ 棨–¥≥ˆ∏√æßõƒªØ—ß Ω£∫____°£

(3) ≤ªøº¬«ø’º‰ππ–Õ£¨[Cu(NH3)4]2£´µƒΩ·ππø…”√ æ“‚Õº±Ì 挙__________________(”√°∞°˙°±±Í≥ˆ∆‰÷–µƒ≈‰Œªº¸)°£
(4) NO3-÷–N‘≠◊”πϵ¿µƒ‘”ªØ¿ý–Õ «____°£”ÎNO3-ª•Œ™µ»µÁ◊”õƒ“ª÷÷∑÷◊”Œ™____(Ãѧ Ω)°£
(5) “∫∞±ø…◊˜÷∆¿‰º¡£¨∆¯ªØ ±Œ¸ ’¥Û¡ø»»¡øµƒ‘≠“Ú «___________________________________________°£
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°øÓ—º∞Ó—∫œΩ‘⁄∫Ωø’∫ΩÃÏ¡Ï≥«æþ”–÷ÿ“™µƒ”¶”√º€÷µ°£Ó—Ã˙øÛ÷˜“™≥…∑÷Œ™Ó—À·—«Ã˙(FeTiO3)£¨¡Ì∫¨”–…Ÿ¡øSiO2°¢Fe2O3µ»‘”÷ °£“‘Ó—Ã˙øÛŒ™‘≠¡œ÷∆±∏Ó—µƒπ§“’¡˜≥ûÁœ¬ÕºÀ˘ æ°£
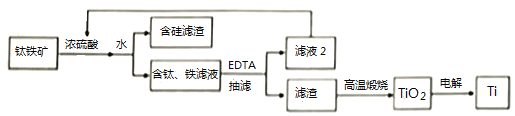
(1)Œ™Ã·∏þÓ—Ã˙øÛÀ·Ω˛ ±µƒΩ˛≥ˆ¬ £¨≥˝¡À≤…”√—≠ª∑Ω˛»°°¢—”≥§ ±º‰°¢»€øÈ∑€ÀÈÕ‚£¨ªπø…“‘≤…”√______________________(–¥“ª÷÷∑Ω∑®)°£
(2)¡ÚÀ·÷ ¡ø∑÷ ˝∂‘Ó—°¢Ã˙Ω˛≥ˆ¬ µƒ”∞œÏ»ÁÕºÀ˘ 棨æð¥À≈–∂œ£¨À·Ω˛ ±À˘º”¡ÚÀ·µƒ÷ ¡ø∑÷ ˝”¶Œ™___________°£
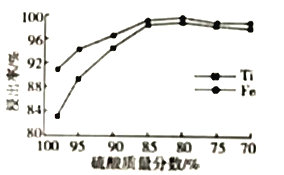
Ó—Ã˙øÛ÷˜“™≥…∑÷”Î≈®¡ÚÀ·∑¥”¶µƒ÷˜“™≤˙ŒÔ «TiOSO4∫ÕFeSO4£¨∏√∑¥”¶µƒªØ—ß∑Ω≥Ã Ω£∫______________________°£
(3)≤È‘ƒ◊ ¡œø…÷™£∫TiO2+”ÎFe3+ÀÆΩ‚◊™ªØŒ™≥¡µÌµƒpHΩ”Ω¸£ª∑¥”¶¢ŸFe3++H2Y2===FeY£≠+2H+£¨K=1024.3)£ª∑¥”¶¢⁄TiO2++H2Y2£≠=== TiO Y2£≠+2H+£¨K=1017.3°£∫¨Ó—Ã˙»Ð“∫æ≠EDTA(H2Y2£≠)¥¶¿Ì∫Û‘Ÿµ˜Ω⁄pH£¨TiO2+ÀÆΩ‚…˙≥…∆´Ó—À·[TiO (OH)2]≥¡µÌ£¨‘ÚTiO2+ÀÆΩ‚µƒ¿Î◊”∑Ω≥Ã ΩŒ™£∫___________£ªFe3+Œ¥◊™ªØŒ™≥¡µÌµƒ‘≠“Ú «______________________°£
(4)»ÙΩ´¬À“∫2æ≠___________¿‰»¥Ω·æß°¢π˝¬À“ªœµ¡–≤Ÿ◊˜ªπø…ªÒµ√∏±≤˙∆∑¬Ã∑Ø(FsO4°§7H2O)°£¬À“∫2æ≠¥¶¿Ì∫Û£¨ªπø…∑µªÿ¡˜≥Ã÷– π”√µƒŒÔ÷ «______________________°£
(5)¿˚”√œ¬ÕºÀ˘ æ◊∞÷√‘⁄“ª∂®Ãıº˛œ¬”…TiO2÷∆»°Ω ÙÓ—µƒªØ—ß∑Ω≥Ã ΩŒ™__________________°£—Ùº´µƒµÁº´∑¥”¶ ΩŒ™______________________°£

≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°ø µ—È “÷∆»°¬»∆¯”–œ¬¡–∑¥”¶£∫2KMnO4+16HCl(≈®)=2MnCl2+2KCl+5Cl2°¸+8H2O
£®1£©∏√∑¥”¶÷–—ıªØº¡ «____£ª±ªªπ‘≠µƒ‘™Àÿ «______£ª—ıªØ≤˙ŒÔ «_______°£
£®2£©”√µ•œþ«≈∑®±Í≥ˆµÁ◊”◊™“∆µƒ∑ΩœÚ∫Õ ˝ƒø£∫2KMnO4+16HCl£®≈®£©=2MnCl2+2KCl+5Cl2°¸+8H2O______
£®3£©∏√∑¥”¶”–1molKMnO4≤Œº”∑¥”¶£¨±ª—ıªØµƒHClŒ™____mol£¨◊™“∆µÁ◊”____mol°£
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
∞Ÿ∂»÷¬–≈ - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com